Den offisielle nomenklaturen for etrene, ifølge IUPAC, kan gjøres på to måter. Se hver enkelt:
1. vei:

Eksempler:
CH3 — O — CH2 — CH3→ møttesoxyetenO
CH3 — CH2 — O — CH2 —CH3→ etoxyetenO
CH3 — CH2 — O — CH2— CH2 —CH3→etoxyrekvisittenO
CH3 — O — CH2— CH═CH —CH3→ møttesoxymennoO
CH3 — CH2 — CH2 — O — CH2— CH2 — CH2 — CH2 — CH3→rekvisittoxypentenO
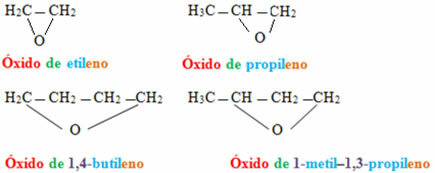
Hvis de er etere av lukkede kjeder, nomenklaturen vil være annerledes:

Eksempler:
Ikke stopp nå... Det er mer etter annonseringen;)
2. vei:
De to gruppene som er koblet til oksygen blir betraktet som substituenter, og blir angitt i rekkefølgen av kompleksiteten med suffikset jegdet vil si at den følger følgende regel:
eter + 1. gruppe + 2. gruppe + jeg
Disse gruppene skal vises og
Eksempler:
CH3— O —CH2 —CH3→ eter etyljeg og metyljeg
CH3 —CH2—O —CH2 —CH3→eterdietyljeg
CH3 —CH2—O —CH2—CH2 —CH3→eteretyljeg og propilejeg
CH3 —CH2 —CH2—O —CH2—CH2 —CH2 —CH2 —CH3→eterpropilejeg og pentyljeg
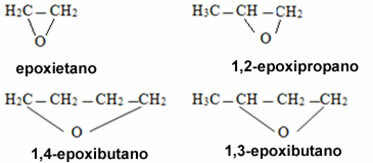
Når det gjelder sykliske forbindelser, kalles de epoksider:
Av Jennifer Fogaça
Uteksamen i kjemi
Vil du referere til denne teksten i et skole- eller akademisk arbeid? Se:
FOGAÇA, Jennifer Rocha Vargas. "Eternes nomenklatur"; Brasilskolen. Tilgjengelig i: https://brasilescola.uol.com.br/quimica/nomenclatura-dos-Eteres.htm. Tilgang 27. juni 2021.
Basenomenklatur, vandig oppløsning, ionisk dissosiasjon, kation, anion, natriumhydroksid, aluminiumhydroksid, jernhydroksid, kobberhydroksid, jernhydroksid, kalsiumhydroksid.