ქიმიური ბალანსი ერთ-ერთი საგანია, რომელიც ყველაზე მეტად ეცემა Enem და მისაღები გამოცდების დროს.
შექცევადი რეაქციების ასპექტებს კითხვებში აქვს განხილული და კანდიდატებს აფასებენ როგორც გამოთვლებით, ასევე კონცეფციებით, რომლებიც მოიცავს ამ თემას.
ამის გათვალისწინებით, ჩვენ შევადგინეთ კითხვების ეს სია, ქიმიური ბალანსის სხვადასხვა მიდგომით.
ისარგებლეთ რეზოლუციის კომენტარებით, რომ მოემზადოთ გამოცდებისთვის და გაეცნოთ ნაბიჯ-ნაბიჯ ინსტრუქციას კითხვების გადაჭრის შესახებ
ქიმიური წონასწორობის ზოგადი ცნებები
1. (უემა) განტოლებაში , ქიმიური წონასწორობის მიღწევის შემდეგ, შეგვიძლია დავასკვნათ წონასწორობის მუდმივა
, რომლის შესახებაც სწორია იმის თქმა, რომ:
ა) რაც უფრო მაღალია Kc მნიშვნელობა, მით უფრო დაბალია პირდაპირი რეაქციის მოსავლიანობა.
ბ) კჩ ტემპერატურის მიუხედავად.
გ) თუ წინ და შებრუნებული რეაქციების სიჩქარე ტოლია, მაშინ Kc = 0.
დ) კჩ ეს დამოკიდებულია რეაქტორების საწყის მოლარობაზე.
ე) რაც უფრო დიდია Kc მნიშვნელობა, მით მეტია პროდუქტების კონცენტრაცია.
სწორი პასუხი: ე) რაც მეტია Kc მნიშვნელობა, მით მეტია პროდუქტების კონცენტრაცია.
პირდაპირი რეაქცია წარმოდგენილია ნომრით 1, სადაც:
შებრუნებული რეაქცია წარმოდგენილია იმით
K– ს მნიშვნელობაჩ იგი გამოითვლება პროდუქციისა და რეაგენტების კონცენტრაციას შორის თანაფარდობით.
მრიცხველი (რომელიც შეიცავს პროდუქტებს) წონასწორობის მუდმივის პირდაპირპროპორციულია. ამიტომ, რაც უფრო მეტია K მნიშვნელობაჩ, რაც მეტია პირდაპირი რეაქციის მოსავლიანობა, რადგან უფრო მეტი პროდუქტი იქმნება და, შესაბამისად, უფრო მეტია პროდუქციის კონცენტრაცია.
K– ს მნიშვნელობაჩ იცვლება ტემპერატურის მიხედვით, რადგან მისი მნიშვნელობის შეცვლისას ენდოთერმული (სითბოს შეწოვა) ან ეგზოთერმული (სითბოს გამოყოფა) რეაქცია შეიძლება იყოს სასურველია და, ამით, უფრო მეტი რეაგენტის ან პროდუქტის მოხმარება ან შექმნა შეიძლება, შესაბამისად შეიცვლება წონასწორობის მუდმივა, რაც დამოკიდებულია კონცენტრაციაზე რეაგენტები.
Kc დამოკიდებულია კომპონენტების მოლურ რაოდენობაზე, როდესაც წონასწორობა დამყარდება და როდესაც წინა და უკუ რეაქციების სიჩქარე ტოლია.
2. (UFRN) ქიმიური ბალანსი ხასიათდება მიკროსკოპულ დონეზე დინამიურად. ქიმიური წონასწორობის მასშტაბის შესახებ რაოდენობრივი ინფორმაციის მისაღებად გამოიყენება წონასწორობის მუდმივი რაოდენობა. განვიხილოთ შემდეგი ზოლები:

გამოიყენება ქიმიური ბალანსი, პერსონაჟის იდეა ბალანსი:
ა) სწორია, რადგან ქიმიური წონასწორობისას, ნახევარი თანხა ყოველთვის პროდუქტია, ხოლო მეორე ნახევარი რეაქტიულია.
ბ) ეს არ არის სწორი, ვინაიდან, ქიმიური წონასწორობის პირობებში, პროდუქტებისა და რეაქტიული ნივთიერებების კონცენტრაცია შეიძლება იყოს განსხვავებული, მაგრამ ისინი მუდმივია.
გ) სწორია, რადგან ქიმიური წონასწორობის დროს რეაქტივებისა და პროდუქტების კონცენტრაცია ყოველთვის ერთი და იგივეა, სანამ წონასწორობა არ დაირღვევა გარე ეფექტით.
დ) ეს არ არის სწორი, რადგან, ქიმიური წონასწორობისას, პროდუქციის კონცენტრაცია ყოველთვის უფრო მაღალია, ვიდრე რეაქტიული ნივთიერებები, სანამ წონასწორობა გავლენას არ ახდენს გარე ფაქტორზე.
ე) სწორია, რადგან ქიმიური წონასწორობისას რეაქტივებისა და პროდუქტების კონცენტრაცია ყოველთვის ერთნაირი არ არის.
სწორი პასუხი: ბ) ეს არ არის სწორი, ვინაიდან, ქიმიური წონასწორობის პირობებში, პროდუქტებისა და რეაქტიული ნივთიერებების კონცენტრაცია შეიძლება იყოს განსხვავებული, მაგრამ ისინი მუდმივია.
წონასწორობის პირობებში პროდუქტებისა და რეაგენტების რაოდენობა შეიძლება გამოითვალოს მუდმივის საფუძველზე ბალანსი, და სულაც არ უნდა იყოს პროდუქციის ნახევარი და მეორე ნახევარი რეაგენტები.
წონასწორობის კონცენტრაცია ყოველთვის ერთი და იგივე არ არის, ისინი შეიძლება განსხვავებული იყოს, მაგრამ მუდმივია, თუ წონასწორობაში არ ხდება რაიმე დარღვევები.
წონასწორობის კონცენტრაცია უნდა იყოს დამოკიდებული იმაზე, თუ რომელი რეაქციაა სასურველი, პირდაპირი იქნება თუ ინვერსიული. ეს შეგვიძლია ვიცოდეთ K მნიშვნელობითჩ: თუ კჩ 1, სასურველია პირდაპირი რეაქცია. უკვე თუ კჩ
1 სასურველია საპირისპირო რეაქცია.
ქიმიური ბალანსის დიაგრამები
3. (UFPE) მე -20 საუკუნის დასაწყისში, პირველი მსოფლიო ომის მოლოდინმა აზოტის ნაერთების დიდი მოთხოვნილება გამოიწვია. ჰაბერმა წამოიწყო ჰაერში აზოტისგან ამიაკის წარმოება. თუ ამიაკი მოთავსებულია დახურულ ჭურჭელში, ის იშლება შემდეგი გაუწონასწორებელი ქიმიური განტოლების შესაბამისად: NH3(ზ) ნ2 (გ) + თ2 (გ). დროთა განმავლობაში კონცენტრაციის ვარიაციები მოცემულია შემდეგ სურათზე:

ზემოთ მოყვანილი ფიგურის ანალიზიდან შეგვიძლია განვაცხადოთ, რომ A, B და C მრუდები წარმოადგენს შემდეგი რეაქციის კომპონენტების კონცენტრაციების დროებით ცვლას:
ა) ჰ2არა2 და NH3
ბ) NH3, ჰ2 და არა2
გ) NH3არა2 და ჰ2
დ) არა2, ჰ2 და NH3
ე) ჰ2, NH3 და არა2
სწორი პასუხი: დ) ნ2, ჰ2 და NH3.
პირველი ნაბიჯი: დააბალანსე ქიმიური განტოლება.
2 NH3(ზ) ნ2 (გ) + 3 ჰ2 (გ)
დაბალანსებული რეაქციით მივხვდით, რომ საჭიროა 2 მოლი ამიაკი აზოტად და წყალბადში დაშლისთვის. ასევე, რეაქციაში წარმოქმნილი წყალბადის რაოდენობა სამჯერ მეტია, ვიდრე ამიაკი.
მე -2 ნაბიჯი: დიაგრამის მონაცემების ინტერპრეტაცია.
თუ ამიაკი იშლება, მაშინ გრაფაში მისი კონცენტრაცია მაქსიმალურია და იკლებს, როგორც ეს ჩანს C მრუდეში.
პროდუქტები, როგორც ისინი იქმნება, რეაქციის დასაწყისში კონცენტრაციები ნულოვანია და იზრდება, რადგან რეაქტივი ხდება პროდუქტი.
მას შემდეგ, რაც წარმოებული წყალბადის რაოდენობა სამჯერ აღემატება აზოტს, მაშინ ამ გაზის მრუდი ყველაზე დიდია, როგორც აღნიშნულია B- ში.
სხვა პროდუქტი, რომელიც წარმოიქმნება არის აზოტი, როგორც ეს ჩანს მრუდე A- ში.
4. (Cesgranrio) სისტემა განტოლებით წარმოდგენილია წონასწორობაში იყო. წონასწორობის მდგომარეობა უცებ შეიცვალა ნივთიერების G დამატებით. სისტემა რეაგირებს ბალანსის აღსადგენად. ქვემოთ ჩამოთვლილი დიაგრამებიდან რომელი წარმოადგენს საუკეთესოდ აღწერილ პროცესში განხორციელებულ ცვლილებებს?
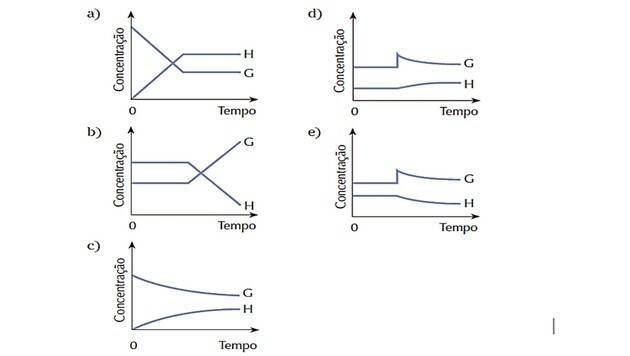
სწორი პასუხი: დ).

რადგან სისტემა თავიდანვე წონასწორობაში იმყოფებოდა, G და H ნივთიერებების რაოდენობა უცვლელი დარჩა.
დარღვევა მოხდა, რადგან G კონცენტრაცია გაიზარდა და სისტემამ რეაგირება მოახდინა ამის გარდაქმნით რეაქტივი მეტ პროდუქტში H, გადააქვს ბალანსი მარჯვნივ, ანუ ემხრობა რეაქციას პირდაპირი
ჩვენ ვაკვირდებით, რომ რეაქტივის მრუდი G მცირდება მისი მოხმარების დროს, ხოლო პროდუქტის მრუდი იზრდება მისი ფორმირებისას.
ახალი წონასწორობის დამყარებისას, სიდიდეები ისევ ხდება მუდმივი.
წონასწორობის მუდმივა: დამოკიდებულება კონცენტრაციასა და წნევას შორის
5. (UFRN) იცის რომ კპ = კჩ (RT)ნ, შეგვიძლია ვთქვათ, რომ კპ = კჩ, ამისთვის:
ფოლადი2(ზ) + თ2 (გ) ↔ CO(ზ) + თ2ო(ზ)
ბ) ჰ2 (გ) +2 (გ) თ2ო(1)
გ) არა2 (გ) + 3 სთ2 (გ) ↔ 2 NH3(ზ)
დ) არა(ზ) + ½ O2(ზ) ↔ არა2(ზ)
ე) 4 FeS(s) + 7 ო2 (გ). 2 თებ2ო3 (s) + 4 ასე რომ2(ზ)
სწორი პასუხი: ა) CO2(ზ) + თ2 (გ) ↔ CO(ზ) + თ2ო(ზ)
კპ K- ს ტოლი იყოსჩ მოლების რაოდენობის ვარიაცია უნდა იყოს ნულის ტოლი, რადგან ნულამდე აყვანილი ნებისმიერი რიცხვი 1-ით არის:
კპ = კჩ (RT)0
კპ = კჩ x 1
კპ = კჩ
მოლების რაოდენობის ცვლილება გამოითვლება:
=n = პროდუქტების მოლების რაოდენობა - რეაგენტების მოლების რაოდენობა
ამ გაანგარიშებაში, მხოლოდ აირისებურ მდგომარეობაში მყოფი ნივთიერებების კოეფიციენტები მონაწილეობენ.
თითოეულ ალტერნატიულ განტოლებაზე დაყრდნობით, ჩვენ გვაქვს:
| ფოლადი2(ზ) + თ2 (გ) ↔ CO(ზ) + თ2ო(ზ) | =n = [(1 + 1) - (1 + 1)] = 2 - 2 = 0 |
| ბ) ჰ2 (გ) +2 (გ) თ2ო(1) | =n = [0 - (1 + 1/2)] = 0 - 3/2 = - 3/2 |
| გ) არა2 (გ) + 3 სთ2 (გ) ↔ 2 NH3 (გ) | =n = [2 - (1 + 3)] = 2 - 4 = - 2 |
| დ) არა(ზ) +2 (გ) ↔ არა2 (გ) | =n = [1 - (1 + 1/2)] = 1 - 3/2 = - 1/2 |
| ე) 4 FeS(s) + 7 ო2 (გ). 2 თებ2ო3 (s) + 4 ასე რომ2 (გ) | =n = [(0 + 4) - (0 + 7)] = 4 - 7 = - 3 |
ამ შედეგებით შეგვიძლია დავაკვირდეთ, რომ ალტერნატივა, რომლის მნიშვნელობაც შეესაბამება შესაბამის შედეგს, არის პირველი განტოლების ვარიანტი.
6. (UEL ადაპტირებული) რეაქციისთვის, რომელსაც წარმოადგენს წონასწორობის მუდმივები Kჩ და კპ გამოხატულია განტოლებებით: (მოცემულია: p = ნაწილობრივი წნევა)
სწორი ალტერნატივა:
წონასწორობის მუდმივა გამოითვლება:
მყარი ნაერთები, მათი მუდმივი კონცენტრაციის გამო, არ მონაწილეობენ K– ს გამოთვლაშიჩშესაბამისად, წონასწორობის მუდმივა მოცემული განტოლებისთვის არის:
წონასწორობის მუდმივისთვის, წნევის თვალსაზრისით, მხოლოდ გაზები მონაწილეობენ გაანგარიშებაში, ასე რომ:
წონასწორობის მუდმივის გაანგარიშება
7. (Enem / 2015) რამდენიმე მჟავა გამოიყენება იმ ინდუსტრიებში, რომლებიც ანაწილებენ თავიანთ ჩამდინარე წყლებს წყლის ობიექტებში, როგორიცაა მდინარეები და ტბები, რამაც შეიძლება გავლენა მოახდინოს გარემოს ბალანსზე. მჟავიანობის გასანეიტრალებლად, ჩამდინარე წყლებს შეიძლება დაემატოს კალციუმის კარბონატის მარილი, შესაბამისი რაოდენობით, რადგან იგი წარმოქმნის ბიკარბონატს, რომელიც ანეიტრალებს წყალს. პროცესში მონაწილე განტოლებებია წარმოდგენილი:
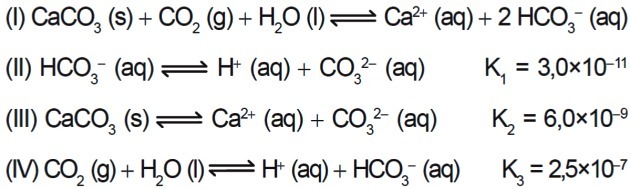
II, III და IV რეაქციების წონასწორობის მუდმივების მნიშვნელობებზე დაყრდნობით 25 ° C ტემპერატურაზე, რა არის I რეაქციის წონასწორობის მუდმივის რიცხვითი მნიშვნელობა?
ა) 4,5 x 10-26
ბ) 5,0 x 10-5
გ) 0,8 x 10-9
დ) 0.2 x 105
ე) 2.2 x 1026
სწორი პასუხი: ბ) 5,0 x 10-5
პირველი ნაბიჯი: გამოიყენე ჰესეს კანონი, საჭირო შესწორებების შესასრულებლად.
ქიმიური განტოლების გათვალისწინებით:
მუდმივი გამოითვლება:
თუ განტოლებას დავცვლით, შედეგად მივიღებთ:
და მუდმივი ხდება შებრუნებული:
კითხვაში მოცემულ 1 განტოლებაზე მისასვლელად, ჩვენ უნდა გადავაბრუნოთ II განტოლება, როგორც წინა მაგალითში.
მეორე ეტაპი: მანიპულირება II, III და IV განტოლებებით, რომ მივიღოთ I განტოლების შედეგი.
მე -3 ნაბიჯი: გამოთვალეთ I განტოლების წონასწორობის მუდმივა.
K გამოთვლამე ხდება მუდმივი მნიშვნელობების გამრავლებით.
როგორც გაანგარიშებისას გვაქვს ბაზების ტოლი ძალა, ჩვენ ვიმეორებთ ფუძეს და დავამატებთ ექსპონატებს.
მას შემდეგ, რაც ახლა ჩვენ გვაქვს ბაზების თანაბარი უფლებამოსილების განყოფილება, ვიმეორებთ ფუძეს და გამოვაკლებთ ექსპონატებს.
8. (UnB) ფოსფორის პენტაქლორიდი ძალიან მნიშვნელოვანი რეაგენტია ორგანულ ქიმიაში. იგი მზადდება გაზის ფაზაში რეაქციის საშუალებით:
3.00 ლ მოცულობის ბოთლი შეიცავს წონასწორობის პირობებში, 200 ° C ტემპერატურაზე: 0,120 მოლი PCl5(ზ)0,600 მოლი PCl3(ზ) და 0.0120 მოლი CL2(ზ). რა მნიშვნელობა აქვს წონასწორობის მუდმივას ამ ტემპერატურაზე?
სწორი პასუხი: 50 (მოლი / ლ)-1
პირველი ეტაპი: წონასწორობის მუდმივის გამოხატვის აწყობა რეაქციისთვის.
მე -2 ეტაპი: გამოთვალეთ კონცენტრაციები მოლ / ლ-ში თითოეული კომპონენტის წონასწორობაზე.
მოლური კონცენტრაციის ფორმულა:
| PCL3 | კლ2 | PCL5 |
მე -3 ნაბიჯი: შეცვალეთ კონცენტრაციები მუდმივ გამოხატვაში და გამოთვალეთ K– ის მნიშვნელობაჩ.
პროგრამები წონასწორობის წონასწორობისთვის
9. (Enem / 2016) მათი სრული ცვეთის შემდეგ, საბურავების დაწვა შესაძლებელია ენერგიის გამომუშავების მიზნით. ვულკანიზებული რეზინის სრული წვის შედეგად წარმოქმნილ გაზებს შორის ზოგიერთი დამაბინძურებელია და იწვევს მჟავე წვიმას. მათი ატმოსფეროში გაქცევის თავიდან ასაცილებლად, ეს გაზები შეიძლება გადაიზარდოს წყალხსნარში, რომელიც შეიცავს შესაბამის ნივთიერებას. გაითვალისწინეთ ცხრილში ჩამოთვლილი ნივთიერებების შესახებ ინფორმაცია.
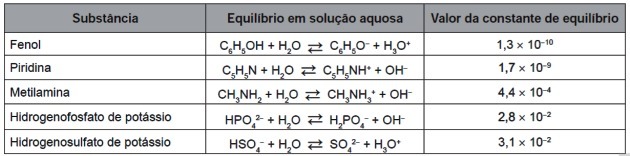
ცხრილში ჩამოთვლილი ნივთიერებებიდან ის, რომელსაც შეუძლია დაბინძურებული გაზების ეფექტურად მოხსნა, არის (ა)
ა) ფენოლი.
ბ) პირიდინი.
გ) მეთილამინი.
დ) კალიუმის წყალბადის ფოსფატი.
ე) კალიუმის წყალბადის სულფატი.
სწორი პასუხი: დ) კალიუმის წყალბადის ფოსფატი.
CO2, გოგირდის ოქსიდები (SO2 ამიტომაც3) და აზოტის ოქსიდები (NO და NO)2) ძირითადი დამაბინძურებელი გაზებია.
როდესაც ისინი რეაგირებენ ატმოსფეროში არსებულ წყალთან, არსებობს მჟავას წარმოქმნა რომლებიც წვიმის მჟავიანობის მატებას იწვევს, რის გამოც მას მჟავე წვიმას უწოდებენ.
ცხრილში მოცემული წონასწორობის მუდმივები გამოითვლება პროდუქციისა და რეაგენტების კონცენტრაციას შორის თანაფარდობით შემდეგნაირად:
გაითვალისწინეთ, რომ წონასწორობის მუდმივა პროპორციულია პროდუქციის კონცენტრაციისა: რაც უფრო მეტია პროდუქციის რაოდენობა, მით მეტია Kჩ.
K– ის ცხრილში გაითვალისწინეთ პირველი და ბოლო კომპოზიტის მნიშვნელობებიჩ:
| პირიდინი | ||
| კალიუმის წყალბადის სულფატი |
ორი რიცხვის შედარებისას ვხედავთ, რომ რაც ნაკლებია უარყოფითი ძალა, მით უფრო დიდია მუდმივის მნიშვნელობა.
დამაბინძურებლების უფრო ეფექტურად მოსაცილებლად, OH- რეაგირება მოახდინონ H იონებთან+ მჟავებში იმყოფება ა ნეიტრალიზაციის რეაქცია.
წარმოდგენილი ნივთიერებებიდან ის, რომლებიც წარმოქმნიან მჟავე ნაერთების გასანეიტრალებლად საჭირო ჰიდროქსილებს, არის: პირიდინი, მეთილამინი და კალიუმის წყალბადის ფოსფატი.
იმის გასარკვევად, რომელი ნაერთია ყველაზე ეფექტური, ჩვენ ვაკვირდებით წონასწორობის მუდმივებს: რაც უფრო მაღალია მუდმივი მნიშვნელობა, მით მეტია კონცენტრაცია OH-.
ამრიგად, ამ მიზნით შესაფერისი ნივთიერების შემცველი წყალხსნარია კალიუმის წყალბადის ფოსფატი, რადგან ის უფრო ბაზირებულია და უფრო ეფექტურად ანეიტრალებს მჟავებს.
მეტი რომ გაიგოთ, წაიკითხეთ ეს ტექსტები.:
- იონური ბალანსი
- ნეიტრალიზაციის რეაქცია
10. (Enem / 2009) საპნები არის გრძელი ჯაჭვის კარბოქსილის მჟავების მარილები, რომლებიც გამოიყენება სარეცხი პროცესების დროს წყალში დაბალი ხსნადობის ნივთიერებების მოცილება, მაგ. ზეთები და ცხიმები შემდეგი ფიგურა წარმოადგენს საპნის მოლეკულის სტრუქტურას.
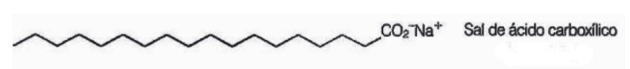
ხსნარში საპნის ანიონებს შეუძლიათ წყლის ჰიდროლიზება და ამით შექმნან შესაბამისი კარბოქსილის მჟავა. მაგალითად, ნატრიუმის სტეარატისთვის დადგენილია შემდეგი ბალანსი:
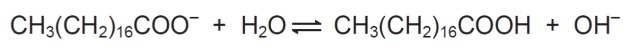
ვინაიდან წარმოქმნილი კარბოქსილის მჟავა ცუდად იხსნება წყალში და ნაკლებად ეფექტურია ცხიმების მოსაშორებლად, საშუალების pH უნდა კონტროლდებოდეს ისე, რომ თავიდან იქნას აცილებული ზემოთ ბალანსის მარჯვნივ გადაწევა.
ტექსტში მოცემული ინფორმაციის საფუძველზე სწორია დავასკვნათ, რომ საპნები მუშაობს ისე:
ა) უფრო ეფექტური საბაზისო pH– ზე.
ბ) უფრო ეფექტურია მჟავე pH– ზე.
გ) უფრო ეფექტურია ნეიტრალური pH– ზე.
დ) ეფექტურია pH ნებისმიერ დიაპაზონში.
ე) უფრო ეფექტურია მჟავე ან ნეიტრალური pH– ზე.
პასუხი: ა) უფრო ეფექტურია pH– ზე.
ნაჩვენებ ბალანსში ვხედავთ, რომ ნატრიუმის სტეარატი წყალთან რეაგირებისას ქმნის კარბოქსილის მჟავას და ჰიდროქსილს.
PH კონტროლის მიზანი არ არის კარბოქსილის მჟავას წარმოქმნის დაშვება და ეს ხდება ბალანსის გადაადგილებით OH კონცენტრაციის შეცვლით-.
მით უფრო OH- ხსნარში, პროდუქციის მხრიდან ადგილი აქვს დარღვევას და ქიმიური სისტემა რეაგირებს ნივთიერების მოხმარებით, რომლის კონცენტრაციაც გაიზარდა, ამ შემთხვევაში ჰიდროქსილი.
შესაბამისად, მოხდება პროდუქტების რეაგენტებად გარდაქმნა.
ამიტომ, საპნები ყველაზე ეფექტურად მუშაობენ ძირითად pH– ზე, რადგან ზედმეტი ჰიდროქსილი გადააქვს წონასწორობას მარცხნივ.
თუ pH მჟავე იქნებოდა, H კონცენტრაცია უფრო მაღალი იქნებოდა+ ეს გავლენას მოახდენს ბალანსს OH– ის მოხმარებით- და ბალანსი იმოქმედებს მეტი ჰიდროქსილის წარმოქმნით, ბალანსის მარცხნივ გადაადგილებით და უფრო მეტი კარბოქსილის მჟავის წარმოებით, რაც არ წარმოადგენს საინტერესო პროცესს.
ქიმიური წონასწორობის ცვლა
11. (Enem / 2011) გამაგრილებელი სასმელები სულ უფრო ხშირად ხდებიან საზოგადოებრივი ჯანდაცვის პოლიტიკის სამიზნეები. წებოვანი პროდუქტები შეიცავს ფოსფორმჟავას, ნივთიერებას, რომელიც საზიანოა კალციუმის, მინერალური ნივთიერებების დასაფიქსირებლად, რომელიც კბილების მატრიქსის მთავარი კომპონენტია. კარიესი არის დისბალანსის დინამიური პროცესი სტომატოლოგიური დემინერალიზაციის პროცესში, მჟავიანობის გამო მინერალების დაკარგვა. ცნობილია, რომ კბილის ემალის ძირითადი კომპონენტია მარილი, რომელსაც ჰიდროქსიაპატიტი ეწოდება. სოდა, საქაროზას არსებობით, ამცირებს ბიოფილმის pH (ბაქტერიული დაფა), რაც იწვევს სტომატოლოგიური მინანქრის დემინერალიზაციას. ნერწყვის დაცვის მექანიზმებს 20–30 წუთს სჭირდება pH დონის ნორმალიზება, ხდება კბილის რემინერალიზაცია. შემდეგი ქიმიური განტოლება წარმოადგენს ამ პროცესს:
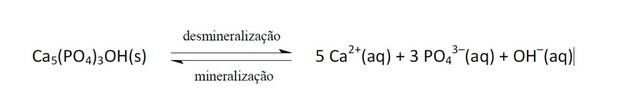 გროისმანი, ს. სოდის გავლენა კბილებზე ფასდება დიეტის მოხსნის გარეშე. Ხელმისაწვდომია: http://www.isaude.net. ნანახია: 2010 წლის 1 მაისი (ადაპტირებულია).
გროისმანი, ს. სოდის გავლენა კბილებზე ფასდება დიეტის მოხსნის გარეშე. Ხელმისაწვდომია: http://www.isaude.net. ნანახია: 2010 წლის 1 მაისი (ადაპტირებულია).
იმის გათვალისწინებით, რომ ადამიანი ყოველდღიურად იყენებს გამაგრილებელ სასმელებს, შეიძლება წარმოიშვას სტომატოლოგიური დემინერალიზაციის პროცესი,
ა) ოჰ–, რომელიც რეაგირებს Ca იონებთან2+, ბალანსის გადატანა მარჯვნივ.
ბ) ჰ+, რომელიც რეაგირებს OH ჰიდროქსილებთან–, ბალანსის გადატანა მარჯვნივ.
გ) ოჰ–, რომელიც რეაგირებს Ca იონებთან2+, ბალანსის გადაადგილება მარცხნივ.
დ) ჰ+, რომელიც რეაგირებს OH ჰიდროქსილებთან–, ბალანსის გადაადგილება მარცხნივ.
ე) Ca2+, რომელიც რეაგირებს OH ჰიდროქსილებთან–, ბალანსის გადაადგილება მარცხნივ.
სწორი პასუხი: ბ) ჰ+, რომელიც რეაგირებს OH ჰიდროქსილებთან–, ბალანსის გადატანა მარჯვნივ.
როდესაც pH მცირდება, ეს იმიტომ ხდება, რომ მჟავიანობა გაიზარდა, ანუ H იონების კონცენტრაცია+როგორც განცხადებაში ნათქვამია, არსებობს ფოსფორის მჟავის არსებობა.
ეს იონები რეაგირებენ OH– სთან- ამ ნივთიერების მოხმარების მიზეზი და, შესაბამისად, წონასწორობის მარჯვნივ გადაწევა, რადგან სისტემა მოქმედებს ამ მოცილებული იონების მეტი წარმოებით.
წონასწორობის ცვლა რეაქტორებსა და პროდუქტებს შორის მოხდა OH კონცენტრაციის შემცირების გამო-.
თუ Ca იონები2+ და ოჰ- კონცენტრაციის გაზრდის შემთხვევაში, ის წონასწორობას მარცხნივ გადააქცევდა, რადგან სისტემა რეაგირებდა მათი მოხმარებით და მეტი ჰიდროქსიაპატიტის წარმოქმნით.
წინა ბალანსის შეცვლა, რომელიც ეხება გამაგრილებლის გაჟონვას აღწერილ პირობებში, იწვევს:
ა) CO გამოყოფა2 გარემოსთვის.
ბ) ჭურჭლის ტემპერატურის ამაღლება.
გ) კონტეინერის შიდა წნევის მომატება.
დ) CO კონცენტრაციის მომატება2 სითხეში.
ე) მნიშვნელოვანი H– ს წარმოქმნა2ო.
სწორი პასუხი: ა) CO გამოყოფა2 გარემოსთვის.
ბოთლის შიგნით ნახშირორჟანგი იხსნება თხევადში მაღალი წნევის გამო.
ბოთლის გახსნისას, ჭურჭლის შიგნით წნევა (რაც მეტი იყო) ტოლია წნევას გარემოში და ამასთან, ნახშირორჟანგის გაქცევა ხდება.
წონასწორობის ცვლა რეაქტორებსა და პროდუქტებს შორის მოხდა წნევის შემცირების გამო: როდესაც წნევა იკლებს, წონასწორობა გადადის უდიდეს მოცულობამდე (მოლების რაოდენობა).
რეაქციამ გადაინაცვლა მარცხნივ და CO2 რომელიც გახსნილი იყო სითხეში, გაათავისუფლეს, როდესაც ბოთლი გაიხსნა.