Едно смесване на разтвори на същото разтворено вещество без химическа реакция тя се състои в обединяване в един и същ контейнер на два разтвора, например с калиев хлорид (Kcl). В този вид смес никога няма да има химическа реакция поради наличието на равни разтворени вещества, тоест и двете имат един и същ катион и един и същ анион. По този начин можем да кажем, че когато изпълняваме смес с тези характеристики, просто добавяме количествата разтворено вещество и разтворител, които съставляват и двата разтвора.
Ако смесим например разтвор от 1L вода и 4 грама KI (калиев йодид) с друг разтвор от 2L вода и 6 грама KI, ще получим нов разтвор от 3L вода и 10 грама KI .
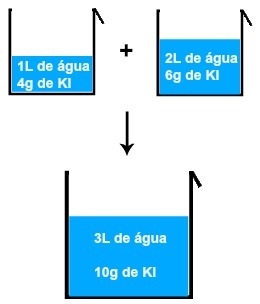
Резултат от смесването на два разтвора на калиев йодид
Анализирайки изображението, можем да заключим, че масата на разтвореното вещество (m1') от първия разтвор се добавя към масата на разтвореното вещество (m1'') на второто решение, в резултат на масата на разтвореното вещество (mF) в крайното решение (Разбъркайте):
м1'+ m1"= mF
В примера:
4 + 6 = 10 грама
Същото се случва и с обема вода, присъстващ във всеки разтвор, т.е. обемът на първия (V '), добавен към обема на втория (V' '), води до крайния обем (V'F):
V '+ V' = VF
В примера:
1 + 2 = 3 L
Тъй като всеки разтвор има количество разтворено разтворено вещество и тук имаме смес от разтвори на същото разтворено вещество, тогава можем, от горното, да определим концентрацията (обща, моларност) на всеки от смесените разтвори, а също и на крайния разтвор.
Следователно трябва да запомним формулите за изчисляване на тези концентрации:
Обща концентрация:
С = м1
V
м1 = маса на разтвореното вещество
V = обем на разтвора
ЗАБЕЛЕЖКА: изолиране на m1 във формулата имаме: м1 = CV
Моларност:
М = м1
М1.V
М1 = моларна маса на разтвореното вещество.
ЗАБЕЛЕЖКА: изолиране на m1 във формулата имаме: м1 = М.М1.V
Тъй като сместа от разтвори на същото разтворено вещество адресира сумата от масата на разтвореното вещество на разтворите, можем да заместим всяко от наблюденията в следния израз:
м1'+ m1'' = mF
C'.V '+ C ". V" = CF.VF
Не спирайте сега... Има още след рекламата;)
C '= обща концентрация на разтвор 1
C "= обща концентрация на разтвор 2
Ако изчисляването на сместа от разтвори включва моларност:
м1'+ m1"= mF
M'.V '+ M' '. V' = MF.VF
ЗАБЕЛЕЖКА: Тъй като разтвореното вещество е същото, моларната маса е еднаква във всеки от разтворите; следователно, той се пренебрегва при изчислението.
сега вижте примери, които обхващат изчисления в смес от разтвори на същото разтворено вещество без химическа реакция:
Пример 1: (Mackenzie-SP-Adaptada) Добавяне на 600 ml от разтвор на 14 g / L KOH към определен обем (v) от 84 g / L разтвор на същата основа, се получава разтвор от 67,2 g / L. Добавеният обем (v) към разтвора от 84 g / L е:
а) 0100 мл
б) 3000 мл
в) 2700 мл
г) 1500 мл
д) 1900 мл
Данните, предоставени от упражнението, са:
V '= 600 ml
C '= 14 g / L
V "=?
C "= 84 g / L
VF = ?
CF = 67,2 g / L
Преди да определим добавения обем на разтвор 1, първоначално трябва да определим крайния обем, използвайки следния израз:
V '+ V' = VF
600 + V "= VF
Замествайки стойностите, дадени в математическия израз по-долу, имаме:
C'.V '+ C ". V" = CF.VF
14. 600 + 84.V "= 67.2. (600 + V")
8400 + 84.V "= 67.2. 600 + 67.2.V "
8400 + 84.V "= 40320 + 67.2.V"
84.V "- 67.2.V" = 40320 - 8400
16.8.V "= 31920
V "= 31920
16,8
V "= 1900 ml
Пример 2: (UFOP) В 1000mL мерителна колба, 250mL от 2M разтвор на сярна киселина се добавят с 300mL от 1M разтвор на същата киселина и обемът се долива до 1000mL с дестилирана вода. Определете моларността на получения разтвор.
Данните, предоставени от упражнението, са:
V '= 250 ml
М '= 2 М
V "= 300 ml
М "= 1 М
VF = 1000мл
МF = ?
За да определите моларността на крайното решение, просто използвайте математическия израз, който представлява процеса:
M'.V '+ M' '. V' = MF.VF
2. 250 + 1. 300 = МF.1000
500 + 300 = М.F. 1000
800 = МF
1000
МF = 0,8 mol / L
От мен Диого Лопес Диас
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
ДНИ, Диого Лопес. "Смес от разтвори на същото разтворено вещество без химическа реакция"; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/mistura-solucoes-mesmo-soluto-sem-reacao-quimica.htm. Достъп на 27 юни 2021 г.