РН съответства на хидрогенния потенциал на разтвора. Определя се от концентрацията на водородни йони (Н+) и служи за измерване на степента на киселинност, неутралност или алкалност на даден разтвор.
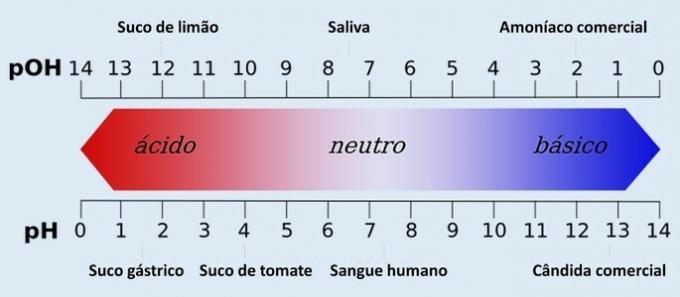
В допълнение към рН има и друго количество, което определя киселинността и основността на водната система: pOH (хидроксилионен потенциал). Тази скала има същата функция като pH, въпреки че е по-малко използвана.
скала на pH
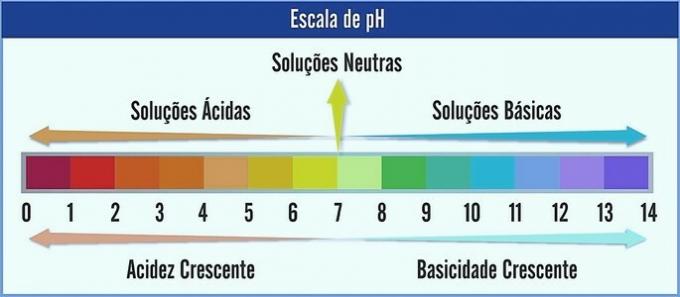
РН е представено в скала, варираща от 0 до 14. Той измерва киселинността и основността на разтвора.
Следователно, pH 7 представлява неутрален разтвор (например чиста вода). Тези преди него се считат за киселинни разтвори (киселинно рН), а тези след 7 са основните разтвори (алкално рН).
С това наблюдение киселинният характер се увеличава отдясно наляво. Основният знак, отляво надясно. Имайте предвид, че колкото по-ниска е стойността на рН, толкова по-кисел ще бъде разтворът.
Научете повече на:
- Буферен разтвор
- Титруване
- Реакция на неутрализация
Примери
Киселинни разтвори
| Решение | рН |
|---|---|
| Стомашен сок | 2,0 |
| Лимонов сок | 2,2 |
| Оцет | 3,0 |
| Кафе | 5,0 |
| Краве мляко | 6,4 |
Основни решения
| Решение | рН |
|---|---|
| човешка кръв | 7,35 |
| Морска вода | 7,4 |
| Сода бикарбонат | 8,4 |
| Мляко от магнезия | 10,5 |
| Избелва | 12,5 |
Как да изчислим рН?
През 1909 г. датският химик Сорен Серенсен (1868-1939) предлага киселинността на разтворите, измерена по отношение на концентрациите на йони Н+, трансформира стойностите си с помощта на логаритми за улесняване на разбирането.
При температура 25 ° C йонният продукт на водата е равен на 10–14 мол2/ L2.
Прилагайки кологаритъма в израза, трябва да:
Чрез този израз можем да получим съответната стойност от една скала до друга чрез изваждане.
Как да се измери pH?
Контролът на pH е важен не само за научни цели, но и в ежедневието.
Трябва да се провери рН на басейна, както и рН на аквариума и дори рН на почвата, за да се даде възможност за някои видове култури.
По-долу са основните начини за измерване на pH.
киселинно-алкален индикатор
Така наречените киселинно-алкални индикатори се използват за измерване на рН на разтвора. Те са вещества, които променят цвета, указвайки характера на разтвора. Най-използваните показатели са: лакмус и фенолфталеин.

Крачкомер
В допълнение към индикаторите, рН на разтвора може да се измери с помощта на инструмент, наречен пиометър. Това електронно устройство измерва електрическата проводимост на разтвора и го преобразува в скалата на стойностите на pH.

Упражнения за приемни изпити с обратна връзка
1. (Enem / 2014) Изследовател осъзнава, че етикетът на една от чашите, в която държи концентрат от храносмилателни ензими, е нечетлив. Той не знае кой ензим съдържа чашата, но подозира, че това е стомашна протеаза, която действа в стомаха, като смила протеини.
Знаейки, че храносмилането в стомаха е кисело, а червата е основна, той сглобява пет епруветки с храна различно, добавете ензимния концентрат към разтвори с определено рН и изчакайте да видите дали ензимът действа в някоя техен.
Епруветката, в която ензимът трябва да действа, за да покаже, че хипотезата на изследователя е правилна, е тази, която съдържа:
а) картофено кубче в разтвор с рН = 9
б) парче месо в разтвор с рН = 5
в) варен яйчен белтък в разтвор с рН = 9
г) порция юфка в разтвор с рН = 5
д) маслена топка в разтвор с рН = 9
Правилна алтернатива: б) парче месо в разтвор с рН = 5.
Протеазата е ензим, който смила протеините и тъй като е стомашен, той действа в стомаха, чието рН е кисело.
Анализирайки алтернативите, трябва да:
а) ГРЕШНО. Картофите са с високо съдържание на въглехидрати и рН на концентрата е основно.
б) ПРАВИЛНО. Месото съдържа протеини и ензимите могат да действат върху него, а рН на концентрата е киселинно, подобно на стомаха.
в) ГРЕШНО. РН на концентрата е основно.
г) ГРЕШНО. Пастата е богата на въглехидрати.
д) ГРЕШНО. РН на концентрата е основно.
2. (Udesc / 2009) "Киселинен дъжд" е термин, отнасящ се до валежи от атмосферата на дъжд с по-големи от нормалните количества азотна и сярна киселини.
Предшествениците на киселинните дъждове идват както от естествени източници, като вулкани и разлагаща се растителност, така и от процеси промишлени емисии, основно серен диоксид и азотни оксиди от изгаряне на горива фосили.
РН на дъждовната вода, която се счита за нормална, е 5,5 (поради наличието на въглеродна киселина от солюбилизацията на въглеродния диоксид). Химик, наблюдаващ силно индустриализиран регион, отбелязва, че рН на дъждовната вода е 4,5.
Като се има предвид, че киселинността е свързана с концентрацията на Н3О+, правилно е да се каже, че вода с рН 4,5 е:
а) два пъти по-основно от нормалното.
б) два пъти по-киселинно от нормалното.
в) десет пъти по-основно от нормалното.
г) десет пъти по-кисели от нормалното.
д) сто пъти по-киселинно от нормалното.
Правилна алтернатива: г) десет пъти по-кисела от нормалната.
Според изразите pH = - log [H+] и [H+] = 10-pH, Ние трябва да:
рН = 5,5
[H+] = 10-5,5
рН = 4,5
[H+] = 10-4,5
Разликата между стойностите е: 10- 5,5 - ( - 4,5) = 10 -1
Тъй като скалата на рН е логаритмична скала, промяната на една единица се равнява на 10 пъти по-кисел разтвор.
3. (UFMG / 2009) Помислете за определено количество вода и лимонов сок, смесени, съдържащи се в чаша. Прегледайте тези три твърдения относно тази система:
I. Системата е кисела.
II. РН на системата е по-голямо от 7.
III. В системата концентрацията на йони Н+ е по-голям от OH–.
Въз основа на този анализ е ПРАВИЛНО да се твърди, че:
а) само твърдения I и II са верни.
б) верни са само твърдения I и III.
в) верни са само твърдения II и III.
г) и трите твърдения са верни.
Правилна алтернатива: б) верни са само твърдения I и III.
I. ПРАВИЛНО Лимонът съдържа лимонена киселина, която в разтвор отделя H йони+ и така системата е кисела.
II. ГРЕШНО. РН е по-малко от 7, характеризиращо киселинна система: колкото по-близо до 0 е рН на разтвора, толкова по-кисело е.
III. ПРАВИЛНО Киселинното рН е резултат от високата концентрация на Н йони+ в разтвор, тъй като pH = - log [H+].
За повече въпроси, с коментирана резолюция, не забравяйте да проверите:Упражнения за pH и pOH.