Хидрогенирането се извършва с ненаситени ациклични въглеводороди, т.е. които имат отворени вериги с двойни или тройни връзки, като алкени, алкини и диени. Може да се появи и в ароматни въглеводороди, тъй като те имат двойни връзки в пръстена и с циклани (циклоалкани) до пет въглерода.
Тези съединения реагират като водороден газ в присъствието на някакъв катализатор, като никел, платина и паладий, при нагряване. По този начин възниква реакция на присъединяване, при която връзката pi (π) се прекъсва, образувайки две нови единични връзки и водородът се въвежда в молекулата.
Като цяло имаме:
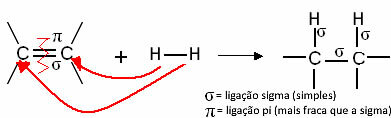
Обща реакция на хидрогениране
Сега нека разгледаме някои примери:
- Хидрогениране до алкени: Полученият продукт е алкан.
По-долу имаме реакция на хидрогениране на етилен (или етилен) за получаване на етан:
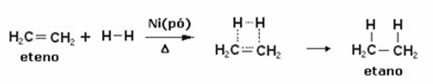
Пример за реакция на хидрогениране на етилен
Този тип каталитично хидрогениране се използва от хранителната промишленост за получаване на полутвърди мазнини като маргарини. Растителните масла и мазнини се различават само по това, че маслата имат дълги молекули с двойни връзки между въглеродните атоми, докато мазнините имат само единични връзки между своите въглерод.
По този начин, за да превърнете маслото в мазнина, е достатъчно да хидрогенирате маслото. По този начин вашите двойни връзки ще бъдат прекъснати и конвертирани в единични облигации. Резултатът е производството на обаждания хидрогенирани растителни мазнини.
- Хидрогениране на алкин: Тъй като алкините имат две pi връзки, пълното им хидрогениране протича на два етапа, в първия се образува алкен, а във втория - алкан.
В реакцията по-долу имаме хидрогениране на пропин с окончателно образуване на пропан:
1-ва стъпка: З.3C C ≡ СН + З.2 → H3C CЗ.═ ° СЗ.2
2-ри етап: З.3C CЗ.═ ° СЗ.2 + 2 часа2 → H3C CЗ.2─ ° СЗ.3
Ако искаме тази реакция да спре в първата стъпка, трябва да използваме някакво вещество, което спира действието на катализатора.
- Хидрогениране на диени: Има три вида диени: натрупана (двойни връзки се появяват по-долу), изолиран (двойните връзки са разделени поне с две единични връзки) и конюгати (двойни връзки се появяват последователно).
Хидрогенирането на натрупаните и изолирани диени се случва по същия начин, както видяхме за алкените, но при двойно, тъй като диените имат по-голяма ненаситеност. Вижте два примера:
* Пример за хидрогениране в натрупан диен:
Н Н Н
│ │ │
З.3С СН ═ ° С ═ CH ─ CH3 + 2 часа2 → H3С СН ─ ° С ─ CH ─ CH3
│ │ │
Н Н Н
* Пример за хидрогениране в изолиран диен:
Н Н Н Н
│ │ │ │
З.3С СН ═ CH─CH2 ─ CH ═ CH ─ CH3 +2 Н2 → H3С СН ─ CH─CH2 ─ CH ─ CH ─ CH3
От друга страна, хидрогенирането на конюгирани диени може да се случи по два начина: с добавяне на 1.2 и добавяне на 1.4. Най-често срещаната е добавката 1,2, при която водородите се добавят към въглеродите, които образуват двойната връзка и при ниски температури. Добавката 1,4, от друга страна, се случва при повишени температури и е когато има резонанс и поява на свободни валенции във въглерод 1 и 4. Вижте примери за всеки случай:
* Пример за добавяне на 1.2 в конюгирани диени:
З.2С СН ─ CH ═ CH2 + З.2 → H2C CH ─ C ─ CH CH2
│ │
Н Н
* Пример за добавяне 1.4 в конюгирани диени:
З.2С СН ─ CH ═ CH2 + З.2 → H2С СН ═ CH CH2
│ │
Н Н
- Хидрогениране на ароматни съединения: Пи връзките на бензеновия пръстен се разкъсват и водородните атоми се добавят към въглеродите, които правят тези връзки.
Този вид пълно хидрогениране е показан по-долу:

Обща реакция на хидрогениране на бензен
- Циклан хидрогениране: Възниква образуване на алкан.
Пример: Хидрогениране на циклопропан:
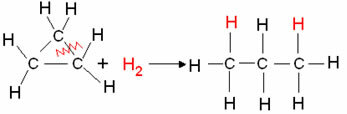
Реакция на хидрогениране на циклопропан
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/reacao-organica-hidrogenacao.htm


