
Количеството калории зависи от конституцията на храната. По този начин, за да определим експериментално количеството топлина, отделяно от храната и което може да бъде усвоено от тялото, използваме устройство, наречено калориметър.
Това устройство измерва топлината, отделяна от храната, когато е изгорена. Има няколко вида калориметри; първият от тях е създаден през 1780 г. от Лавоазие и Лаплас и е бил леден калориметър.
В днешно време най-използваната и която взема предвид обяснената по-горе концепция за калориите е воден калориметър. Това устройство е покрито с изолационен материал, за да се предотврати загубата на топлина от средата; и храната за анализ се поставя в горивна камера, който съдържа кислороден газ и електроди. Тези електроди се подлагат на електрически разряд и причиняват тяхното запалване и изгаряне на храната.
Известната маса вода, съдържаща се в калориметъра, поглъща топлината, отделяна от изгорената храна и a термометър измерва повишаването на температурата на водата. Освен това калориметърът съдържа a
бъркалка което позволява температурата на водата да остане равномерна през цялата си цялост.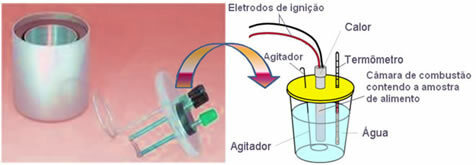
Така че, ако използваме например маса от 1 грам захар и калориметърът има 1000 g вода и наблюдаваме, че в крайна сметка от реакцията, температурата на водата се е повишила от 20 ° C до 24 ° C, тоест тя се е увеличила с 4 ° C, след което можем да достигнем енергийната стойност на захар. Като? Е, като се има предвид първоначалната концепция за калории, имаме:
| Вдигнете от 1 ° C → 1 кал на грам вода |
| Вдигнете от 4 ° C → 4 кал на грам вода |
Така 1 г вода абсорбира 4 вар. Използвани са обаче 1000 g вода и като се има предвид, че цялата топлина, отделена при горенето, е погълната от нея, общата енергия, погълната от водата, е 4000 cal или 4 kcal. Следователно заключаваме, че:
| Енергийната стойност на захарта = 4000 кал / г или 4 ккал / г. |
Преобразуване в SI:
1 kcal 4,18 kJ
4 kcal / g x
x = 16,72 kJ / g
Освен това можем да използваме следното уравнение, за да изчислим количеството топлина, отдадено или погълнато от водата:
| Q = m. ° С. T |
Където:
Q = топлина, отдадена или абсорбирана от вода;
m = маса вода;
c = специфична топлина на водата, която е равна на 1,0 cal / g. ° C или 4.18 J / g. ° С;
Δt = изменение на температурата, претърпяно от водата, което се дава от намаляването на крайната температура с първоначалната (tе - Ti).
Използвайки тази формула, получаваме същия резултат:
Q = m. ° С. T
Q = 1000 g. 1,0 кал / g. ° С. (24-20) ° С
Q = 4000 кал
Q = 4,0 kcal
или
Q = m. ° С. T
Q = 1000 g. 4,18 kJ / g. ° С. (24-20) ° С
Q = 16,72 kJ
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm
