НА ъглова геометрия е един от няколко вида молекулярна геометрия, които все още могат да бъдат линейни, пирамидални, плоски тригонални, тетраедричени т.н. Ъгловата геометрия може да бъде намерена само в молекули, които имат следните характеристики:
Триатомиката, тоест те имат само три атома;
Имате поне три електронни облака в централния атом.
Забележка: електронният облак е всичко ковалентна връзка (единични, двойни, тройни или координатни) между атоми и електронни двойки на валентен слой които не участват в разговор.
Вижте някои примери за молекули, които имат ъглова геометрия:
1-ви пример: вода (H2О)

конвенционална водна структура
В структурата на водата имаме:
Три атома: два водорода и един кислород;
Кислородът е централният атом, тъй като той образува по-голям брой връзки (две, тъй като принадлежи към семейството VIA);
Две единични връзки между кислород и водород. Това е така, защото всеки водород може да направи само една връзка, а кислородът - две връзки;
Четири несвързани електрона в кислорода, тъй като той има шест електрона във валентната обвивка и използва само два в връзките.
Следователно, както във водната молекула има три атома и четири електронни облака (две единични връзки и две несвързващи се електронни двойки) в централния атом, геометрията е ъглова.
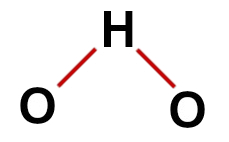
Правилна структурна формула на водата
Забележка: Винаги, когато молекулата представя тези модели, ъгълът, образуван между атомите, е приблизително 109º 28'.
2-ри пример: Серен диоксид (SO2)

Конвенционална структура на серен диоксид
В структурата на серен диоксид имаме:
Три атома: два кислорода и един серен атом;
Сярата е централният атом, тъй като е най-малкият елемент в молекулата, тъй като всички елементи трябва да образуват еднакъв брой връзки (две);
Двойна връзка между сярата и един от кислородите. Това е така, защото и двете се нуждаят от две връзки;
Едно координатна или дативна ковалентна връзка, тъй като сярата е била стабилна след сдвояване с другия кислород, но все още има кислороден атом, който се нуждае от два електрона;
Четири несвързващи електрона в кислород. Това е така, защото кислородът има шест електрона във валентната обвивка и използва само два във връзките.
По този начин, както в молекулата на серен диоксид има три атома и четири електронни облака (две единични връзки и две двойки несвързващи се електрони) в централния атом, геометрията е ъглова.
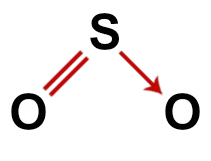
Правилна структурна формула на серен диоксид
Забележка: Винаги, когато молекулата има тези модели, ъгълът, образуван между атомите, е приблизително 120О.
От мен Диого Лопес Диас
Източник: Бразилско училище - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm

