Изобарна трансформация се получава, когато газът е под постоянно налягане. Например, ако се извърши в открита среда, трансформацията ще бъде изобарна, тъй като налягането ще бъде атмосферно налягане, което няма да се промени.
В този случай температурата и обемът варират. Двама водещи учени са изследвали как възниква тази вариация в изобарни трансформации. Първият, който свързва обема и температурата на газовете, е Жак Шарл (1746-1823), през 1787 г., а след това, през 1802 г., Джоузеф Гей-Люсак (1778-1850) определя количествено тази връзка.
По този начин се появи закон, който обяснява изобарните трансформации на газове, които станаха известни като Закона на Чарлз / Гей-Люсак. Посочва се, както следва:
„В система с постоянно налягане обемът на фиксирана маса на газ е право пропорционален на температурата.“

Това означава, че ако удвоим температурата, обемът, зает от газа, също ще се удвои. От друга страна, ако намалим температурата, обемът на газа също ще намалее в същата пропорция.
Това може да се види в много прост експеримент. Ако поставим балон в гърлото на бутилка, фиксирана маса въздух ще бъде уловена. Ако потопим тази бутилка в купа с ледена вода, балонът ще се спусне. Сега, ако го поставим в купа с гореща вода, балонът ще се напълни.
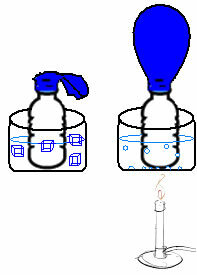
Това е така, защото с увеличаване на температурата кинетичната енергия на газовите молекули се увеличава и скоростта, с която те се движат, също се увеличава. По този начин газът се разширява, увеличавайки обема, който заема, и балонът се надува. Обратното се получава, когато понижим температурата, като я поставим в студена вода.
Не спирайте сега... Има още след рекламата;)
Тази връзка между температурата и обема при изобарни трансформации се дава от следната връзка:
V = k
T
"k" е константа, както може да се види на следната графика:
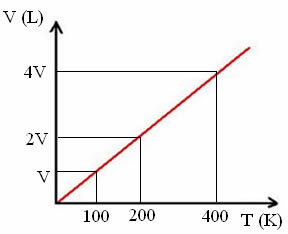
Имайте предвид, че съотношението V / T винаги дава константа:
_V_ =_2V_ = _4V_
100 200 400
По този начин можем да установим следната връзка за изобарни трансформации:
Vпървоначална = VФинал
Tпървоначална TФинал
Това означава, че когато има някаква промяна в температурата на газа при постоянно налягане, можем да открием обема му чрез този математически израз. Вярно е и обратното, знаейки обема на газа, ние откриваме при каква температура е той. Вижте пример:
„Газовата маса заема обем от 800 cm3 при -23 ° C, при дадено налягане. Каква е температурата, регистрирана, когато газообразната маса при същото налягане заема обем от 1,6 L? "
Резолюция:
Данни:
Vпървоначална = 800 см3
Tпървоначална = -23 ºC, като към 273 имаме 250 K (Келвин)
VФинал = 1,6 L
TФинал = ?
* Първо трябва да оставим силата на звука на същата единица. Известно е, че 1 dm3 се равнява на 1 литър. като 1 dm3 е същото като 1000 cm3, изглежда, че 1 литър = 1 000 cm3:
1 L 1000 cm3
х 800 см3
x = 0,8 L
* Сега заместваме стойностите на формулата и намираме крайната стойност на температурата:
Vпървоначална = VФинал
Tпървоначална TФинал
0,8_ = 1,6
250 ТФинал
0.8 TФинал = 250. 1,6
TФинал = 400
0,8
TФинал = 500K
* Преминавайки към скалата на Целзий, имаме:
T (K) = T (° C) + 273
500 = T (° C) + 273
T (° C) = 500 - 273
Т (° С) = 227 ° С
От Дженифър Фогаса
Завършва химия
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
FOGAÇA, Дженифър Роча Варгас. „Изобарна трансформация“; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/transformacao-isobarica.htm. Достъп на 27 юни 2021 г.
Какво представляват газовете, какви са свойствата на газовете, молекулярни съединения, сгъстимост, фиксиран обем, кинетична енергия средна, абсолютна температура на газ, идеален газ, реални газове, перфектен газ, променливи на състоянието на газа, обем на газ, сезони
Химия

Закони на Гей-Люсак, Прустов закон, Химическа реакция, Постоянна пропорция, Маси вещества, Чисто вещество, Анализ качествени и количествени, закон на съвършените газове, закон на постоянните пропорции, закон на определени пропорции, закон обемни.