Едно от най-големите предизвикателства за всеки, който учи химия, се нарича електронно разпространение. Това, което ще представим в този контекст, може значително да улесни вашите изследвания, свързани с електронната конфигурация, предложена от учения Линус Полинг.
Максималният брой електрони, който се побира във всеки слой или енергийно ниво, е даден чрез таблицата:
Енергиен слой Максимален брой електрони
1-во К 2
2-ри L 8
3-ти М 18
4-ти N 32
5 ° O 32
6-то Р 18
7-мо Q 8
Нарастващият ред на енергията на поднивата е редът в последователността на диагоналите. Диаграмата на Linus Pauling е показана по-долу:
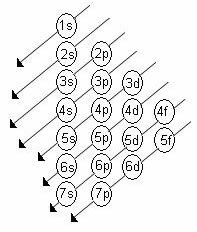
Основни правила:
1. Атомният номер (Z) на елемента, в неутрално състояние, показва броя на електроните, които трябва да бъдат разпределени. Този номер е представен в долната лява част на символа на елемента.
2. Използвайки диаграмата на Полинг, започнете да разпределяте електроните отгоре надолу, като вземете предвид нарастващия ред на енергията (ориентиран от посоката на стрелките).
3. Напълнете поднивата с максимално ниво на електрони. Ако дадено подниво съдържа само 6 електрона, не надвишавайте това количество.
4. Проверете броя на електроните, като ги съберете във всяко подниво.
Нека го приложим на практика?
Разпределете електроните на железния атом (Z = 26).
Ако атомният номер е 26, това означава, че в нормалния железен атом има 26 електрона. Прилагайки диаграмата на Полинг, ще имаме:

От Лирия Алвес
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm


