В обикновени батерии са наречени Батерии Leclanché кръстен на изобретателя си, френския химик Джордж Лекланче (1839-1882).

Джордж Лекланче (1839-1882)
Leclanché създава този тип батерии през 1866 година. Тя също се нарича суха клетка тъй като дотогава имаше само батерии, които използваха водни разтвори, като напр Купчината на Даниел.
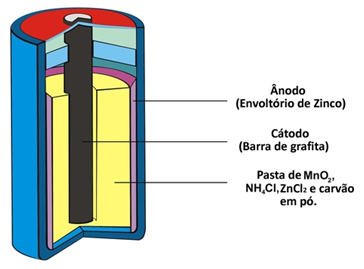
Две други имена, които този тип купчини получава поради конституцията си киселинна купчина или цинкова въглеродна батерия. Основно се формира от цинкова обвивка, отделена от останалите химически видове, които изграждат купчината посредством пореста хартия.
Този цинк съответства на отрицателния полюс на клетката или анода, тъй като той се окислява, губейки два електрона, съгласно полуреакцията по-долу:
Отрицателен полюс - анод: Zn (с) → Zn2+(тук) + 2 и-
Тази купчина също има положителен полюс катодът, който представлява графитна лента, монтирана в средата на купчината, заобиколена от манганов диоксид (MnO2), прахообразен въглен (С) и мокра паста, съдържаща амониев хлорид (NH4Cl), цинков хлорид (ZnCl2) и вода (H2О).
Амониевият хлорид и цинковият хлорид са соли с киселинен характер, откъдето идва и името „киселинни клетки”.
Графитната лента провежда електроните, загубени от цинка, до манган, намалявайки мангановия диоксид2) до манганов триоксид (Mn2О3), съгласно следната полуреакция:
Положителен полюс - Катод: 2 MnO2 (aq) + 2 NH41+(тук) + 2e- → 1 Mn2О3(с) + 2NH3 (g) + 1 час2О(1)
Влажната паста действа като солена точка, позволявайки миграцията на хидроксилни аниони (OH-) от графит до цинк.
Цялостната реакция се дава от:
Zn (с) + 2 MnO2 (aq) + 2 NH41+(тук) → Zn2+(тук) + 1 Mn2О3(с) + 2NH3 (g)
Като такива, тези батерии не се презареждат, тъй като целият манганов диоксид се превръща в манганов триоксид. Когато батерията спре да работи, тя трябва да бъде изхвърлена.
Ddp на тези батерии е 1,5V. Въпреки това, амонякът (NH3 (g)), образуван на катода, може да се отложи върху графитната лента, затруднявайки преминаването на електрони и намалявайки напрежението на батерията. За да се върнете към нормална работа, просто оставете батерията да почива извън устройството, като цинковия катион (Zn2+(тук)), образуван на анода, реагира с амоняк, оставяйки графитната лента свободна.
Освен това поставянето на купчината в хладилника също може да помогне, тъй като понижаването на температурата благоприятства разтворимостта на амоняка във влажната паста в купчината.
Друг важен фактор за сухите клетки на Leclanché, който трябва да имаме предвид, е този цинковият корпус може да корозира и по този начин да изтече корозивния материал и да повреди устройството.. Затова най-доброто нещо е да не оставяте батериите вътре в устройства, които не се използват непрекъснато.
Сухите батерии са показани за оборудване, което изисква леко и непрекъснато разреждане, като дистанционно управление, стенен часовник, преносимо радио и играчки.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/pilha-seca-leclanche.htm

