Ковалентната връзка възниква, когато два атома споделят двойки електрони, за да придобият електронната конфигурация на an благороден газ (с 8 електрона във валентната обвивка или с 2, в случая с тези само с K черупката), съгласно правилото на октет.
Има обаче специални случаи на ковалентни връзки, при които споделената електронна двойка идва само от един от атомите, който вече е стабилен. Преди това беше наречен този тип ковалентна връзка дателен, днес по-често се нарича координира.
Вижте няколко примера, за да разберете как се случва това:
- CO (въглероден оксид):
Въглеродът има 4 електрона във валентната си обвивка. Следователно, според правилото на октета, за да бъде стабилен, той трябва да получи още 4 електрона, общо 8. От друга страна, кислородът има 6 електрона във валентната обвивка и трябва да получи 2 електрона, за да получи конфигурацията на неона на благородния газ.
Първо, въглеродът и кислородът споделят две двойки електрони, така че кислородът да е стабилен:
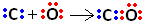
Въглеродът обаче остава нестабилен, тъй като все още има 6 електрона и се нуждае от 2. Следователно кислородът, който вече е стабилен, споделя една от своите двойки електрони с въглерод, тоест свързва дативна връзка с него, което го прави стабилен:

Обърнете внимание, че координатната ковалентна връзка може да бъде представена с тире, точно като общата ковалентна връзка.
- САМО2 (Серен диоксид):
Всеки атом на сяра и кислород има 6 електрона във валентните си обвивки, така че те трябва да получат по 2 електрона всеки. Първоначално сярата образува две общи ковалентни връзки, споделяйки две двойки електрони с един от кислородните атоми, като и двата остават стабилни с 8 електрона.
Но другият кислороден атом не е стабилен, така че сярата споделя двойка от своите електрони с него чрез координирана или дативна ковалентна връзка:
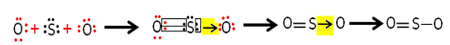
Имайте предвид, че в този случай имаме три атома в молекулата, така че може да има миграция на връзката от един атом към друг. Молекулата на серен диоксид също може да бъде представена по следния начин: O ─ S ═ O.
Ние наричаме това свързващо явление резонанс. Вижте още три примера в таблицата по-долу:
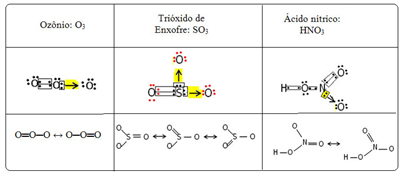
Извикват се възможни структури резонансни структури или канонични форми.
Този тип връзка се среща и при образуването на йони, както при хидрониевите йони (Н3О+) и амоний (NH4+).
Първо, катионът Н+ образува се, когато водородът загуби единичния си електрон, оставяйки го с положителен заряд. Така че ще трябва да получи два електрона, за да бъде стабилен. Това се случва чрез дативна връзка с вода (в случай на хидрониев йон) и с амоняк (в случай на амониев йон). Гледам:

От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/ligacao-covalente-dativa-ou-coordenada.htm

