Помислете за общата обратима реакция по-долу, където малките букви съответстват на балансираните коефициенти на реакция, а големите букви са реагентите и всички продукти са газообразни:

Разглеждайки всяка от посоките на реакцията поотделно, степента на тяхното развитие (Td) се дава от
* Директна реакция: aA + bB → cC + dD
всичкодиректен = Kдиректен. [THE]The. [B]Б.
* Обратна реакция: cC + dD → aA + bB
всичкообратна = Kобратен. [° С]° С. [Д]д
Константата на химическото равновесие по отношение на концентрацията в количество вещество (K° С) и по отношение на парциалното налягане (KP) ще бъде дадено чрез разделяне на Kдиректен от Кобратен.
Така че имаме:
Кдиректен. [THE]The. [B]Б. = 1 → Кдиректен__ = __[° С]° С. [Д]д___
Кобратен. [° С]° С. [Д]д Кобратен [THE]The. [B]Б.
Същество, К° С =_Kдиректен_
Кобратен
Така че имаме:
К° С =__[° С]° С. [Д]д___ или КP =__(Praça)° С. (pD)д___ |
Където p е парциалното налягане на всяко вещество в равновесие.
По този начин всяка концентрация се повишава до степен, съответстваща на коефициента на съответното вещество в реакцията, и К
° С няма единица *.В допълнение, много важен аспект, който трябва да се подчертае, е този в този изразне трябва да се представят нито твърди компоненти, нито чисти течности., тъй като в този израз участват само материи, които могат да претърпят вариация. Концентрацията в количество вещество на веществото в твърдо състояние е постоянна и по този начин вече е включена в стойността на самия К.° С. Същото важи и за чистите течности като водата. Накратко, в експресията участват само вещества в газообразно състояние и във воден разтвор.
Обърнете внимание на примерите по-долу:
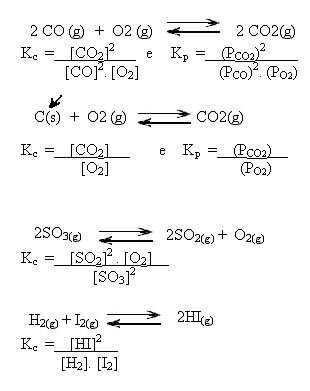
K стойности° С може да ни покаже дали концентрацията на реагентите и продуктите са еднакви или единият е по-голям от другия:
- ако К° С или КP е равно на единица (K° С = 1), това означава, че концентрацията на реагентите и продуктите е еднаква;
- Ако стойността на К° С или КP бъдете високи, това означава, че продуктите са в по-голяма концентрация, тъй като в израза на K° С продуктите са в числителя;
- Ако стойността на К° С или КP е ниско, това означава, че реагентите са в по-висока концентрация, тъй като в експресията на К° С реагентите са в знаменателя.
* К° С и КP те са безразмерни числа, тоест чисти числа, без единица, свързана с каквато и да е величина или връзка между величините.
От Дженифър Фогаса
Завършва химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm
