Алкохолите могат да бъдат подложени на окисляване, когато са изложени на окислител, като воден разтвор на калиев дихромат (K2Кр2О7) или калиев перманганат (KMnO4) в кисела среда.
Зараждащ се кислород [O] в средата ще атакува въглерода, свързан с алкохолната функционална група (хидроксил - OH), образувайки много нестабилно съединение, наречено двоен диол, което има два хидроксилни групи, свързани към едно и също въглерод. Тъй като е нестабилно, това съединение отделя вода и води до нов продукт.
Този продукт ще зависи от вида алкохол, който е бил окислен, независимо дали е първичен, вторичен, третичен или метанол.
Накратко имаме:
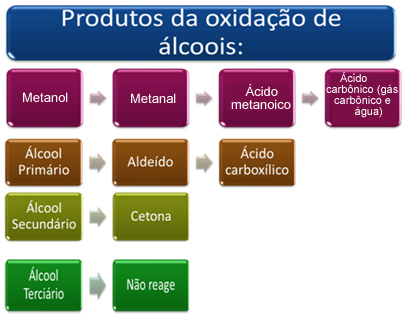
Вижте всеки случай по-долу:
- Метанол (H3C─ OH):
Метанолът е единственият алкохол, който има три водорода, свързани с въглерода, които ще бъдат подложени на окисляване. В този случай, тъй като има три точки на молекулата, които зараждащият се кислород може да атакува, ще настъпят три последователни окисления, както е показано на диаграмата по-долу:
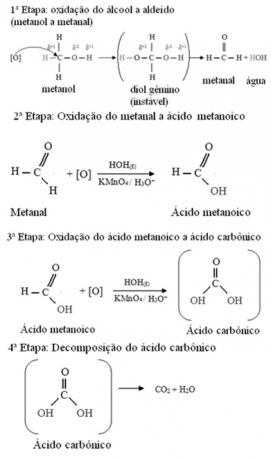
- Първични алкохоли:
В тези съединения хидроксилният въглерод е свързан само с един въглероден атом, тоест другите два лиганда са водороди и има две места за атака на зараждащия се кислород.
Първо, ще има образуване на алдехид, както е показано по-долу:
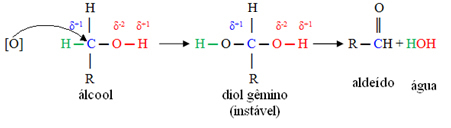
Но окисляването продължава, тъй като реагентите, използвани за окисляване на алкохола, са по-силни от тези, използвани за окисляване на алдехид. След това друг зараждащ се кислород атакува карбонилния въглерод и произвежда карбоксилна киселина.
Следва пример за окисляване на етанол, първо до етанал и след това до етанова киселина (оцетна киселина). Тази пълна реакция е превръщането на виното в оцет.
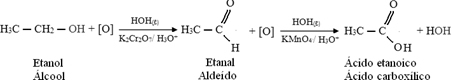
Частично окисление на етанол до етанал се случва, когато алкохолик направи тест с алкотестер за еднократна употреба. Вътре в това устройство има твърда смес от калиев бихромат и силициев диоксид в кисела среда, като протича следната реакция:
К2Кр2О7(aq) +4Н2САМО4(aq) + 3 CH3CH2о(ж) → Кр2(САМО4)3(aq) + 7 сутринта2О(1) + 3 CH3CHO(ж) + К2САМО4(aq)
оранжевоетанол (безцветен)зеленоетанал (безцветен)
Имайте предвид, че в допълнение към окисляването на етанол (алкохол) до етанал (алдехид), има едновременно редукция на дихромат, който е оранжев, до хром (III) или дори хром (II), който е зелен. Промяната в цвета ще покаже, че човекът има повече алкохол в кръвта, отколкото е позволено.
- Вторични алкохоли:
Това са съединения, в които хидроксилният въглерод е свързан с два други въглеродни атома и само един водороден атом. Следователно, ще има само едно място в молекулата, където зараждащият се кислород може да атакува и ще се образува само един вид продукт, който винаги ще бъде кетон:
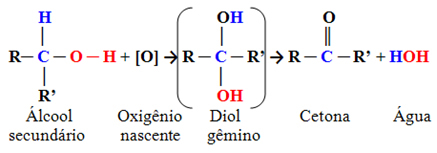
Тъй като карбониловият въглерод на кетона няма водород, свързан директно с него, вече няма никаква възможност за по-нататъшно окисление. Следователно, реакцията спира на кетона.
- Третични алкохоли:
Третични алкохоли са тези, при които въглеродът, който има -OH групата, прави три връзки с други въглеродни атоми. Тъй като те не се свързват с водороди, няма точка от молекулата, която може да бъде атакувана от зараждащ се кислород. Поради този факт третичните алкохоли не се подлагат на окисляване.
* Източник и автор на изображението: CostaPPPR.
От Дженифър Фогаса
Завършил химия
Източник: Бразилско училище - https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm
