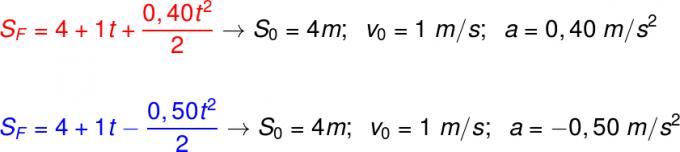Третият закон на термодинамиката се занимава с поведението на материята с ентропия, приближаваща се до нула.
Според този закон, когато система е в термодинамично равновесие, нейната ентропия се доближава до нула.
Вторият закон на термодинамиката се отнася до ентропията. Впоследствие третият закон се появява като a опит за установяване на абсолютна референтна точка, която определя ентропията.
Валтер Нернст (1864-1941) е физикът, който се занимава с принципите, които са в основата на третия закон на термодинамиката.
Според Нернст ентропията ще има тенденция да има минимална стойност, ако температурата на чисто вещество е равна или се приближава до абсолютната нула.
За това Нернст предложи формулата по-долу, която показва, че варирането на ентропията (ΔS) и температурата (T) има тенденция към минимални стойности, т.е. 0:
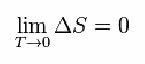
Но какво е Ентропия?
Ентропия това е начинът, по който молекулите се организират в системата. Тази организация се превръща в разстройство, не в смисъл на объркване, а в смисъл на движение и възбуда на молекулите.
Колкото повече молекули могат да се движат, толкова по-дезорганизирани са, толкова повече ентропия имат.
Първоначално Нернст предположи, че предложената от него ентропия ще бъде възможна само върху перфектни кристали.
Накрая той стигна до заключението, че температурата, равна на абсолютна нула, не съществува, което прави третия закон спорен закон.
Така че за много физици това не е закон, а правило.
След толкова много години (от 1912 г.) учените се опитват да получат тази температура или температури, които се приближават все повече до абсолютната нула. По този начин те откриха, че е възможно само в газове, изхвърляйки всяко вещество в твърдо или течно състояние.
Прочетете също:
- Нулев закон на термодинамиката
- Първи закон на термодинамиката
- Втори закон на термодинамиката
- Упражнения по термодинамика