Редът на химичната реакция е математическата връзка, която съществува между скоростта на развитие или скоростта на реакцията и концентрацията на количество вещество в реагентите.
Например, помислете за елементарната реакция, обхваната в текста Закон за скоростта за неелементарни реакции:
CO + NO2 → CO2 + НЕ
Законът за скоростта на тази реакция се дава от:
v = k. [НА2]2
Имаме, че в този случай глобалният ред на тази реакция ще бъде равен на 2, реда на реакцията по отношение на NO реагента2 той също ще бъде равен на 2 и по отношение на реагента СО ще бъде равен на нула.
Стигаме до това заключение, защото редът на глобалната реакция е сумата от степента на концентрациите на реагентите в закона. на скоростта и реда на реакцията спрямо даден реагент е степента на концентрацията му в закона на скорост.
Например, помислете, че имаме следната обща реакция:
aA + bB → cC + dD
Тъй като законът за скоростта на тази реакция е:
v = k. [THE]α. [B]β
Ние казваме, че тази обща реакция е:
- α ред по отношение на A;
- Ред β по отношение на B;
α + β = глобален ред на реакция
Вижте още два примера:
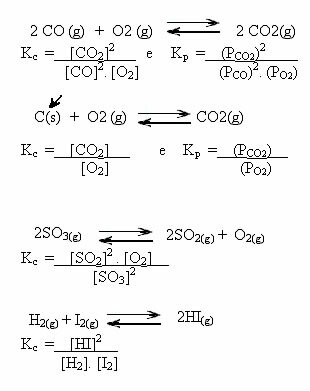
1) Елементарна реакция: 2 CO(ж) + O2 (g)→ 2 CO2 (g)
Не спирайте сега... Има още след рекламата;)
Тъй като това е елементарна реакция, степента в закона на скоростта е равна на коефициента на реагента: v = k. [CO]2. [O2]1
И така, имаме, че тази реакция е от порядък 2 по отношение на CO, от ред 1 по отношение на O2 и нейният глобален ред е 3 (2 + 1 = 3).
2) Неелементарна реакция: 2 часа2 (g) + 2 НЕ(ж)→ 1 N2 (g) + Н2О(ж)
Стъпките на тази реакция се дават от:
Етап 1 (бавен): Един час2 (g) + 2 НЕ(ж) → 1 N2Ож) + 2 Н2О(1)
Стъпка 2 (бърза): 1 N2Ож) + 2 Н2О(1) → 1 N2 (g) + 2 Н2О(1)
Глобално уравнение:2 часа2 (g) + 2 НЕ(ж) → 1 N2 (g) + 2 Н2О(1)
Показателите в закона за скоростта се дават от коефициентите на реагентите в бавен етап: v = k [Н2]1. [НА]2.
Тази реакция е от 1ª ред по отношение на H2, в 2ª ред по отношение на NO и на 3ª ред по отношение на глобалната реакция (сума на показателите: 1 + 2 = 3).
Едно ЗабележкаВажно е, че има някои реакции, които протичат на повърхността на метали с нулев ред, тъй като скоростта не зависи от концентрацията на реагентите.
От Дженифър Фогаса
Завършва химия
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
FOGAÇA, Дженифър Роча Варгас. „Ред за реакция“; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/ordem-reacao.htm. Достъп на 27 юни 2021 г.