В реакции на добавянев алкени(въглеводороди, които имат двойна връзка между два въглеродни атома), връзката pi между два въглерода се прекъсва и всеки от въглеродните атоми се свързва с нов атом. Виж:
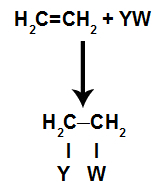
Общ схематичен модел на реакция на присъединяване
Принципи на реакция на присъединяване
а) Прекъсване на връзката pi
Пи връзката лесно се прекъсва, защото е по-слаба връзка от сигма връзката. За да се случи обаче, е необходимо алкенът да бъде подложен на условия, които осигуряват това разрушаване. След прекъсване на връзката pi между два въглерода, мястото за свързване (за нови атоми) винаги се появява на всеки от участващите въглероди.
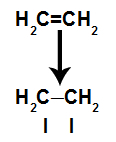
Схема, изобразяваща прекъсване на връзката pi
б) Условия за разкъсване на пи връзката
Факторите, които благоприятстват скъсването на връзката pi са:
Използване на катализатори;
Отопление;
Наличие на киселина в реакционната среда.
в) Появата на реакцията на присъединяване
Местата на свързване, създадени след разрушаване на пи-връзката, винаги ще бъдат заети от атоми на реагента, който се намира в същия контейнер като алкена. Реакцията на добавяне е кръстена на вида на реагента, смесен с алкена.
Видове реакции на присъединяване в Алкенес
а) Хидрогениране
Алкенът се смесва с водород (H2) в контейнер и подложен на действието на твърд катализатор (никел, платина или паладий) и нагряване (Δ).
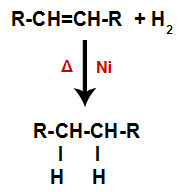
Обща схема на реакция на хидрогениране в алкени
Присъствието на катализатора и нагряването причиняват пи връзката на алкена и сигма връзката между водородите на Н2 да бъдат счупени по-бързо. С това имаме създаването на две свързващи места в алкена и два свободни водородни атома в реакционната среда.

Създаване на места за свързване и разделяне на атоми
Така веднага след това всеки свободен водороден атом заема едно от местата за свързване, образувани в алкена. Тъй като образуваното вещество има само въглерод и водород, както и само прости връзки между въглеродите, то е a алкан.
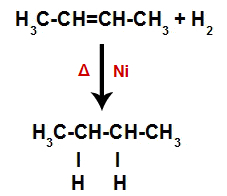
Уравнение, представляващо образуването на алкан при хидрогениране
Б) Халогениране
Алкенът се смесва с прости вещества (F2, Cl2, бр2 Хей2), образуван от халогени (хлор, флуор, йод и бром) в контейнер и подложен на действието на светлина (λ) и нагряване (Δ).

Обща схема на реакция на халогениране в алкени
Действието на светлината и нагряването кара пи-връзката на алкена и сигма-връзката между образуваните от халогена вещества да се разкъсват по-бързо. С това имаме създаването на две места за свързване в алкена и два свободни халогенни атома в реакционната среда.
Не спирайте сега... Има още след рекламата;)

Създаване на места за свързване и разделяне на атоми
Така веднага след това всеки свободен халогенен атом заема едно от местата за свързване, образувани в алкена. Тъй като образуваното вещество има халоген, свързан със структура, съставена от въглеродни и водородни атоми, той е органичен халогенид.

Уравнение, представляващо образуването на органични халогениди при халогениране
в) Хидратация
Алкенът се смесва с вода (Н2O) в контейнер и подложен на действието на катализатор (в този случай сярна киселина).
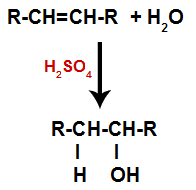
Обща схема на реакция на хидратация в алкени
Наличието на сярна киселина в реакцията кара пи-връзката на алкена и сигма-връзката между водорода (Н) и хидроксила (ОН) на водата да се разкъсат по-бързо. С това имаме създаването на две места за свързване в алкена и свободен водород и хидроксил в реакционната среда.
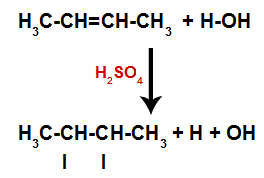
Създаване на места за свързване и разделяне на атоми
По този начин, малко след това, водородът и хидроксилът заемат едно от местата за свързване, образувани в алкена. Тъй като образуваното вещество има хидроксилна връзка с наситен въглерод (образува само прости връзки), това е алкохол.
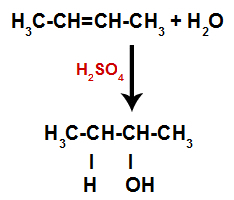
Уравнение, представляващо образуването на алкохол при хидратация
г) Добавяне с водородни халогениди
Алкен се смесва с халогенирана неорганична киселина (HF, HI, HCl, HBr) в контейнер.

Обща схема на киселинна халогенидна реакция в алкени
Наличието на киселина в реакцията кара пи-връзката на алкена да се разрушава по-бързо. Единичната връзка в киселината се прекъсва, тъй като тези вещества естествено йонизират. По този начин в алкена се създават две места за свързване и в реакционната среда има наличие на свободен водород и халоген.
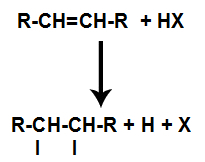
Създаване на места за свързване и разделяне на атоми
По този начин, малко след това, водородът и халогенът заемат едно от местата за свързване, образувани в алкена. Тъй като образуваното вещество има халоген, свързан със структура, съставена от въглерод и водород, това е органичен халогенид.
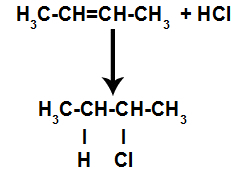
Уравнение, представляващо образуването на органични халогениди при халогениране
От мен Диого Лопес Диас
Искате ли да се позовавате на този текст в училище или академична работа? Виж:
ДНИ, Диого Лопес. „Реакции на добавяне в Алкени“; Бразилско училище. Наличен в: https://brasilescola.uol.com.br/quimica/reacoes-adicao-alcenos.htm. Достъп на 28 юни 2021 г.
Химия

Алкани, въглеводороди, метан, наситена верига, алифатни, парафини, горива, бензин, минерален восък, нефт, шисти, природен газ, нефтохимическа промишленост.
Химия

Алкени, газ, етен, етилен, пластмаси, синтетичен каучук, багрила, синтетични тъкани, експлозиви, петролен крекинг, полиетилен, олефиен газ, олефини, въглеводороди, верига ацикличен въглероден диоксид.
Алкини, етични въглеводороди, ацетиленови въглеводороди, ациклична въглеродна верига, въглеродна верига хомогенна, ненаситена въглеродна верига, тройна връзка, PVC, PVA, ацетилен, синтетични каучуци, пластмаси, жици текстил.
