Sabit bir sıcaklıkta aşağıdaki kimyasal dengeyi göz önünde bulundurun:
3 saat2(g) + N2(g) ↔ 2 NH3(g)
Gay-Lussac'a göre, bir reaksiyondaki gaz halindeki katılımcıların hacimlerinin oranı, ilgili stokiyometrik katsayıların oranına eşittir. Basit bir ifadeyle, reaktanlarda ve ürünlerde bulunan moleküllerin sayısının denklemdeki katsayılara eşit olduğunu söyleyebiliriz.
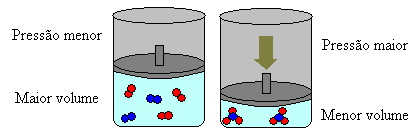
Yukarıdaki durumda, reaktiflerde 4 molekülümüz var ve ürünlerde 2 molekülümüz var, bu da reaktiflerin hacminin daha büyük ve ürünlerin hacminin daha küçük olduğu anlamına gelir.
Bu sistemdeki basıncı arttırırsak, bu basıncı azaltmak için denge daha küçük hacme doğru kayar. Düşündüğümüz reaksiyon durumunda, yer değiştirme doğrudan ürün oluşumu yönünde olacaktır (NH3(g)).
Bununla birlikte, basıncı düşürürsek, reaksiyon, reaktanların oluşumunun zıt yönü olan en büyük hacme doğru hareket edecektir (3 H2(g) + N2(g)).
Şimdi durma... Reklamdan sonra devamı var ;)
Bu, herhangi bir rahatsızlığın (basıncın azaltılması veya arttırılması gibi) neden olduğunu söyleyen Le Chatelier İlkesine göre gerçekleşir. dengedeki bir sistemde, kendisini yeni bir düzene yeniden ayarlayarak, bu bozukluğu en aza indiren yönde hareket etmesini sağlayacaktır. denge.
Basınç değişiminin kimyasal dengeye etkisi durumunda kısaca şunları söyleyebiliriz:
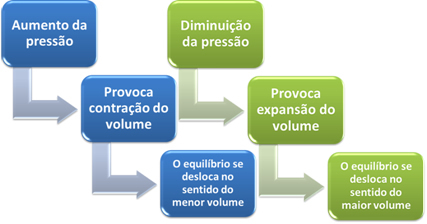
Tepkimeye girenlerin hacminin ürünlerin hacmine eşit olduğu tepkimelerde kimyasal denge değişmez.
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Basınç değişimi ve kimyasal dengenin yer değiştirmesi"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm. 28 Haziran 2021'de erişildi.
Kimya

Kimyasal dengelerle ilgili bu çözülmüş alıştırmalar listesiyle bilginizi sınayın ve daha fazlasını öğrenin. Bu materyal sayesinde, denge sabitlerinin (Kp, Kc ve Ki), denge kaymasının, pH ve pOH'nin ve ayrıca sözde tampon çözeltilerdeki dengenin nasıl çalıştığını daha iyi anlayabileceksiniz.



