bu entalpi (H) her malzemenin enerji içeriği veya bir sistemin toplam enerjisi olarak tanımlanabilir. Ancak bir maddenin entalpisini belirlemek pratikte mümkün değildir. Yani, genellikle ölçülen şey, entalpi değişimi 

Burada, ısı salınımının olduğu reaksiyonlar olan ekzotermik reaksiyonlardaki entalpi varyasyonunu analiz edeceğiz (“exo” kelimesi Yunancadan gelir ve “dışarı, dışarı, dışarı” anlamına gelir). Günlük yaşamda, yanma ve sönmemiş kirecin su ile karışımı gibi meydana gelen bu reaksiyonların birçok örneği vardır.
Bu durumlarda, entalpi değişimi 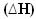 son entalpi eksi ilk entalpi (H) değeri ile verilen, tam olarak salınan ısı miktarı olacaktır.f -Hben) veya bir reaksiyon olduğu için, ürünlerin entalpi değeri eksi reaktanların entalpi değeri (HP -H$).
son entalpi eksi ilk entalpi (H) değeri ile verilen, tam olarak salınan ısı miktarı olacaktır.f -Hben) veya bir reaksiyon olduğu için, ürünlerin entalpi değeri eksi reaktanların entalpi değeri (HP -H$).
Isı açığa çıktıkça enerji kaybedilir. Böylece sistemin toplam enerjisi azalır, böylece ürünlerin entalpisi her zaman reaktiflerin, bu nedenle ekzotermik reaksiyonlardaki entalpi değişimi her zaman negatif olacaktır, sıfır 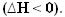
Şimdi durma... Reklamdan sonra devamı var ;)
Genel bir ekzotermik reaksiyon göz önüne alındığında:
| A → B + ısı |
Bu, aşağıdaki gibi bir entalpi diyagramı kullanılarak ifade edilebilir:
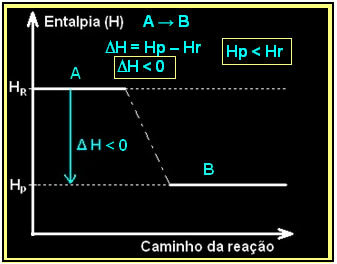
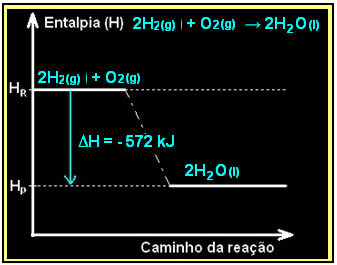
Sıvı su oluşumu ile hidrojen gazının yanması, enerjinin açığa çıkması ile gerçekleşir. Bu reaksiyonda sistemin entalpi değişiminin değeri şu şekilde verilir:
2 saat2(g) + O2(g) → 2H2Ö(1)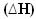 = - 572 kJ
= - 572 kJ
Diyagramınız aşağıdaki gibi temsil edilecektir:
Jennifer Foğaça tarafından
Kimya mezunu
Bu metne bir okulda veya akademik bir çalışmada atıfta bulunmak ister misiniz? Bak:
FOGAÇA, Jennifer Rocha Vargas. "Ekzotermik Reaksiyonlarda Entalpi Değişimi"; Brezilya Okulu. Uygun: https://brasilescola.uol.com.br/quimica/variacao-entalpia-reacoes-exotermicas.htm. 28 Haziran 2021'de erişildi.
Kimya

Termokimya, Entalpi, Yayılan Isı, Ekzotermik Reaksiyon, Yanma Reaksiyonu, Dış Ortam, Endotermik Reaksiyon, Reaksiyon kimya, enerji değişimi, reaktifler, ışık emisyonu, ışık absorpsiyonu, ısı, elektrik, bileşenler, fiziksel durum, Ürün:% s.



