Tonoscopy คือ กรรมสิทธิ์ร่วมกัน ที่ศึกษาการลดลงของ แรงดันไอน้ำสูงสุด ของตัวทำละลายที่กำหนดเนื่องจากการละลายของตัวถูกละลายที่ไม่ระเหย (โมเลกุลหรือไอออนิก) คุณสมบัติคอลลิเกทีฟอื่นๆ ได้แก่:
Ebulioscopy
cryoscopy
ออสโมสโคป
จากคำจำกัดความข้างต้น จะเห็นได้ว่า เข้าใจจริงๆ to Tonoscopy คืออะไร จำเป็นต้องรู้แนวคิดอื่นๆ อีกสามประการ:
มันคือแรงที่กระทำโดยไอน้ำ ของของเหลวบางชนิดบนผนังของภาชนะปิดเมื่ออัตราการระเหยเท่ากับอัตราการควบแน่น
ในภาชนะที่มีเอทานอลจำนวนหนึ่งซึ่งระเหยภายใต้อิทธิพลของอุณหภูมิของ สิ่งแวดล้อม เมื่อไอน้ำมาบรรจบกับผนังของภาชนะ มันก็จะจบลงที่ ของเหลว เมื่อเวลาผ่านไป อัตราการระเหยจะเท่ากับอัตราการควบแน่น ณ จุดนี้ แรงดันไอน้ำที่กระทำต่อผนังถังบรรจุเรียกว่าแรงดันไอน้ำสูงสุด
แผนที่จิต: Tonometry หรือ Tonoscopy

* ในการดาวน์โหลดแผนที่ความคิดในรูปแบบ PDF คลิกที่นี่!
การละลาย
เป็นความสามารถของตัวทำละลายในการละลายตัวถูกละลายบางชนิด. หลังจากการละลาย ตัวถูกละลายและตัวทำละลายเริ่มสร้างปฏิสัมพันธ์ระหว่างโมเลกุลระหว่างกัน กล่าวคือ พวกมันเชื่อมต่อถึงกัน
ตัวละลายไม่ระเหย
มันคือ วัสดุที่มีจุดเดือดสูงกล่าวคือไม่สามารถเปลี่ยนเป็นก๊าซที่อุณหภูมิแวดล้อมได้ เป็นต้น ดังนั้น เมื่อเติมลงในตัวทำละลายแล้ว
จะไม่สูญเสียวัสดุนี้ต่อสิ่งแวดล้อมในรูปของก๊าซ.โอ ตัวละลายโมเลกุลไม่ระเหย คือสิ่งที่ ไม่สามารถเกิดไอออไนซ์หรือแยกตัวออกได้ เมื่อละลายในตัวทำละลาย ดังนั้น หากเราเติมโมเลกุลของตัวถูกละลายนี้เข้าไปในตัวทำละลาย มันจะอยู่ตรงกลาง
คุณionic olute ที่ไม่ระเหย é ที่ทุกข์ทรมานจากปรากฏการณ์ของ ความแตกแยกหรือไอออไนซ์กล่าวคือเกิดการสลายตัวของพันธะระหว่างอะตอมซึ่งทำให้เกิด การแยกส่วนของหน่วยโมเลกุล. ถ้าเราละลายกรดซัลฟิวริก 1 โมล (H2เท่านั้น4) ในน้ำ ตัวอย่างเช่น เราจะมีไฮโดรเนียมไอออนบวกสองโมลและไอออนซัลเฟตหนึ่งโมลอยู่ตรงกลาง ดังแสดงในสมการด้านล่าง:
โฮ2เท่านั้น4 +2H2O → 2H+ + OS4-2
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
การชี้แจงแนวคิดพื้นฐานเหล่านี้จะทำให้เข้าใจ Tonoscopy ได้ง่ายขึ้นและชัดเจนขึ้น
ทำความเข้าใจ Tonoscopy
เพื่อให้เข้าใจ tonoscopy เรามาศึกษาพฤติกรรมของของเหลวอย่างน้ำและเอทานอลกัน จุดเดือดของตัวทำละลายทั้งสองนี้ตามลำดับ 100อู๋C และ 78อู๋ค. ดังนั้นเอทานอลจะระเหยเร็วกว่าน้ำเมื่ออยู่ในอุณหภูมิและปริมาณเท่ากัน
หากมีเอทานอล 50 มล. ในภาชนะหนึ่งและมีน้ำ 50 มล. ในภาชนะอื่นเช่นปิดและ 250อู๋C แรงดันไอน้ำสูงสุดในภาชนะเอทานอลจะสูงขึ้นเนื่องจากปริมาณไอน้ำภายในสูงขึ้น
การพูดแบบกราฟิกเมื่อใดก็ตามที่เส้นโค้งของของเหลวอยู่ห่างจากแกน y (แนวตั้ง) ความดันไอสูงสุดของของเหลวก็จะยิ่งต่ำลง ดังในกราฟด้านล่าง:
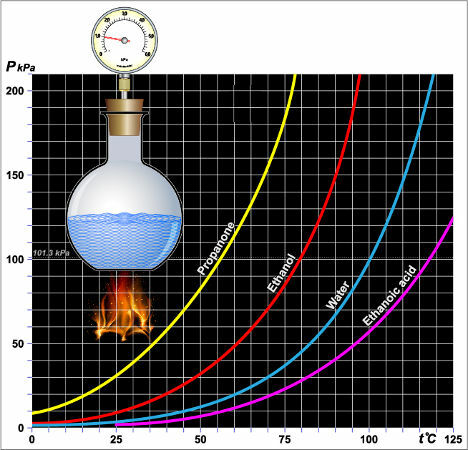
ความดันไอของของเหลวต่างๆ
คำบรรยายภาพ: โพรพาโนน = โพรพาโนน (อะซิโตน)
เอทานอล = เอทานอล
น้ำ = น้ำ
กรดเอทานิก = กรดเอทาโนอิก
ในกราฟ เราสามารถยืนยันได้ว่าความดันไอของเอทานอล (เส้นโค้งสีแดง) มากกว่าน้ำเสมอ (เส้นโค้งสีน้ำเงิน) ที่อุณหภูมิใดก็ได้
บันทึก: กล่าวโดยสรุป ยิ่งจุดเดือดของตัวทำละลายที่กำหนดสูงเท่าใด ความดันไอสูงสุดก็จะยิ่งต่ำลงและในทางกลับกัน
ชอบ Tonoscopy ศึกษาการลดลงของความดันไอสูงสุด เนื่องจากการละลายของตัวถูกละลายที่ไม่ระเหยในตัวทำละลาย หากเราผสมโซเดียมคลอไรด์ (NaCl) ในน้ำ ความดันไอน้ำสูงสุดที่ 100อู๋C ซึ่งเท่ากับ 760 mmHg จะลดลงอย่างแน่นอน แต่ทำไมสิ่งนี้ถึงเกิดขึ้น?
เมื่อโซเดียมคลอไรด์ (ตัวถูกละลายไอออน) ละลายในน้ำ ไอออนของโซเดียมจะทำปฏิกิริยากับโมเลกุลของน้ำ ปฏิกิริยานี้ทำให้การระเหยตัวทำละลายทำได้ยากขึ้น เนื่องจากการระเหยถูกขัดขวาง จะมีไอน้ำในภาชนะน้อยลง ซึ่งจะทำให้ความดันไอสูงสุดลดลง
ดังนั้น ยิ่งโซเดียมคลอไรด์มีปริมาณมากในน้ำปริมาณเท่ากัน การระเหยยิ่งยากขึ้นและความดันไอสูงสุดก็จะยิ่งต่ำลง
By Me. Diogo Lopes Dias
เคมี

การแยกตัวและการแตกตัวเป็นไอออน, นักวิทยาศาสตร์ชาวอิตาลีโวลตา, กระแสไฟฟ้า, นักเคมีกายภาพชาวสวีเดน Svant August Arrhenius, ทฤษฎีของ อาร์เรเนียส, ไอออนบวก, ไพเพอร์, ไอออนลบ, แอนไอออน, โซดาไฟ, เกลือแกง, โมเลกุลมีขั้ว, การแยกตัวออกจากกัน อิออน,
เคมี

สมบัติคอลลิเกทีฟ, โทนอสโคปี, อีบูลลิออสโคปี, ไครออสโคปี, ออสโมสโคปี, ผลคอลลิเกทีฟ, การลดศักยภาพทางเคมี ของตัวทำละลาย อุณหภูมิจุดเดือด จุดหลอมเหลว จุดหลอมเหลว แรงดันออสโมติก ตัวถูกละลายที่ไม่ระเหย ตัวถูกละลาย ตัวทำละลาย เทมเป้


