โอ รัศมีอะตอม (r) มักจะถูกกำหนดเป็น ครึ่งหนึ่งของระยะห่างระหว่างนิวเคลียสสองนิวเคลียสของอะตอมข้างเคียงดังรูปด้านล่างแสดงถึง:

รัศมีอะตอม
รัศมีอะตอมแตกต่างกันไปในแต่ละอะตอมตามตระกูลและระยะเวลาในตารางธาตุ เกี่ยวกับองค์ประกอบที่เป็นของ ตระกูลเดียวกันรัศมีอะตอมจะเพิ่มขึ้นเมื่อเลขอะตอมเพิ่มขึ้นนั่นคือจากบนลงล่าง สำหรับในแง่นี้ มันหมายความว่าจากอะตอมหนึ่งไปยังอีกอะตอมหนึ่งมีระดับพลังงานหรือชั้นอิเล็กทรอนิกส์เพิ่มขึ้น ดังนั้นรัศมีของอะตอมจึงเพิ่มขึ้นตามสัดส่วน
ว่าด้วยเรื่องธาตุ ในช่วงเวลาเดียวกัน, นั่นคือ, แนวนอน, รัศมีเพิ่มขึ้นจากขวาไปซ้ายหรือเมื่อเลขอะตอมลดลง. เนื่องจากแต่ละชั้นมีจำนวนชั้นเท่ากัน สิ่งที่ทำให้เกิดความแตกต่างคือปริมาณของ อิเล็กตรอนในชั้นเหล่านี้ และยิ่งมีอิเล็กตรอนมากเท่าใด นิวเคลียสก็จะยิ่งดึงดูดมากขึ้น รัศมีของ อะตอม.

ทิศทางการเติบโตของรัศมีอะตอมตามตระกูลและระยะเวลาในตารางธาตุ
อย่างไรก็ตามรัศมีอะตอมอาจแตกต่างกันไปขึ้นอยู่กับการเชื่อมต่อที่ทำ มาดูกันว่าสิ่งนี้เกิดขึ้นได้อย่างไร:
*พันธะไอออนิก: ถ้าอะตอมสร้าง a ไอออนบวก รัศมีอะตอมจะลดลงเนื่องจากสูญเสียอิเล็กตรอนไปหนึ่งตัวหรือมากกว่า นิวเคลียสจะดึงดูดอิเล็กตรอนมากขึ้น ตอนนี้ถ้า
เกิดเป็นประจุลบ กล่าวคือ ได้รับอิเล็กตรอน รัศมีของอะตอมจะเพิ่มขึ้นเนื่องจากประจุทั้งหมดของอิเล็กโตรสเฟียร์จะมากกว่าประจุทั้งหมดของนิวเคลียส แรงดึงดูดจึงลดลง ยิ่งคุณได้รับหรือสูญเสียอิเล็กตรอนมากเท่าใด ขนาดของลำแสงก็จะยิ่งเปลี่ยนแปลงมากขึ้นเท่านั้นอย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
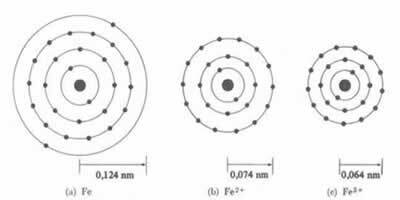
เส้นผ่านศูนย์กลางหรือรัศมีของไอออนบวกนั้นเล็กกว่าเส้นผ่านศูนย์กลางหรือรัศมีของอะตอมเสมอ
นอกจากนี้ในชุดของ ไอออนไอโซอิเล็กทรอนิกส์ซึ่งมีอิเล็กตรอนและระดับพลังงานเท่ากัน ไอออนที่มีเลขอะตอมน้อยที่สุดจะมีรัศมีมากกว่า ตัวอย่างเช่น ไอออน 13อัล3+, 12มก.2+, 11ที่1+, 9F-1, 8โอ2- และ 7นู๋-3ทั้งหมดมี 10 อิเล็กตรอนและ 2 ระดับอิเล็กทรอนิกส์ แต่รัศมีที่ใหญ่ที่สุดคือ largest 7นู๋-3เพราะมันมีเลขอะตอมน้อยที่สุด (Z= 7)
*พันธะโควาเลนต์: เมื่อสองอะตอมสร้างพันธะโควาเลนต์ ถ้าสองอะตอมเท่ากันเช่นเดียวกับในกรณีของก๊าซไฮโดรเจน (โฮ2), เราสามารถพูดถึงรัศมีโควาเลนต์ (r) ซึ่งเป็นครึ่งหนึ่งของความยาวของพันธะ (d) นั่นคือครึ่งหนึ่งของระยะทางที่แยกนิวเคลียสทั้งสอง. แม้ว่า, ถ้าพันธะเกิดจากอะตอมต่างกันเช่นเดียวกับในกรณีของไฮโดรเจนคลอไรด์ (HCl) ความยาวหรือระยะทาง (d) จะเป็นผลรวมของรัศมีโควาเลนต์ (r1 + r2) ของอะตอมที่เกี่ยวข้องกับโควาเลนซ์
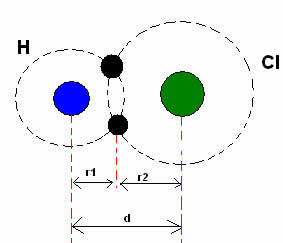
ผลรวมของรัศมีอะตอมในพันธะโควาเลนต์
แน่นอน เราต้องจำไว้ว่าปัญหานี้ซับซ้อนกว่ามาก เนื่องจากรัศมีโควาเลนต์ของอะตอมสามารถแปรผันตามพันธะกับอะตอมอื่น
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "ความแปรปรวนของรัศมีอะตอมในพันธะเคมี"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/variacao-raio-atomico-ligacoes-quimicas.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.

