ที่ พันธะเคมี คือปฏิกิริยาที่เกิดขึ้นระหว่างอะตอมจนกลายเป็นโมเลกุลหรือสารพื้นฐานของสารประกอบ ลิงค์มีสามประเภท: โควาเลนต์, เมทัลลิก และ อิออน อะตอมแสวงหาโดยการสร้างพันธะเคมีเพื่อทำให้ตัวเองเสถียรทางอิเล็กทรอนิกส์ กระบวนการนี้อธิบายโดย ทฤษฎีออคเต็ตซึ่งกำหนดว่าแต่ละอะตอมเพื่อให้เกิดความเสถียรต้องมีอิเล็กตรอนแปดตัวในเปลือกเวเลนซ์
พันธะเคมีและกฎออคเต็ต
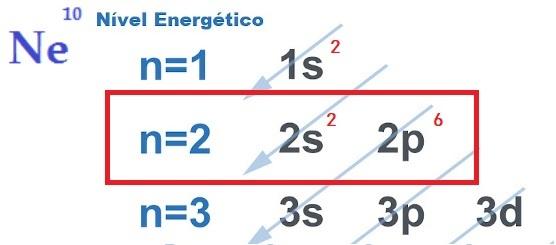
เธ ค้นหาเสถียรภาพทางอิเล็กทรอนิกส์ ซึ่งแสดงให้เห็นถึงความสมเหตุสมผลของพันธะเคมีระหว่างอะตอมอธิบายโดย ทฤษฎีออคเต็ต. เสนอโดยนิวตัน ลูอิส ทฤษฎีนี้ระบุว่าปฏิกิริยาของอะตอมเกิดขึ้นเพื่อให้แต่ละองค์ประกอบได้รับความเสถียรของก๊าซมีตระกูล กล่าวคือ แปดอิเล็กตรอนใน ชั้นวาเลนซ์.
สำหรับสิ่งนี้องค์ประกอบ ให้ รับ หรือแบ่งปัน อิเล็กตรอนจากเปลือกนอกสุด ทำให้เกิดพันธะเคมีที่มีลักษณะเป็นไอออนิก โควาเลนต์ หรือโลหะ คุณ ก๊าซมีตระกูล พวกมันเป็นอะตอมเพียงอะตอมเดียวที่มีอิเล็กตรอนแปดตัวในเปลือกนอกสุดของพวกมัน และนั่นเป็นสาเหตุที่พวกมันไม่ทำปฏิกิริยากับองค์ประกอบอื่นมากนัก
ดูยัง: กฎการจำหน่ายทางอิเล็กทรอนิกส์: ทำอย่างไร
ประเภทของพันธะเคมี
เพื่อให้ได้อิเล็กตรอนแปดตัวในเปลือกเวเลนซ์ตามที่ทำนายโดยกฎออกเตต อะตอมจะยึดติดกัน ซึ่งแตกต่างกันไปตามความจำเป็นในการบริจาค รับ หรือแบ่งอิเล็กตรอน และลักษณะของพันธะอะตอม
พันธะไอออนิก
ยังเป็นที่รู้จักกันในนาม พันธะอิเล็กโทรวาเลนต์หรือเฮเทอโรโพลาร์เกิดขึ้นระหว่าง โลหะ และองค์ประกอบทางไฟฟ้ามาก (อเมทัลและไฮโดรเจน) ในการโทรประเภทนี้ โลหะมักจะสูญเสียอิเล็กตรอน กลายเป็นไอออนบวก (ไอออนบวก) และอโลหะและไฮโดรเจนได้รับอิเล็กตรอน กลายเป็นแอนไอออน (ไอออนลบ)
คุณ สารประกอบไอออนิก มีความแข็งและเปราะ มีจุดเดือดและนำไฟฟ้าสูง กระแสไฟฟ้า เมื่ออยู่ในสถานะของเหลวหรือเจือจางในน้ำ
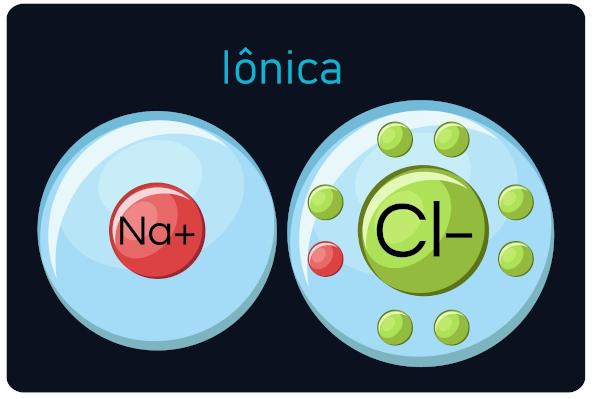
การสังเกต: โปรดทราบว่าอะตอมที่ได้รับอิเล็กตรอนจะกลายเป็นไอออนที่มีเครื่องหมายลบ และอะตอมที่สูญเสียอิเล็กตรอนจะกลายเป็นสัญญาณบวก
ตัวอย่างของสารไอออนิก:
- ไบคาร์บอเนต (HCO3-);
- แอมโมเนียม (NH4+);
- ซัลเฟต (SO4-).
หากต้องการเรียนรู้เพิ่มเติมเกี่ยวกับพันธะเคมีประเภทนี้ โปรดไปที่เนื้อหาของเรา: พันธะไอออนิก.
พันธะโควาเลนต์
ที่ พันธะโควาเลนต์ เกิดขึ้นโดย การแบ่งปันอิเล็กตรอน. เนื่องจากความแตกต่างของอิเล็กโตรเนกาติวีตี้ต่ำระหว่างองค์ประกอบการจับ พวกมันจะไม่บริจาคหรือรับอิเล็กตรอน แต่ แบ่งปันคู่อิเล็กทรอนิกส์ เพื่อให้มีเสถียรภาพตามกฎออกเตต การเชื่อมต่อประเภทนี้พบได้ทั่วไปในองค์ประกอบง่ายๆ เช่น Cl2, H2, O2และในโซ่คาร์บอนด้วย ความแตกต่างของ อิเล็กโตรเนกาติวีตี้ ระหว่างแกนด์เป็นตัวกำหนดว่าพันธะมีขั้วหรือไม่มีขั้ว

อ่านด้วย:ขั้วของโมเลกุล: วิธีการระบุ?
พันธะโควาเลนต์ dative
เรียกอีกอย่างว่า พันธะโควาเลนต์ พันธะกึ่งขั้ว พันธะเดทีฟหรือพันธะประสาน มันคล้ายกับพันธะโควาเลนต์มาก ความแตกต่างระหว่างทั้งสองคือหนึ่งในอะตอมในพันธะดาทีฟรับผิดชอบในการแบ่งปันอิเล็กตรอนสองตัว ในการเชื่อมต่อประเภทนี้ว่า เกิดขึ้นเทียม, โมเลกุลได้มาซึ่งคุณลักษณะเดียวกันกับโมเลกุลที่เกิดจากพันธะโควาเลนต์ที่เกิดขึ้นเอง
ลิงค์โลหะ
พันธะประเภทนี้เกิดขึ้นระหว่างโลหะซึ่งรวมถึงองค์ประกอบของตระกูล 1A (โลหะอัลคาไล), 2A (โลหะอัลคาไลน์เอิร์ ธ) และโลหะทรานซิชัน (บล็อก B ของตารางธาตุ - กลุ่ม 3 ถึง 12) สร้างสิ่งที่เราเรียกว่า โลหะผสม. ลักษณะความแตกต่างที่สัมพันธ์กับการเชื่อมต่อประเภทอื่นคือ การเคลื่อนที่ของอิเล็กตรอนซึ่งอธิบายข้อเท็จจริงที่ว่าวัสดุโลหะในสถานะของแข็งเป็นตัวนำไฟฟ้าและความร้อนที่ดีเยี่ยม นอกจากนี้ โลหะผสมยังมีจุดหลอมเหลวและจุดเดือด ความเหนียว ความอ่อนตัว และเงาสูง ตัวอย่างของโลหะผสม ได้แก่
เหล็ก: เหล็ก (Fe) และคาร์บอน C;
บรอนซ์: ทองแดง (Cu) + ดีบุก (Sn);
ทองเหลือง: ทองแดง (Cu) + สังกะสี (Zn);
ทอง: ทอง (Au) + ทองแดง (Cu) หรือเงิน (Ag)

สรุป
- พันธะเคมี: ปฏิสัมพันธ์ระหว่างอะตอมที่แสวงหาเสถียรภาพทางอิเล็กทรอนิกส์
- ประเภทของลิงค์: ไอออนิก โควาเลนต์ และเมทัลลิก
- กฎออคเต็ต: กำหนดว่า เพื่อให้อะตอมมีความเสถียร จะต้องมีอิเล็กตรอนแปดตัวในเปลือกเวเลนซ์ของมัน
แก้ไขแบบฝึกหัด
คำถามที่ 1 - (Mackenzie-SP) เพื่อให้อะตอมของกำมะถันและโพแทสเซียมได้รับการกำหนดค่าทางอิเล็กทรอนิกส์เท่ากับของก๊าซมีตระกูล จำเป็นที่:
(ข้อมูล: เลขอะตอม S = 16; เค = 19)
ก) กำมะถันได้รับ 2 อิเล็กตรอนและโพแทสเซียมได้รับ 7 อิเล็กตรอน
b) กำมะถันให้อิเล็กตรอน 6 ตัวและโพแทสเซียมได้รับ 7 อิเล็กตรอน
c) กำมะถันให้อิเล็กตรอน 2 ตัว และโพแทสเซียมให้อิเล็กตรอน 1 ตัว
d) กำมะถันได้รับ 6 อิเล็กตรอนและโพแทสเซียมให้ 1 อิเล็กตรอน
จ) กำมะถันได้รับ 2 อิเล็กตรอนและโพแทสเซียมให้ 1 อิเล็กตรอน
ความละเอียด
ทางเลือก E เนื่องจากกำมะถันอยู่ในตระกูล 6A หรือ 16 ซึ่งเป็นไปตามกฎออกเตต จึงต้องได้รับอิเล็กตรอน 2 ตัวจึงจะมี 8 อยู่ในเปลือกเวเลนซ์ของมัน โพแทสเซียมซึ่งอยู่ในตระกูลแรกของตารางธาตุ (1A หรือตระกูลไฮโดรเจน) เพื่อให้มีการกำหนดค่าของก๊าซมีตระกูลในชั้นเวเลนซ์จะต้องสูญเสียอิเล็กตรอน 1 ตัว การรวมอะตอมของโพแทสเซียม 2 อะตอมกับอะตอมของกำมะถัน 1 อะตอม เราสามารถสร้างพันธะไอออนิกซึ่งธาตุทั้งสองมีความเสถียรทางไฟฟ้า
คำถาม2 - (UFF) นมแม่เป็นอาหารที่อุดมไปด้วยสารอินทรีย์ เช่น โปรตีน ไขมันและน้ำตาล และสารแร่ธาตุ เช่น แคลเซียม ฟอสเฟต สารประกอบอินทรีย์เหล่านี้มีลักษณะเฉพาะของพันธะโควาเลนต์ในการก่อตัวของโมเลกุล ในขณะที่แร่ธาตุก็มีพันธะไอออนิกเช่นกัน ตรวจสอบทางเลือกที่นำเสนอแนวคิดของพันธะโควาเลนต์และไอออนิกอย่างถูกต้องตามลำดับ:
ก) พันธะโควาเลนต์เกิดขึ้นในสารประกอบอินทรีย์เท่านั้น
b) พันธะโควาเลนต์ทำได้โดยการถ่ายโอนอิเล็กตรอน และพันธะไอออนิกทำได้โดยใช้อิเล็กตรอนร่วมกันกับสปินที่ตรงกันข้าม
c) พันธะโควาเลนต์เกิดจากการดึงดูดของประจุระหว่างอะตอม และพันธะไอออนิกเกิดจากการแยกประจุ
d) พันธะโควาเลนต์เกิดขึ้นจากการรวมอะตอมในโมเลกุล และพันธะไอออนิก โดยการรวมอะตอมในสารเชิงซ้อนทางเคมี
จ) พันธะโควาเลนต์ทำได้โดยใช้อิเล็กตรอนร่วมกัน และพันธะไอออนิกทำได้โดยการถ่ายโอนอิเล็กตรอน
ความละเอียด
ทางเลือก E
ลองวิเคราะห์คนอื่น ๆ :
- ทางเลือกแทน: ไม่ถูกต้องเนื่องจากพันธะโควาเลนต์ยังเกิดขึ้นในสารประกอบอนินทรีย์เช่น CO2.
- ทางเลือก b: ไม่ถูกต้อง เนื่องจากพันธะโควาเลนต์เกิดขึ้นจากการแบ่งปัน และพันธะไอออนิกโดยการถ่ายโอนอิเล็กตรอน
- ทางเลือก c: ทั้งพันธะโควาเลนต์และพันธะไอออนิกเกิดขึ้นจากความจำเป็นในการสูญเสียหรือรับอิเล็กตรอน ไม่ได้เกิดจากการดึงดูดด้วยไฟฟ้าสถิตระหว่างนิวเคลียส
- ทางเลือก d: พันธะทั้งสอง ทั้งโควาเลนต์และไอออนิก เกิดขึ้นจากการรวมตัวกันของอะตอมในโมเลกุล
คำถาม 3 - (PUC-MG) ตรวจสอบตารางซึ่งแสดงคุณสมบัติของสารสามชนิด X, Y และ Z ภายใต้สภาวะแวดล้อม
| สาร | อุณหภูมิหลอมเหลว (c°) | การนำไฟฟ้า | การละลายในน้ำ |
| x | 146 | ไม่มี |
ละลายน้ำได้ |
| y | 1600 | สูง | ไม่ละลายน้ำ |
| z | 800 | แค่ละลายหรือละลายในน้ำ | ละลายน้ำได้ |
เมื่อพิจารณาจากข้อมูลนี้ เป็นการถูกต้องที่จะระบุว่าสาร X, Y และ Z ตามลำดับ:
ก) อิออน, โลหะ, โมเลกุล
b) โมเลกุล, อิออน, โลหะ
c) โมเลกุล, โลหะ, ไอออนิก
d) อิออน, โมเลกุล, โลหะ
ความละเอียด
ทางเลือก C
สาร X เป็นโมเลกุลในฐานะพันธะโมเลกุลที่เรียกว่าโควาเลนต์ มีจุดเดือดต่ำเนื่องจากความแตกต่างของอิเล็กโตรเนกาติวีตี้ระหว่างลิแกนด์ไม่ได้ สูงมาก. โดยทั่วไปแล้ว สารประกอบโควาเลนต์ไม่มีค่าการนำไฟฟ้า และความสามารถในการละลายเป็นตัวแปร
เราสามารถรับรู้สาร Y เป็นโลหะ เนื่องจากโลหะมีจุดหลอมเหลวสูง เป็นตัวนำไฟฟ้าที่ดีเยี่ยม และไม่ละลายในน้ำ
สุดท้าย สาร Z เป็นไอออนิก เนื่องจากสารนี้จะมีจุดหลอมเหลวค่อนข้างสูง ซึ่งเป็นผลมาจากการจัดเรียงตัวของผลึกของโมเลกุล เมื่อสารไอออนิกละลายในน้ำหรือในสถานะของเหลว สารจะมีไอออนอิสระ ซึ่งทำให้เป็นสื่อกระแสไฟฟ้าของอิเล็กตรอนและละลายได้ในน้ำ
โดย Laysa Bernardes Marques
ครูสอนเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/ligacoes-quimicas.htm