การเปลี่ยนแปลงไอโซบาริกเกิดขึ้นเมื่อก๊าซอยู่ที่ความดันคงที่ ตัวอย่างเช่น หากทำในสภาพแวดล้อมเปิด การเปลี่ยนแปลงจะเป็นไอโซบาริกเนื่องจากความดันจะเป็นความดันบรรยากาศที่จะไม่เปลี่ยนแปลง
ในกรณีนี้ อุณหภูมิและปริมาตรจะแตกต่างกันไป นักวิทยาศาสตร์ชั้นนำสองคนได้ศึกษาว่าการเปลี่ยนแปลงในการเปลี่ยนแปลงไอโซบาริกนี้เกิดขึ้นได้อย่างไร คนแรกที่เกี่ยวข้องกับปริมาตรและอุณหภูมิของก๊าซคือ Jacques Charles (1746-1823) ในปี 1787 จากนั้นในปี 1802 Joseph Gay-Lussac (1778-1850) ได้ประเมินความสัมพันธ์นี้
ดังนั้น กฎหมายจึงเกิดขึ้นที่อธิบายการเปลี่ยนแปลงไอโซบาริกของก๊าซ ซึ่งกลายเป็นที่รู้จักในชื่อกฎชาร์ลส์/เกย์-ลูสแซก ระบุไว้ดังนี้:
"ในระบบแรงดันคงที่ ปริมาตรของมวลคงที่ของก๊าซจะเป็นสัดส่วนโดยตรงกับอุณหภูมิ"

ซึ่งหมายความว่าถ้าเราเพิ่มอุณหภูมิเป็นสองเท่า ปริมาตรของก๊าซก็จะเพิ่มขึ้นเป็นสองเท่าด้วย ในทางกลับกัน หากเราลดอุณหภูมิ ปริมาตรของแก๊สก็จะลดลงในสัดส่วนเดียวกันด้วย
สามารถเห็นได้ในการทดลองง่ายๆ ถ้าเราวางบอลลูนไว้ที่คอขวด มวลอากาศคงที่ก็จะติดอยู่ ถ้าเราจุ่มขวดนี้ลงในชามที่ใส่น้ำแข็ง บอลลูนจะปล่อยลมออก ทีนี้ถ้าเราใส่ลงในชามน้ำร้อน ลูกโป่งก็จะเต็ม
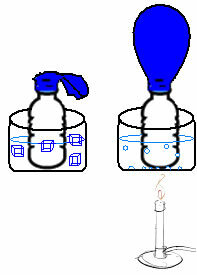
เนื่องจากเมื่ออุณหภูมิเพิ่มขึ้น พลังงานจลน์ของโมเลกุลแก๊สจะเพิ่มขึ้นและความเร็วของการเคลื่อนที่ก็เพิ่มขึ้นด้วย ดังนั้น ก๊าซจะขยายตัว เพิ่มปริมาตรที่มันครอบครอง และบอลลูนจะพองตัว ตรงกันข้ามเกิดขึ้นเมื่อเราลดอุณหภูมิโดยใส่ในน้ำเย็น
ความสัมพันธ์ระหว่างอุณหภูมิและปริมาตรในการแปลงแบบไอโซบาริกนี้กำหนดโดยความสัมพันธ์ต่อไปนี้:
วี = k
ตู่
"k" เป็นค่าคงที่ ดังแสดงในกราฟต่อไปนี้:
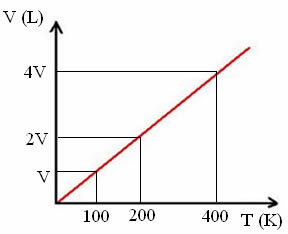
โปรดทราบว่าอัตราส่วน V/T จะให้ค่าคงที่เสมอ:
_V_ =_2V_ = _4V_
100 200 400
ดังนั้น เราสามารถสร้างความสัมพันธ์ต่อไปนี้สำหรับการแปลงไอโซบาริก:
วีเริ่มต้น = วีสุดท้าย
ตู่เริ่มต้น ตู่สุดท้าย
ซึ่งหมายความว่าเมื่อมีการเปลี่ยนแปลงอุณหภูมิของก๊าซที่ความดันคงที่ เราสามารถหาปริมาตรของก๊าซผ่านนิพจน์ทางคณิตศาสตร์นี้ได้ สิ่งที่ตรงกันข้ามก็เป็นจริงเช่นกัน เมื่อทราบปริมาตรของก๊าซ เราจะพบว่าอุณหภูมินั้นอยู่ที่เท่าใด ดูตัวอย่าง:
"มวลก๊าซมีปริมาตร 800 ซม.3 ที่อุณหภูมิ -23°C ที่ความดันที่กำหนด อุณหภูมิที่บันทึกไว้เมื่อมวลก๊าซที่ความดันเท่ากันมีปริมาตร 1.6 ลิตร”
ความละเอียด:
ข้อมูล:
วีเริ่มต้น = 800 ซม.3
ตู่เริ่มต้น = -23 ºC เพิ่มเป็น 273 เรามี 250 K (เคลวิน)
วีสุดท้าย = 1.6 ลิตร
ตู่สุดท้าย = ?
* ขั้นแรกเราต้องปล่อยระดับเสียงไว้ที่หน่วยเดียวกันก่อน เป็นที่ทราบกันดีอยู่แล้วว่า 1 dm3 เท่ากับ 1 ลิตร เหมือน 1 dm3 เท่ากับ 1000 cm3, ปรากฏว่า 1 ลิตร = 1 000 cm3:
1 ลิตร 1,000 ซม.3
x 800 ซม.3
x = 0.8 ลิตร
* ตอนนี้เราแทนที่ค่าสูตรและค้นหาค่าอุณหภูมิสุดท้าย:
วีเริ่มต้น = วีสุดท้าย
ตู่เริ่มต้น ตู่สุดท้าย
0,8_ = 1,6
250 ตันสุดท้าย
0.8 ตันสุดท้าย = 250. 1,6
ตู่สุดท้าย = 400
0,8
ตู่สุดท้าย = 500K
* ย้ายไปที่ระดับเซลเซียสเรามี:
T (K) = T (°C) + 273
500 = ที (°ซ) + 273
ที (°ซ) = 500 - 273
T (°C) = 227°C
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/transformacao-isobarica.htm
