ปฏิกิริยาซัลโฟเนชันในอัลเคน พวกเขาเป็น ปฏิกิริยาการทดแทนสารอินทรีย์, ดำเนินการโดยมีจุดมุ่งหมายในการผลิต กรดซัลโฟนิก (สารประกอบอินทรีย์ที่มีหมู่ SO3H ติดอยู่กับอะตอมของคาร์บอนหรือกับโซ่คาร์บอน) และน้ำ (H2อ.)
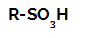
สูตรโครงสร้างของกรดซัลโฟนิก
สำหรับการทำปฏิกิริยาซัลโฟเนชั่นบน แอลเคนเราต้องผสมอัลเคน (สารประกอบที่เกิดจากโซ่คาร์บอนอิ่มตัวด้วยอะตอมของคาร์บอนและไฮโดรเจนเท่านั้น) และ กรดซัลฟูริก (ฮ2เท่านั้น4) เข้มข้นภายใต้ความร้อน (∆).
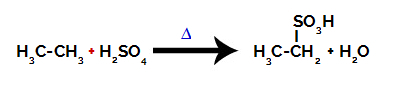
สมการเคมีแทนซัลโฟเนชันของอัลเคนสองคาร์บอน
หลักการของปฏิกิริยาซัลโฟเนชันในอัลเคน
เช่น ปฏิกิริยาอัลเคนซัลโฟเนชัน มันเป็นปฏิกิริยาการแทนที่ เรามีการแลกเปลี่ยนระหว่างส่วนประกอบที่เล็กกว่า อิเล็กโตรเนกาติวีตี้ ของสารตั้งต้น นั่นคือ ระหว่างอัลเคนและกรดซัลฟิวริก อัลเคนมีไฮโดรเจน และกรดซัลฟิวริก เป็นกลุ่มซัลโฟนิก
ด้านล่างนี้ เรามีกลไกของ a. ทีละขั้นตอน ปฏิกิริยาซัลโฟเนชันในอัลเคน. ตัวอย่างเช่น เราจะใช้อัลเคนที่ง่ายที่สุด มีเทน (CH4):
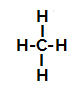
สูตรโครงสร้างของมีเทน
ขั้นตอนที่ 1: การหยุดชะงักของพันธะระหว่างไฮดรอกซิล (OH) และกำมะถัน (S) ในกรดซัลฟิวริก
กลุ่มไฮดรอกซิลแต่ละกลุ่มที่มีอยู่ในกรดซัลฟิวริกมีลักษณะเฉพาะโดยมีค่าอิเล็กโตรเนกาทีฟมากกว่า ด้วยความร้อนระหว่างปฏิกิริยา มีแนวโน้มว่าพันธะระหว่างหมู่ไฮดรอกซิลกับกำมะถันจะแตกออก:
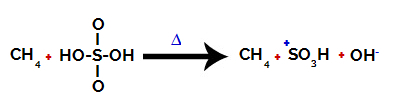
การหยุดชะงักของพันธะระหว่างกำมะถันและไฮดรอกซิล
อย่างไรก็ตาม การแตกพันธะของไฮดรอกซิลทั้งหมดไม่ได้เกิดขึ้นเนื่องจากการจัดเรียงใหม่ทางอิเล็กทรอนิกส์ในโครงสร้าง จากนั้นจึงได้ไอออนไฮดรอกไซด์ (OH)-) และไอออนซัลโฟนิก
ขั้นตอนที่ 2: กลุ่มไฮดรอกซิลโจมตีโมเลกุลอัลเคน
จากนั้นกลุ่มไฮดรอกซี (OH-) ทำการโจมตีอัลเคน ทำให้พันธะระหว่างคาร์บอนและไฮโดรเจน (ซึ่งมีความเปราะบางมากขึ้นเนื่องจากความแตกต่างของอิเล็กโตรเนกาติวีตี้ระหว่างพวกมัน) แตกออก
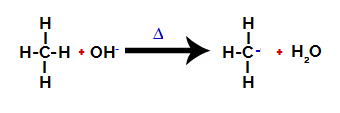
การทำลายพันธะระหว่างคาร์บอนและไฮโดรเจนในด่าง
บันทึก: การหยุดชะงักของพันธะระหว่างคาร์บอนและไฮโดรเจนมักเกิดขึ้นบ่อยที่สุดกับคาร์บอนที่มีความหนาแน่นหรือประจุไฟฟ้าต่ำกว่า คาร์บอนไฮโดรเจนที่น้อยกว่าหรือกลุ่มที่ติดอยู่กับคาร์บอนนั้นความหนาแน่นของอิเล็กตรอนก็จะยิ่งต่ำลง ดังนั้นเราจึงมี:
คาร์บอนตติยภูมิ < คาร์บอนทุติยภูมิ < คาร์บอนปฐมภูมิ
หลังจากพันธะขาด แอลเคนจะกลายเป็นคาร์บอนที่ขาดอิเล็กตรอน (คาร์โบเคชั่น) กลุ่มไฮดรอกไซด์ (OH)-) ทำปฏิกิริยากับไฮโดรเจนที่ปล่อยออกมาและก่อตัวเป็นโมเลกุลของน้ำ
ขั้นตอนที่ 3: การโจมตีของอนุมูลอิสระที่เกิดขึ้นบนกลุ่มซัลโฟนิก
ในที่สุด กลุ่มซัลโฟนิกก็ถูกอัลเคนที่เหลือโจมตี ทำให้เกิดกรดซัลโฟนิก
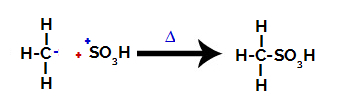
โครงสร้างที่โต้ตอบและก่อตัวเป็นกรดซัลโฟนิก
ตัวอย่างสมการแทนปฏิกิริยาซัลโฟเนชันในแอลเคน
ตัวอย่างที่ 1: ซัลโฟเนชั่นของโพรเพน
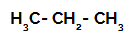
สูตรโครงสร้างของโพรเพน
โพรเพนมีคาร์บอนปฐมภูมิสองชนิดและคาร์บอนทุติยภูมิหนึ่งคาร์บอนซึ่งมีประจุต่างกันเพราะถูกพันธะกับไฮโดรเจนในปริมาณต่างกัน เนื่องจากคาร์บอนมีอิเลคโตรเนกาติตีมากกว่าไฮโดรเจน คาร์บอนเหล่านี้จึงมีความหนาแน่นของอิเล็กตรอนต่างกัน
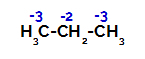
การกระจายประจุในแต่ละอะตอมของคาร์บอนของโพรเพน
สำหรับคาร์บอนปฐมภูมิ ประจุคือ -3 (เพราะถูกพันธะกับไฮโดรเจนสามตัว) และสำหรับคาร์บอนทุติยภูมิ ประจุคือ -2 (เพราะถูกพันธะกับไฮโดรเจนสองตัว) ดังนั้นจะเกิดการแตกหักในพันธะระหว่างคาร์บอนกับไฮโดรเจน บางครั้งที่คาร์บอน 1 (ของโมเลกุลหนึ่ง) บางครั้งที่คาร์บอน 2 (ของอีกโมเลกุลหนึ่ง)
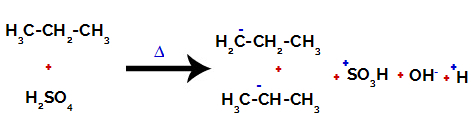
การทำลายพันธะระหว่างคาร์บอนและไฮโดรเจนกับคาร์บอนที่แตกต่างกัน
หลังจากการแตกหักระหว่างพันธะทั้งในกรดซัลฟิวริกและอัลเคนจะเกิด ผลิตภัณฑ์ที่มีการแทนที่ไฮโดรเจนในคาร์บอน 1 โดยกลุ่มซัลโฟนิกและเช่นเดียวกันกับคาร์บอน 2.
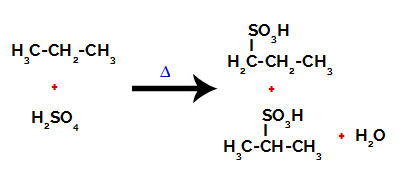
ผลิตภัณฑ์ที่เกิดจากซัลโฟเนชั่นของโพรเพน
ตัวอย่างที่ 2: ซัลโฟเนชันของ 2-เมทิล-บิวเทน

สูตรโครงสร้างของ 2-เมทิล-บิวเทน
2-เมทิล-บิวเทนมีคาร์บอนหลักสามชนิด คาร์บอนทุติยภูมิและคาร์บอนตติยรีซึ่งมี which ประจุต่างกันและความหนาแน่นทางอิเล็กทรอนิกส์ต่างกัน ดังที่เห็นได้ในโครงสร้างต่อไปนี้
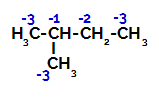
การกระจายประจุไฟฟ้าใน 2-เมทิล-บิวเทน
ดังนั้นจึงมีความเป็นไปได้หลายประการในการทำลายพันธะระหว่างคาร์บอนและไฮโดรเจนใน 2-เมทิล-บิวเทน ซึ่งสามารถเกิดขึ้นได้กับคาร์บอน 1 (ของโมเลกุล), คาร์บอน 2 (ของโมเลกุลอื่น), คาร์บอน 3 หรือคาร์บอน 4. อย่างไรก็ตาม เป็นที่น่าสังเกตว่าการหยุดชะงักของคาร์บอนหมายเลข 2 เป็นเรื่องปกติมากกว่า
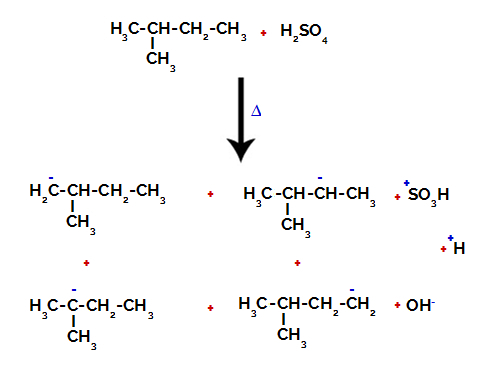
การทำลายพันธะระหว่างคาร์บอนและไฮโดรเจนกับคาร์บอนที่แตกต่างกัน
หลังจากการแตกตัวระหว่างพันธะทั้งในกรดซัลฟิวริกและอัลเคน การก่อตัวของ ผลิตภัณฑ์ที่มีการแทนที่ไฮโดรเจนบนคาร์บอน 1 โดยกลุ่มซัลโฟนิก และสิ่งเดียวกันนี้เกิดขึ้นบน คาร์บอน 2

ผลิตภัณฑ์ที่เกิดจากซัลโฟเนชันของ 2-เมทิล-บิวเทน
By Me. Diogo Lopes Dias
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm
