เมื่อวงแหวนเบนซินมีหมู่แทนที่อยู่แล้ว รากศัพท์นี้จะส่งผลต่อการแทนที่ H อื่นๆ ทั้งหมดบนวงแหวน สารทดแทนนี้สามารถเป็นออร์โธและพาราไดเร็กเตอร์หรือเมตาไดเร็กทอรี แต่คำถามก็เกิดขึ้น:
| อะไรทำให้กลุ่มที่ติดอยู่กับวงแหวนเบนซินมีอิทธิพลต่อทิศทางและการเกิดปฏิกิริยาของปฏิกิริยาการแทนที่? |
| อะไรทำให้บางกลุ่มที่ปรึกษาเป้าหมาย (ปิดการใช้งาน) และอื่น ๆ ortho-para (เปิดใช้งาน)? |
คำถามสองข้อนี้ตอบได้โดยเข้าใจการเรียก เอฟเฟกต์อิเล็กทรอนิกส์ ที่กลุ่มเหล่านี้ออกกำลังกายในสังเวียน ผลกระทบนี้เกิดขึ้นเนื่องจาก ความต่างศักย์ไฟฟ้า ระหว่างองค์ประกอบตามที่ตัวแทนจะ โพลาไรซ์พันธะของนิวเคลียสอะโรมาติก สลับกันกระตุ้นคุณลักษณะเชิงบวกของคาร์บอนในวงแหวนบางส่วน ในขณะที่บางชนิดยังคงมีลักษณะเชิงลบ
| การแทนที่ใหม่จะเกิดขึ้นในอะตอมของคาร์บอนที่มีลักษณะเฉพาะ เชิงลบ. |
เรามาดูกันว่าเอฟเฟกต์อิเล็กทรอนิกส์เหล่านี้เกิดขึ้นได้อย่างไรในวงแหวนอะโรมาติก โดยคำนึงถึงลำดับอิเล็กโตรเนกาติวีตี้ขององค์ประกอบ: F > O > N > Cl > Br > S > C > I > H
กรณีแรก: Radical activating หรือ ortho-to-director:
ตัวอย่างเช่น ในกรณีที่อยู่ต่ำกว่าโมเลกุลเบนซอล (ฟีนอล) ออกซิเจนเป็นองค์ประกอบที่มีอิเล็กโตรเนกาติฟมากที่สุด ดังนั้น มันดึงดูดอิเล็กตรอนเข้ามาเอง ทำให้คาร์บอนมีประจุบวกบางส่วน ซึ่งทำให้เกิด
โพลาไรซ์วงแหวนสลับ. ตำแหน่งที่เป็นค่าลบคือตำแหน่งออร์โธและตำแหน่งพารา นั่นคือเหตุผลที่ กลุ่ม -OH คือ activating radical หรือ ortho-to-directors. ดังจะเห็นได้จากปฏิกิริยาฟีนอลไนเตรตด้านล่าง ทำให้เกิดโอไนโตรฟีนอลและพี-ไนโตรฟีนอลเป็นผลิตภัณฑ์: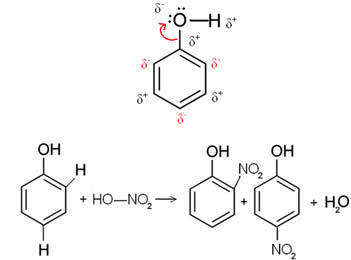
กรณีที่สอง: ปิดการใช้งานหัวรุนแรงหรือ meta-leader:
พิจารณากรณีของไนโตรเบนซีน:
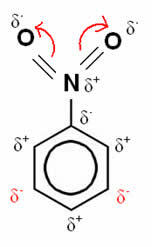
ในตัวอย่างนี้ ออกซิเจนยังคงเป็นองค์ประกอบที่มีอิเล็กโตรเนกาทีฟมากที่สุด ดังนั้นมันจึงดึงดูดพันธะที่สร้างด้วยไนโตรเจนมาสู่ตัวมันเอง ซึ่งมีประจุบวกบางส่วน ทำให้อะตอมของคาร์บอนที่ติดอยู่กับอะตอมกลายเป็นขั้วลบและดังนั้น ตามลำดับ ดังนั้นตำแหน่งที่กลายเป็นลบและอ่อนไหวต่อการเปลี่ยนตัวมากที่สุดคือตำแหน่ง เป้าหมาย, เป็น, ดังนั้น, เป็ ปิดการใช้งาน.
ดูรายละเอียดเพิ่มเติมเกี่ยวกับเอฟเฟกต์อิเล็กทรอนิกส์นี้ซึ่งเรียกว่า เอฟเฟกต์จังหวะ.
| เอฟเฟกต์จังหวะ มันคือแรงดึงดูดหรือแรงผลักของอิเล็กตรอนบนพันธะ π (pi) ของพันธะคู่หรือสามพันธะ เมื่อพวกมันสะท้อนกับวงแหวนเบนซีนเอง |
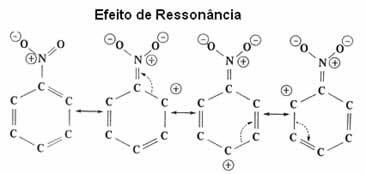
อย่างที่เห็น กลุ่ม NO2 กำลังปิดการทำงานของวงแหวน เนื่องจากกำลังดึงอิเล็กตรอนจากวงแหวนนี้ และทำให้ความหนาแน่นของอิเล็กตรอนลดลง ดังนั้นกลุ่มที่จะโจมตีและทำการเปลี่ยนตัว (electrophile) จึงเป็นบวก ดังนั้นจะโจมตีตำแหน่ง meta ที่มีประจุลบเป็นพิเศษ
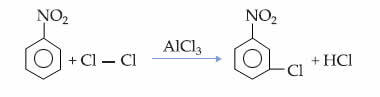
ข้อเท็จจริงนี้สามารถเห็นได้ในปฏิกิริยาโมโนคลอรีนของไนโตรเบนซีนซึ่งการแทนที่เกิดขึ้นเฉพาะในตำแหน่งเมตา:
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ทีมโรงเรียนบราซิล
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm
