โดยปกติปฏิกิริยาของ อิเล็กโทรลิซิสในน้ำ และ อิเล็กโทรไลต์อัคนี พวกมันทำด้วยอิเล็กโทรดกราไฟต์และแพลตตินัมซึ่งไม่มีส่วนร่วมในปฏิกิริยา พวกเขานำกระแสไฟฟ้าเท่านั้น อย่างไรก็ตาม มีบางกรณีที่จำเป็นต้องใช้ อิเล็กโทรดที่ใช้งานอยู่นั่นคือที่ผ่านการรีดักชันและออกซิเดชัน
กรณีการใช้งานหลักของอิเล็กโทรดเหล่านี้ที่มีส่วนร่วมในกระบวนการรีดอกซ์คือ: a การทำให้บริสุทธิ์ด้วยโลหะด้วยไฟฟ้าเช่น สังกะสี โคบอลต์ นิกเกิล และทองแดงโดยเฉพาะ และยัง การชุบด้วยไฟฟ้า. มาดูกันว่าแต่ละกรณีเกิดขึ้นได้อย่างไร:
• การทำให้บริสุทธิ์ด้วยไฟฟ้าทองแดง: การกลั่นทองแดงด้วยไฟฟ้านี้สามารถผลิตความบริสุทธิ์ได้ประมาณ 99.9% และส่วนใหญ่ใช้ในการผลิต ลวดทองแดง ซึ่งถ้ามีสิ่งเจือปนน้อยที่สุด อาจมีความสามารถในการนำกระแสไฟฟ้าได้มาก ลดลง
สังเกตว่ากระบวนการนี้เกิดขึ้นได้อย่างไร โดยดูแผนผังของถังอิเล็กโทรไลต์ที่ประกอบอยู่ด้านล่าง:

ความแตกต่างที่อาจเกิดขึ้นกับสารละลายที่เป็นน้ำของคอปเปอร์ซัลเฟต (CuSo4(aq)) – ซึ่งนำไฟฟ้า – เพื่อให้แอโนดซึ่งเป็นทองแดงที่เป็นโลหะที่ไม่บริสุทธิ์สูญเสียอิเล็กตรอน กล่าวคือ ผ่านออกซิเดชันและปล่อยประจุบวกออกมา (Cu2+) ซึ่งวางอยู่บนแผ่นลบ นี่อาจเป็นแผ่นแพลตตินั่มเฉื่อย หรือดีกว่า แผ่นทองแดงบริสุทธิ์ มันประกอบด้วยแคโทดซึ่งลดลงเมื่อทองแดงสะสมอยู่ในนั้น ดังนั้นกึ่งปฏิกิริยาที่เกิดขึ้นในอิเล็กโทรดคือ:
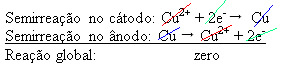
ความจริงที่ว่ามันให้ผลลัพธ์เป็นศูนย์บ่งชี้ว่าไม่มีปฏิกิริยาทางเคมี แต่มีเพียงการขนส่งทองแดงเท่านั้น ที่ด้านล่างของภาชนะมีสารที่ไม่บริสุทธิ์อื่นๆ ที่อยู่ในทองแดง เช่น ทอง เงิน ซิลิกา (ทราย) และแร่ธาตุอื่นๆ ซึ่งสามารถขายได้ด้วยซ้ำ
• การชุบด้วยไฟฟ้า: การเคลือบโลหะใช้กับวัสดุที่จะป้องกันการกัดกร่อน
โลหะที่เลือกใช้สำหรับเคลือบ - ซึ่งสามารถเป็นโครเมียม (ชุบโครเมียม), นิกเกิล (ชุบนิกเกิล), เงิน (ชุบเงิน), ทอง (ปิดทอง) หรือสังกะสี (สังกะสี) - จะเป็นขั้วบวกขั้วบวกซึ่งผ่านการเกิดออกซิเดชันทำให้สูญเสียอิเล็กตรอน มันผ่านการเกิดออกซิเดชันแทนวัสดุที่ได้รับการปกป้อง เนื่องจากมีศักยภาพในการลดลงมากกว่า
อิเล็กโทรดลบ กล่าวคือ แคโทดซึ่งรับอิเล็กตรอนเหล่านี้และผ่านการรีดิวซ์เป็นวัสดุที่เคลือบด้วยตัวเอง ด้วยวิธีนี้ มันยังคงได้รับการปกป้องแม้ว่าพื้นผิวของมันถูกละเมิดอย่างใด
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm
