ไอออไนซ์ เป็นปรากฏการณ์ทางเคมีที่สารที่เป็นกรด (ซึ่งมีสูตรทั่วไปคือ HX) เมื่อละลายในน้ำจะทำให้เกิดไอออน 2 ตัว คือ ไฮโดรเนียม ไอออน (H3โอ+ หรือ H+) และประจุลบใดๆ (X-). ปรากฏการณ์นี้แสดงจากสมการ ดู:
HX + H2O → H3โอ+ + X-
ในระหว่างการแตกตัวเป็นไอออน จะมีเฉพาะไฮโดรเจนที่แตกตัวเป็นไอออนจาก กรด พวกมันจะถูกเปลี่ยนเป็นไอออนบวกของไฮโดรเนียมซึ่งเป็นปัจจัยที่ขึ้นอยู่กับความจุไอออไนเซชันของกรดนี้ซึ่งก็คือระดับของการแตกตัวเป็นไอออน (α) ดังนั้น ไม่ใช่ไฮโดรเจนทั้งหมดที่จะเกิดเป็นไฮโดรเนียม เว้นแต่กรดจะมีระดับของการแตกตัวเป็นไอออนเท่ากับ 100%
อย่างไรก็ตามเมื่อเราเป็น การสร้างสมการไอออไนซ์ เราไม่ได้คำนึงถึงระดับของการแตกตัวเป็นไอออนของกรด แต่ปริมาณของ ไฮโดรเจนที่แตกตัวเป็นไอออนได้ ที่เขานำเสนอ
ตามกฎทั่วไป เราถือว่าไฮโดรเจนที่แตกตัวเป็นไอออนได้นั้นเป็นไฮโดรเจนทั้งหมดที่มีอยู่ในไฮดราซิด ในกรณีของออกซีแอซิด เฉพาะไฮโดรเจนที่ถูกพันธะกับอะตอมของคาร์บอนเท่านั้นที่สามารถแตกตัวเป็นไอออนได้ ดังที่เห็นได้ในสูตรโครงสร้างที่แสดงด้านล่าง:
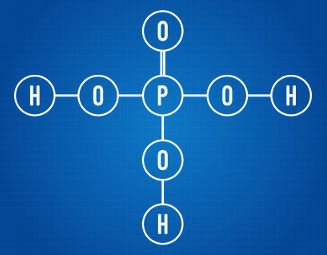
กรดฟอสฟอริกมีไฮโดรเจนที่แตกตัวเป็นไอออนได้สามตัว
จากการวิเคราะห์สูตรโครงสร้างด้านบน เราจะเห็นได้ว่ากรดที่เป็นปัญหานั้นมีไฮโดรเจนสามอะตอมที่ถูกผูกมัดกับอะตอมออกซิเจน จึงมีไฮโดรเจนที่แตกตัวเป็นไอออนได้ทั้งหมดสามชนิด
ดูตัวอย่างการประกอบ ของสมการไอออไนเซชันของกรดบางชนิด:
ตัวอย่างที่ 1: กรดไฮโดรโบรมิก (HBr)
HBr + H2O → H3โอ+ + บรา-
กรดไฮโดรโบรมิกเป็นไฮดราซิดที่มีไฮโดรเจนเพียงตัวเดียวในองค์ประกอบ เนื่องจากไฮโดรเจนทั้งหมดในไฮดราซิดสามารถแตกตัวเป็นไอออนได้ จึงก่อตัวเมื่อละลายในน้ำเท่านั้น ไฮโดรเนียมไอออนบวกหนึ่งโมล มันเป็น โบรไมด์แอนไอออน (Br-).
ตัวอย่างที่ 2: ไฮโดรเจนซัลไฟด์ (H2ส)
โฮ2Y+ 2 โฮ2O → 2 โฮ+ + ส-2
ไฮโดรเจนซัลไฟด์เป็นไฮดราซิดที่มีไฮโดรเจนสองชนิดอยู่ในองค์ประกอบ เนื่องจากไฮโดรเจนทั้งหมดในไฮดราซิดสามารถแตกตัวเป็นไอออนได้ จึงก่อตัวเมื่อละลายในน้ำ ไฮโดรเนียมไอออนบวกสองโมล มันเป็น ไอออนซัลไฟด์ (S-2). สำหรับสิ่งนี้เราใช้ we น้ำสองโมล
ตัวอย่างที่ 3: กรดแมงกานิก (H2MnO4)
โฮ2MnO4 + 2 โฮ2O → 2 โฮ3โอ+ + MnO4-2
กรดแมงกานิกเป็นออกซีกรดที่มีไฮโดรเจนสองชนิดอยู่ในองค์ประกอบ เช่นเดียวกับใน oxyacids เฉพาะไฮโดรเจนที่ยึดติดกับออกซิเจนเท่านั้นที่สามารถแตกตัวเป็นไอออนได้ - ในกรณีของกรดแมงกานิก ไฮโดรเจนทั้งสองจะก่อตัวขึ้นเมื่อละลายในน้ำ ไฮโดรเนียมไอออนบวกสองโมล มันเป็น แมงกาเนตแอนไอออน (MnO4-2). สำหรับสิ่งนี้เราใช้ we น้ำสองโมล
ตัวอย่างที่ 4: กรดฟอสฟอรัส (H3ฝุ่น3)
โฮ3ฝุ่น3 + 2 โฮ2O → 2 โฮ3โอ+ + HPO3-2
กรดฟอสฟอรัสเป็นออกซีกรดที่มีไฮโดรเจนสามชนิดอยู่ในองค์ประกอบ เช่นเดียวกับใน oxyacids เฉพาะไฮโดรเจนที่ยึดติดกับออกซิเจนเท่านั้นที่สามารถแตกตัวเป็นไอออนได้ - ในกรณีของกรดฟอสฟอรัส ไฮโดรเจนทั้งสองจะก่อตัวขึ้นเมื่อละลายในน้ำ ไฮโดรเนียมไอออนบวกสองโมล มันเป็น ฟอสไฟต์แอนไอออน (HPO3-2). สำหรับสิ่งนี้เราใช้ we น้ำสองโมล
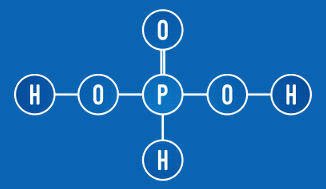
กรดฟอสฟอรัสมีไฮโดรเจนสองชนิดที่แตกตัวเป็นไอออนได้ (กลุ่ม OH)
ตัวอย่างที่ 5: กรดบอริก (H3BO3)
โฮ3BO3 + 3 โฮ2O → 3 โฮ+ + โบ3-3
กรดบอริกเป็นออกซีกรดที่มีไฮโดรเจนสามตัวอยู่ในองค์ประกอบ เช่นเดียวกับใน oxyacids เฉพาะไฮโดรเจนที่ยึดติดกับออกซิเจนเท่านั้นที่สามารถแตกตัวเป็นไอออนได้ - ในกรณีของกรดบอริก ไฮโดรเจนสามชนิดคือ - มันจะก่อตัวขึ้นเมื่อละลายในน้ำ ไฮโดรเนียมไอออนบวกสามโมล มันเป็น แอนไอออนบอเรต (BO3-3). สำหรับสิ่งนี้เราใช้ we น้ำสามโมล
ตัวอย่างที่ 6: กรดไพโรฟอสฟอริก (H4พี2โอ7)
โฮ4พี2โอ7 + 4 โฮ2O → 4 โฮ3โอ+ + พี่2โอ7-4
กรดไพโรฟอสฟอริกเป็นออกซีกรดที่มีไฮโดรเจนสี่ตัวอยู่ในองค์ประกอบ เช่นเดียวกับใน oxyacids เฉพาะไฮโดรเจนที่ถูกพันธะกับออกซิเจนเท่านั้นที่สามารถแตกตัวเป็นไอออนได้ - ในกรณีของกรดบอริก ไฮโดรเจนสี่ตัวคือ - มันจะก่อตัวขึ้นเมื่อละลายในน้ำ ไฮโดรเนียมไอออนบวกสี่โมล มันเป็น ประจุลบไพโรฟอสเฟต (P2โอ7-4). สำหรับสิ่งนี้เราใช้ we น้ำสี่โมล
By Me. ดิโอโก้ โลเปส ดิอาส
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/equacoes-ionizacao-dos-acidos.htm
