เธ ออกซิเดชันเล็กน้อย mild ในแอลคีน เป็นปฏิกิริยาอินทรีย์ที่กระทำเมื่อให้ แอลคีน วางในสื่อที่เกิดจากเบสที่มีน้ำและเกลือโปแตสเซียมเปอร์แมงกาเนต (KMnO4) เกลือที่เรียกกันทั่วไปว่า น้ำยาไบเออร์.
ผลิตภัณฑ์ที่เกิดขึ้นเรียกว่า แอลกอฮอล์ vicinal นั่นคือ แอลกอฮอล์ที่มีสองกลุ่มไฮดรอกซิล (OH-) วางบนคาร์บอนใกล้เคียง ดังในสูตรทั่วไปต่อไปนี้:
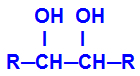
บันทึก: R สามารถเป็นอะตอมของอนุมูลหรือไฮโดรเจนได้
น้ำยาไบเออร์
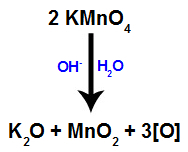
เมื่อ น้ำยาของไบเออร์ (KMnO4) ผสมกับน้ำต่อหน้าเบสอนินทรีย์ (OH-) ทำปฏิกิริยาและสร้างโพแทสเซียมออกไซด์ (K2O), แมงกานีสไดออกไซด์ (MnO2) และออกซิเจนตั้งไข่ (ออกซิเจนอิสระ แสดงโดย [O]) ดูสมการสมดุลของกระบวนการ

ออกซิเจนที่เกิดขึ้นใหม่เหล่านี้เกิดจากรีเอเจนต์ของไบเออร์มีหน้าที่ในการเกิดปฏิกิริยาออกซิเดชันเล็กน้อยในแอลคีน (ดังที่เราจะเห็นในรายการต่อไปนี้)
กลไกในปฏิกิริยาออกซิเดชันเล็กน้อยในแอลคีน
กลไกที่ 1: การก่อตัวของออกซิเจนตั้งไข่จากน้ำยาของไบเออร์
กลไกที่ 2: การโจมตีของออกซิเจนตั้งไข่กับพันธะคู่ที่มีอยู่ในอัลคีนทำให้เกิดการหยุดชะงักของ พันธะ pi และการเกิดเวเลนซ์อิสระในแต่ละคาร์บอนที่เกี่ยวข้องกับ ลิงค์ปี่
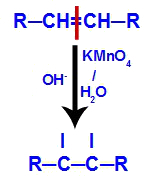
กลไกที่ 3:
ออกซิเจนที่พึ่งเกิดจะรวมตัวกับไฮโดรเนียม (H+) เกิดขึ้นจากการแตกตัวเป็นไอออนในน้ำทำให้เกิดหมู่ไฮดรอกซิล (OH-).
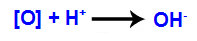
กลไกที่ 4: การเชื่อมต่อของไฮดรอกซิลที่เกิดขึ้นในแต่ละเวเลนซ์อิสระที่อยู่บนคาร์บอนซึ่งมีพันธะไพ ทำให้เกิดไดอัลโคฮอลในช่องปาก

ตัวอย่างปฏิกิริยาออกซิเดชันเล็กน้อยในแอลคีน
→ ปฏิกิริยาออกซิเดชันเล็กน้อยบน but-2-ene
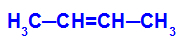
สูตรโครงสร้างของ but-2-ene
ในขั้นต้น พันธะคู่ระหว่างคาร์บอน 2 และ 3 ของอัลคีนจะถูกทำลายโดยการโจมตีของออกซิเจนตั้งไข่ ทำให้เกิดวาเลนซ์อิสระ (ร่องรอยแนวตั้ง) บนคาร์บอน 2 และ 3

ทำลายพันธะ pi ระหว่างคาร์บอน 2 และ 3 ใน but-2-ene
จากนั้นออกซิเจนตั้งไข่จะรวมตัวกับไฮโดรเนียม (H+) จากการแตกตัวเป็นไอออนของน้ำ ทำให้เกิดหมู่ไฮดรอกซิล (OH-) ซึ่งจับกับเวเลนซ์อิสระของคาร์บอน 2 และ 3 ทำให้เกิดไดอัลคอลโฮล
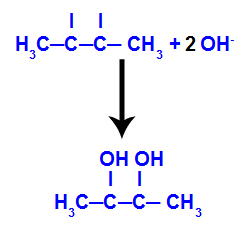
Vicinal แอลกอฮอล์ที่เกิดจาก but-2-ene
→ ปฏิกิริยาออกซิเดชันเล็กน้อยบน 2-methyl-propene
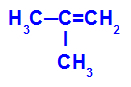
สูตรโครงสร้างของ 2-เมทิล-โพรพีน
ในขั้นต้น พันธะคู่ระหว่างคาร์บอน 1 และ 2 ของอัลคีนถูกทำลายโดยการโจมตีของออกซิเจนตั้งไข่ ทำให้เกิดวาเลนซ์อิสระ (ร่องรอยแนวตั้ง) บนคาร์บอน 1 และ 2
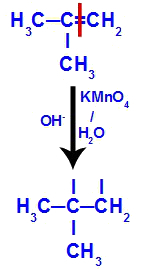
การทำลายพันธะ pi ระหว่างคาร์บอน 1 และ 2 ใน 2-methyl-propene
จากนั้นออกซิเจนตั้งไข่จะรวมตัวกับไฮโดรเนียม (H+) จากการแตกตัวเป็นไอออนของน้ำ ทำให้เกิดหมู่ไฮดรอกซิล (OH-) ซึ่งจับกับเวเลนซ์อิสระของคาร์บอน 1 และ 2 ทำให้เกิดไดอัลโคฮอลในช่องปาก
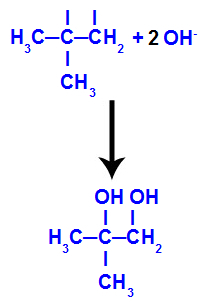
Vicinal แอลกอฮอล์ที่เกิดจาก 2-methyl-propene
By Me. Diogo Lopes Dias
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/oxidacao-branda-alcenos.htm
