สสารสามารถผ่านการเปลี่ยนแปลงได้สองประเภทหลัก คือ ทางกายภาพและทางเคมี การเปลี่ยนแปลงทางกายภาพคือเมื่อธรรมชาติของสสารไม่เปลี่ยนแปลง นั่นคือองค์ประกอบของสสาร ตัวอย่างเช่น เมื่อเราตัดไม้ชิ้นหนึ่ง มันได้รับการแปลงร่าง แต่มันเป็นปรากฏการณ์ทางกายภาพ เพราะมันยังคงเป็นไม้ โครงสร้างของมันเหมือนกับในตอนแรก
ในทางกลับกัน, การเปลี่ยนแปลงทางเคมีหรือปรากฏการณ์เกิดขึ้นเมื่อธรรมชาติหรือองค์ประกอบของสสารมีการเปลี่ยนแปลง ในกรณีนี้ อนุภาคตั้งต้น (ซึ่งอาจเป็นโมเลกุล อะตอม กลุ่มไอออนิก ไอออน ฯลฯ) จะมีลักษณะดังนี้ แยกชิ้นส่วนและอะตอมของพวกมันจัดเรียงใหม่ ประกอบโมเลกุลใหม่ กระจุก อะตอม ไอออน เป็นต้น นั่นคือ ใหม่ สาร มันคือ ปฏิกิริยาเคมี.
ตัวอย่างเช่น ลองนึกภาพว่าเรานำไม้ขีดไฟติดไฟไว้ใกล้กับเอทิลแอลกอฮอล์ เรารู้ว่าจะเกิดอะไรขึ้น: แอลกอฮอล์จะเริ่มไหม้ ซึ่งหมายความว่ากำลังทำปฏิกิริยาเคมีกับออกซิเจนในอากาศ (O2) และจะเปลี่ยนองค์ประกอบไม่ให้เป็นเอทานอลอีกต่อไป (C2โฮ6O) และออกซิเจนก็จะไม่มีองค์ประกอบเริ่มต้นอีกต่อไป ซึ่งทำให้เกิดสารใหม่ ซึ่งก็คือคาร์บอนไดออกไซด์ (CO)2) และน้ำ (H2อ.)

แอลกอฮอล์ติดไฟ - ปฏิกิริยาการเผาไหม้
ในปฏิกิริยาเคมีจะเรียกสารตั้งต้นว่า
รีเอเจนต์ และจุดสิ้นสุดของ สินค้าและปฏิกิริยาจะแสดงผ่าน สมการเคมีซึ่งเป็นไปตามโครงสร้างทั่วไปดังต่อไปนี้:รีเอเจนต์ → ผลิตภัณฑ์
เมื่อพิจารณาจากตัวอย่างก่อนหน้าของปฏิกิริยาการเผาไหม้ที่สมบูรณ์ของแอลกอฮอล์ (เอทานอล) เรามีสมการทางเคมีดังต่อไปนี้:
เอทานอล + แก๊สออกซิเจน → คาร์บอนไดออกไซด์ + น้ำ
ปฏิกิริยาเคมีนี้แสดงด้านล่างโดยใช้อะตอมตามแบบจำลองดาลตัน ในรูปของทรงกลมอย่างง่าย:
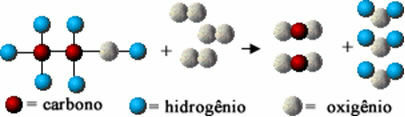
การแสดงแบบจำลองของปฏิกิริยาการเผาไหม้ของเอทานอล
สังเกตว่าพันธะเริ่มต้นระหว่างอะตอมแตกออกและก่อตัวเป็นพันธะใหม่ และสารใหม่ก็ปรากฏขึ้น
ดังนั้น สมการเคมีจึงเขียนโดยใช้สูตรและสัญลักษณ์ที่แสดงถึงรูปแบบข้างต้นได้ดีที่สุด ในกรณีที่พิจารณา (ปฏิกิริยาการเผาไหม้ของเอทานอล) เรามีสมการทางเคมีที่แสดงดังนี้:
ค2โฮ5โอ้(?) + 3 ออน2(ก.) → 2 CO2(ก.) + 3 ชั่วโมง2โอ(v)
มีปัจจัยทางสายตาบางอย่างที่บ่งชี้ว่ามีปฏิกิริยาเคมี ได้แก่
* การปล่อยก๊าซ;
* เปลี่ยนสี;
* การตกตะกอน;
* ลักษณะของเปลวไฟหรือความส่องสว่าง
กระบวนการสำคัญที่เกิดขึ้นในร่างกายของเรา ในธรรมชาติ และในอุตสาหกรรม เช่น การผลิตยาและอาหารอุตสาหกรรม เป็นปฏิกิริยาทางเคมี ดังนั้นจึงมีความสำคัญอย่างยิ่งต่อการเกิดขึ้นและการบำรุงรักษาชีวิต
ปฏิกิริยาเคมีมีหลายประเภท ซึ่งสามารถจำแนกได้ตามเกณฑ์ต่างๆ แต่ประเภทหลักที่ศึกษาในวิชาเคมี ได้แก่
1. ปฏิกิริยาอนินทรีย์: โดยปกติแล้วจะจำแนกตามจำนวนของสารที่เกิดขึ้น จำนวนรีเอเจนต์ และการมีอยู่หรือไม่มีของสารธรรมดาและสารผสม ปฏิกิริยาอนินทรีย์มีสี่ประเภทหลัก:
1.1. ปฏิกิริยาสังเคราะห์หรือเติม addition;
1.2. ปฏิกิริยาการสลายตัวหรือการวิเคราะห์;
1.3. ปฏิกิริยาการแลกเปลี่ยน การกระจัด หรือรีดอกซ์อย่างง่าย;
1.4. ปฏิกิริยาการแลกเปลี่ยนหรือเมทาธีซิสสองครั้ง;
2. ปฏิกิริยาอินทรีย์: สิ่งเหล่านี้เกี่ยวข้องกับสารประกอบคาร์บอน โดยทั่วไปจะแบ่งออกเป็นสามประเภทหลัก:
2.1. ปฏิกิริยาเพิ่มเติม;
2.2. ปฏิกิริยาทดแทน;
2.3. ปฏิกิริยาการกำจัด.
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-reacao-quimica.htm
