เธ รัทเทอร์ฟอร์เดียม เป็นธาตุสังเคราะห์ที่มีเลขอะตอม 104 อยู่ในหมู่ที่ 4 ของ ตารางธาตุโดยเป็นสมาชิกคนแรกของซีรีส์ทรานแซกทิไนด์ การตรวจจับครั้งแรกเกิดขึ้นเมื่อปีพ. ศ. 2507 ในห้องปฏิบัติการที่มีชื่อเสียงของเมือง Dubna เช่นเดียวกับทรานแซกทิไนด์อื่นๆ ชื่ออย่างเป็นทางการขององค์ประกอบ 104 เกี่ยวข้องกับความขัดแย้งระหว่างโซเวียตและอเมริกา ในส่วนสงครามเย็นในประวัติศาสตร์เคมี
รัทเทอร์ฟอร์เดียม ไม่มีการใช้งานจริงโดยที่ไอโซโทปที่เสถียรที่สุดของไอโซโทปมีประมาณสองชั่วโมงครึ่งของ ครึ่งชีวิต. อย่างไรก็ตาม การศึกษาในระบบแก๊สและสารละลายได้พิสูจน์ให้เห็นถึงความคล้ายคลึงทางเคมีกับองค์ประกอบอื่นๆ ของกลุ่มที่ 4 เช่น เซอร์โคเนียมและ แฮฟเนียม.
อ่านด้วย: Seaborgium — องค์ประกอบสังเคราะห์ที่ตั้งชื่อตามนักวิทยาศาสตร์ Glenn Seaborg
บทสรุปของรัทเทอร์ฟอร์เดียม
- เป็นองค์ประกอบทางเคมีสังเคราะห์ที่อยู่ในกลุ่มที่ 4 ของตารางธาตุ
- มันถูกสังเคราะห์ขึ้นครั้งแรกในปี 2507 ที่สถาบันร่วมเพื่อการวิจัยนิวเคลียร์ในเมือง Dubna ประเทศรัสเซีย
- มันคือ ธาตุกัมมันตรังสียาย.
- เช่นเดียวกับทรานส์แซกทิไนด์อื่นๆ รัทเทอร์ฟอร์เดียมทนทุกข์ทรมานจากความเสถียรต่ำ และเป็นการยากที่จะสังเคราะห์ตัวอย่างจำนวนมากเพื่อการศึกษา
- ชื่อนี้มีขึ้นอย่างเป็นทางการในปี 1997 หลังจากข้อพิพาทระหว่างอเมริกากับโซเวียตเป็นเวลาหลายปี
คุณสมบัติของรัทเทอร์ฟอร์เดียม
- สัญลักษณ์: Rf
- เลขอะตอม: 104
- มวลอะตอม: 267 c.u.s.
- การกำหนดค่าทางอิเล็กทรอนิกส์: [Rn] 7s2 5f14 6 วัน2
- ไอโซโทปที่เสถียรที่สุด: 267Rf (ครึ่งชีวิต 2.5 ± 1.5 ชั่วโมง)
- ชุดเคมี: กลุ่มที่ 4, ทรานแซกทิไนด์, ธาตุหนักมาก
คุณสมบัติของรัทเทอร์ฟอร์เดียม
เช่นเดียวกับทรานแซกทิไนด์ทั้งหมด เช่น องค์ประกอบหลังลอเรนซ์ (Lr), รัทเทอร์ฟอร์ดเดียม เป็นธาตุกัมมันตภาพรังสี. ไอโซโทปที่เสถียรที่สุดถูกตรวจพบในปี 2547 และครึ่งชีวิตของมัน (เวลาที่ต้องใช้สำหรับปริมาณของ ไอโซโทปรังสี ลดลงครึ่งหนึ่ง) คือสองชั่วโมงครึ่งโดยมีข้อผิดพลาดเกิดขึ้นหนึ่งชั่วโมงครึ่งไม่มากก็น้อย
ความยากลำบากอย่างมากในการสร้างคุณสมบัติทางเคมีของรัทเทอร์ฟอร์เดียมและอื่น ๆ โดยทั่วไปแล้วทรานแซกทิไนด์จะมีอัตราการผลิตต่ำไม่ว่าจะในปริมาณหรือใน ความเร็ว. ตัวอย่างเช่น ในองค์ประกอบเหล่านี้ เป็นเรื่องปกติมากที่จะประเมินทางเคมีเพียงค่าเดียว อะตอมซึ่งในทางหนึ่งต้องมีการดัดแปลงในแง่ของการคำนวณเนื่องจากสมการส่วนใหญ่ถูกสร้างขึ้นสำหรับระบบที่มีอะตอมมากกว่าหนึ่งตัว นอกจากนี้ บ่อยครั้งที่ ไอโซโทปมีครึ่งชีวิตสั้นมากซึ่งทำให้การศึกษาเชิงลึกยากขึ้นหรือเป็นไปไม่ได้
ในกรณีเฉพาะของ Rf นักวิทยาศาสตร์ได้พิสูจน์แล้วว่าพฤติกรรมของมันในสถานะของเหลวนั้นคล้ายคลึงกับขององค์ประกอบอื่นๆ ไฟแช็กกลุ่ม 4, เซอร์โคเนียมและแฮฟเนียม เช่นเดียวกับการก่อตัวของฟลูออไรด์ในสารละลายด้วยการสกัดที่ตามมาในเรซินแลกเปลี่ยนไอออน พฤติกรรมนี้ช่วยเสริมการมีอยู่ของรัทเทอร์ฟอร์เดียมในกลุ่มที่ 4 ของตารางธาตุ
อ่านด้วยนะ: ธาตุเคมีใหม่ — ธาตุทั้งสี่ที่ขาดหายไปในช่วงที่ 7
รับรัทเทอร์ฟอร์เดียม
Transactinides ต้องการโครงสร้างพื้นฐานขนาดใหญ่สำหรับการผลิต ทั้งหมด ถูกสังเคราะห์ด้วย เครื่องเร่งอนุภาคซึ่งชนิดไอออนิกชนกับธาตุหนัก การตรวจจับองค์ประกอบเหล่านี้ไม่ง่ายและตรงไปตรงมา
เมื่อก่อตัวขึ้น โดยธรรมชาติแล้ว ธาตุกัมมันตรังสีจะเริ่มสลายตัวและแสดงการปลดปล่อย เช่น อนุภาคแอลฟาและเบตา บ่อยครั้งจำเป็นต้องประเมิน การสลายตัวของสารกัมมันตรังสี ของอะตอมที่ก่อตัวขึ้นหรือแม้แต่ระบุชนิดของอะตอมที่อาจเกิดขึ้นจากปฏิกิริยานิวเคลียร์เหล่านี้ เช่นเดียวกับในปริศนา
เพิ่มสิ่งนี้ให้กับข้อเท็จจริงที่ว่าครึ่งชีวิตของไอโซโทปของทรานแซกติไนด์มักจะสั้นในช่วง วินาที ทำให้สามารถรับปริมาณในช่วงไม่กี่อะตอมหรือแม้แต่อะตอมเดียวได้ อะตอม.
ในกรณีของ Rf การสังเคราะห์ครั้งแรกที่รายงานสำหรับองค์ประกอบนี้เกี่ยวข้องกับ การชนกันของไอโซโทปพลูโทเนียม Pu กับไอออนของไอโซโทปนีออน 22,ฮะ.
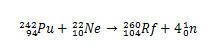
อย่างไรก็ตาม ไอโซโทปอื่นๆ ของรัทเทอร์ฟอร์เดียมสามารถผลิตได้โดยการดัดแปลงสปีชีส์ที่จะชนกัน ตัวอย่างเช่น ไอโซโทป 261 สามารถผลิตได้โดยปฏิกิริยาระหว่างออกซิเจน -18 และคูเรียม-248 ซึ่งสร้างห้านิวตรอน
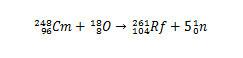
ตรวจสอบในพอดคาสต์ของเรา: เครื่องเร่งอนุภาคทำงานอย่างไร
ข้อควรระวังกับรัทเทอร์ฟอร์เดียม
เนื่องจากรัทเทอร์ฟอร์เดียมไม่สามารถผลิตได้ในปริมาณมาก ความเสี่ยงที่เกี่ยวข้องกับธาตุนี้จึงเชื่อมโยงกับ ผลกระทบของ รังสี. อย่างไรก็ตาม ในห้องปฏิบัติการควบคุม ความเสี่ยงเหล่านี้ถูกคาดการณ์ไว้และดังนั้นจึงลดน้อยลง
ประวัติของรัทเทอร์ฟอร์เดียม

ทรานแซกทิไนด์ทั้งหมดมีส่วนร่วมในการแข่งขันเพื่อการค้นพบของพวกเขาในทศวรรษ 1960 และ 1970 ตอนนี้มีรายงานว่าเป็น War of Transfers ชิ้นส่วนของ สงครามเย็น ในประวัติศาสตร์เคมี. แม้จะเรียกว่าสิ่งนั้น ซึ่งแสดงว่ามีข้อพิพาทเกิดขึ้นกับธาตุหลังเฟอร์เมียมเป็นธาตุ เลขอะตอม 100 องค์ประกอบที่เกี่ยวข้องโดยตรงคือ 104 ถึง 109 ที่เพิ่งค้นพบ ทรานแซกทิไนด์
ในกรณีของรัทเทอร์ฟอร์เดียม ข้อพิพาทเริ่มขึ้นในปี 2507เมื่อนักวิจัยโซเวียตที่สถาบันร่วมเพื่อการวิจัยนิวเคลียร์ในเมือง Dubna รัสเซียรายงานการค้นพบไอโซโทป 104 260 โดยการทิ้งระเบิดพลูโทเนียม-242 ด้วยไอออน นีออน-22. แต่นักวิจัยของ Dubna ได้นำเสนอหลักฐานเพียงชิ้นเดียว ซึ่งก็คือการตรวจหาไอโซโทป ที่เสื่อมสลายไปเองโดยมิได้ระบุมวลและเวลาของ .ให้ชัดเจน ครึ่งชีวิต. เป็นผลให้มีการดูการค้นพบด้วยความสงสัย
ห้าปีต่อมา ในปี 1969 ทีมนักวิทยาศาสตร์ชาวอเมริกันที่ห้องปฏิบัติการแห่งชาติ Lawrence Berkeley ในเมืองเบิร์กลีย์ รัฐแคลิฟอร์เนีย นำโดย Albert Ghiorso กล่าวว่าเขาได้ให้หลักฐานเพียงพอสำหรับการค้นพบไอโซโทป 104 257 โดยชนกับ californium-249 กับ คาร์บอน-12 นักวิทยาศาสตร์คนเดียวกันสามารถผลิตไอโซโทป 259 ของธาตุ 104 ได้ในเวลาต่อมา ในปีพ.ศ. 2516 นักวิทยาศาสตร์จากห้องปฏิบัติการแห่งชาติโอ๊คริดจ์ได้ยืนยัน เลขอะตอม 104 สำหรับมวล 257 ไอโซโทปที่ผลิตที่เบิร์กลีย์
ปีถัดมามีความขัดแย้งกันอย่างมากระหว่างนักวิทยาศาสตร์ของทั้งสองประเทศ จนกระทั่งในปี พ.ศ. 2528 เคมีบริสุทธิ์และเคมีประยุกต์ (IUPAC) และสหพันธ์ฟิสิกส์บริสุทธิ์และประยุกต์ระหว่างประเทศ (IUAP) แบบฟอร์ม a คณะกรรมการผสมของนักวิทยาศาสตร์เก้าคนที่เรียกว่าคณะทำงานการโอน (คณะทำงานด้านการโอนย้ายหรือ TWG) TWG ถูกสร้างขึ้นเพื่อตัดสินใจว่าใครเป็นผู้รับผิดชอบในการค้นพบองค์ประกอบตั้งแต่ 101 ถึง 112
ถึงกระนั้น การตัดสินใจของ TWG ก็ไม่ได้ไร้คำถามเสมอไป ในกรณีขององค์ประกอบ 104 คณะทำงานตัดสินใจว่า ควรมีการแบ่งเครดิตระหว่างนักวิทยาศาสตร์โซเวียตและอเมริกันซึ่งเป็นสิ่งที่นักวิทยาศาสตร์ของ Berkeley ไม่ชอบเลย
ในปี 1991 Ghiorso และ Seaborg จากทีม Berkeley อ้างว่าการระบุองค์ประกอบ 104 โดยนักวิทยาศาสตร์ Dubna คือ ผิดอย่างชัดเจนและถึงจุดหนึ่งปฏิเสธความถูกต้องของข้อสรุปของ TWG ถือว่าเป็นการก่อความเสียหายต่อชุมชน ทางวิทยาศาสตร์
ไม่น่าแปลกใจใน ในช่วงต้นทศวรรษ 1990 ชื่อขององค์ประกอบใหม่ยังไม่เป็นเอกฉันท์. จากนั้นมีการเจรจาระหว่างนักวิทยาศาสตร์ชาวเยอรมัน รัสเซีย และอเมริกัน ซึ่งพิสูจน์ให้เห็นแล้วว่าผิดหวัง ที่นั่น ในปี 1992 ห้องทดลองของเยอรมัน Gesellschaft für Schwerionenforschung (GSI) ได้เสนอชื่อสำหรับองค์ประกอบ 102 ถึง 109 โดยใส่ไมต์เนเรียมสำหรับองค์ประกอบ 104
นักวิทยาศาสตร์ที่เกี่ยวข้องก็ไม่ยอมรับรายชื่อนี้แม้จะได้รับการยกย่องก็ตาม การตัดสินใจสามารถทำได้ในปี 1994 ระหว่างการประชุม Iupac Inorganic Compound Nomenclature Commission (CNIC) ในนั้นชื่อ dubnium ได้รับเลือกสำหรับองค์ประกอบ 104 อย่างไรก็ตาม American Chemical Society นำมาใช้ในปีเดียวกันชื่อ rutherfordium สำหรับองค์ประกอบ 104 องค์ประกอบที่ 104 ในช่วงเวลาแห่งความเสื่อมเสียของชาวอเมริกัน ที่มาตั้งคำถามถึงอำนาจของ IUPAC ในการสร้างรูปแบบใหม่ ชื่อ.
เฉพาะในปี 1997ที่การประชุมใหญ่สามัญของ IUPAC ที่เจนีวาก็คือ ในที่สุดองค์ประกอบ 104 ก็เป็นทางการในฐานะรัทเทอร์ฟอร์เดียมหลังจากที่ ACS หลีกทางให้ระบบการตั้งชื่อขององค์ประกอบใกล้เคียงอื่นๆ
แบบฝึกหัดแก้บน rutherfordium
คำถามที่ 1
Rutherfordium เป็นองค์ประกอบสังเคราะห์และหนึ่งในปัญหาหลักในการศึกษาคือความจริงที่ว่าไม่สามารถสังเคราะห์จำนวนมากได้
ในบรรดาปัจจัยที่เป็นไปได้ที่นำไปสู่ความยากลำบากนี้ เราสามารถระบุได้:
(A) รัทเทอร์ฟอร์ดเดียมมีไอโซโทปครึ่งชีวิตที่ยาวนานซึ่งเรียงลำดับกันเป็นล้านปี
(B) รัทเทอร์ฟอร์เดียมสลายตัวอย่างรวดเร็วและเป็นธรรมชาติ ทำให้ไม่สามารถตรวจพบปริมาณมหภาคของมันได้
(C) ไม่มีเทคโนโลยีใดที่สามารถสังเคราะห์รัทเทอร์ฟอร์เดียมได้ ข้อมูลของพวกมันเป็นข้อมูลทางทฤษฎีที่เคร่งครัดและไม่มีพื้นฐานทางวิทยาศาสตร์
(D) กฎเคมีระบุว่าเป็นไปไม่ได้ที่จะสังเคราะห์องค์ประกอบที่มีเลขอะตอมเกินกว่าของลอเรนซ์ 103
(E) ในระหว่างการสังเคราะห์รัทเทอร์ฟอร์เดียม ธาตุที่เบากว่าของกลุ่มจะถูกจัดลำดับความสำคัญทางเคมี
ตอบกลับ: ตัวอักษร B
ธาตุทรานแซกติไนด์ เช่น Rf มีกัมมันตภาพรังสีและสลายตัวได้เองด้วยความเร็วสูง เนื่องจากครึ่งชีวิตสั้น ดังนั้น เมื่อสิ้นสุดการทดลอง อะตอมของสปีชีส์สังเคราะห์เหลืออยู่ไม่กี่อะตอม
คำถาม2
ในปี 1964 นักวิจัยจาก Dubna อ้างว่าได้สังเคราะห์ไอโซโทป-260 ของ rutherfordium (Z = 104) ในกรณีของไอโซโทปนี้ จำนวนนิวตรอนเป็นเท่าใด?
(A) 104
(B) 260
(C) 151
(D) 156
(E) 161
ตอบกลับ: ตัวอักษร D
จำนวน นิวตรอน (n) สามารถคำนวณได้โดยใช้เลขมวล (A) และเลขอะตอม (Z) ผ่านสมการต่อไปนี้
A = Z + n
แทนที่เรามี:
260 = 104 + n
n = 260 - 104
n = 156
เครดิตภาพ
[1] กุหลาบอับบาส / shutterstock
โดย Stefano Araújo Novais
ครูสอนเคมี
แหล่งที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/rutherfordio-rf.htm

