กลไกคือการจำลองวิธีการประมวลผลปฏิกิริยา โดยอธิบายขั้นตอนที่สารตั้งต้นต้องผ่านเพื่อไปถึงผลิตภัณฑ์ขั้นสุดท้าย
มีการเสนอกลไกตามการทดลอง เนื่องจากไม่สามารถเห็นภาพทีละขั้นตอนของปฏิกิริยาได้ และมีประโยชน์มากใน เคมีอินทรีย์ เนื่องจากสารประกอบอินทรีย์ทำปฏิกิริยาซึ่งกันและกันในรูปแบบต่างๆ ได้แก่ พันธะแตก ก่อตัวเป็นสารประกอบ คนกลาง
มีปัจจัยที่รบกวนผลิตภัณฑ์สุดท้ายของปฏิกิริยา เช่น ลักษณะของตัวทำละลาย ขั้วของพันธะ การแลกเปลี่ยนอิเล็กตรอน เป็นต้น ดังนั้นกลไกบางอย่างจึงไม่ใช่วิธีเดียวสำหรับการก่อตัวของผลิตภัณฑ์เสมอไป แต่อาจเกิดขึ้นได้หลายวิธี เช่น ไอออนิกหรือผ่านอนุมูลอิสระ เป็นต้น
1. กลไกไอออนิก: กระบวนการที่เริ่มต้นจากการแตกเฮเทอโรไลติกของพันธะโควาเลนต์และการเกิดไอออน (คาร์โบเคชั่นและคาร์บาเนียน)
ติดตามกลไกอัลคีนฮาโลเจน
เราสามารถแบ่งกลไกออกเป็นขั้นตอน:
สเตจที่ 1: การหยุดชะงักของเฮเทอโรไลติกของพันธะโควาเลนต์ (Cl — Cl): การก่อตัวของคาร์โบเคชั่นและแอนไอออน (Cl-).
ระยะที่ 2: คลอไรด์ไอออน (Cl-) โจมตี carbocation
สเตจที่ 3: การก่อตัวของผลิตภัณฑ์ 1,2 - ไดคลอโรโพรเพน.
ดังที่เห็นได้ชัดเจน การเกิดฮาโลเจนของแอลคีนเกิดขึ้นผ่านกลไกไอออนิก
หมายเหตุ: ตามความหมายของชื่อ การทำฮาโลเจนทำได้โดยการเพิ่มฮาโลเจน (คลอรีน) ให้กับโมเลกุล
2. กลไกการเกิดอนุมูลอิสระ: การแตกของโฮโมไลติกของพันธะโควาเลนต์ก่อให้เกิดอนุมูลอิสระ (ไม่เสถียรและมีปฏิกิริยามาก) มาดูตัวอย่างกัน:
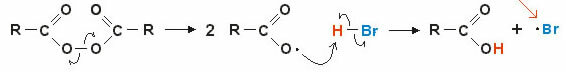
ปฏิกิริยาเริ่มต้นด้วยการทำลายพันธะเปอร์ออกซิดิกและการเกิดอนุมูลอิสระ ในขั้นตอนกลาง การโจมตีแบบรุนแรงจะเกิดขึ้นกับไฮโดรเจนโพลาไรซ์ของ (H — Br) และการเกิดอนุมูลอิสระใหม่ตามมา • br (ไม่เสถียรและมีปฏิกิริยาสูง)
โดย Líria Alves
จบเคมี
ทีมโรงเรียนบราซิล
ดูเพิ่มเติม!
อนุมูลอิสระในเคมีอินทรีย์
เคมีอินทรีย์ - เคมี - โรงเรียนบราซิล
แหล่งที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/mecanismos-reacoes-organicas.htm
