ปฏิกิริยากับ ออกไซด์พื้นฐาน เป็นปรากฏการณ์ทางเคมีที่มีสารของออกไซด์ประเภทนี้อยู่ในภาชนะเดียวกันกับ a กรดอนินทรีย์, NS กรดออกไซด์ หรือหนึ่ง แอมโฟเทอริกออกไซด์.
ดูด้วย:ปฏิกิริยากับแอมโฟเทอริกออกไซด์
เกลืออนินทรีย์ และน้ำเป็นผลิตภัณฑ์ทั่วไปใน a ปฏิกิริยากับออกไซด์พื้นฐาน เพื่อหาว่าเกลือหรือน้ำอนินทรีย์จะผลิตขึ้นหรือไม่ เราต้องดูที่สารที่มาพร้อมกับออกไซด์พื้นฐานในรีเอเจนต์ ดูตัวอย่างด้านล่างและทำความเข้าใจว่ากระบวนการนี้เกิดขึ้นได้อย่างไร
ปฏิกิริยากับออกไซด์พื้นฐานและกรดอนินทรีย์
ในปฏิกิริยาระหว่างออกไซด์พื้นฐานและกรดอนินทรีย์ จะเกิดเกลืออนินทรีย์และน้ำขึ้น เนื่องจากไอออนออกไซด์พื้นฐาน (Y+) โต้ตอบกับประจุลบ (X-) ของกรดและไฮโดรเนียมไอออนบวก (H+) ของกรดทำปฏิกิริยากับไอออนของออกไซด์:
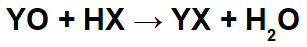
ตัวอย่าง: เรเดียมออกไซด์และกรดไฮโดรโบรม
ในปฏิกิริยานี้ เรามีเรเดียมออกไซด์ (RaO) และกรดไฮโดรโบรมิก (Hbr) เป็นสารตั้งต้น ดังนั้น การโต้ตอบต่อไปนี้จึงเกิดขึ้น:
วิทยุไอออนบวก (Ra+2) ด้วยไอออนโบรไมด์ (Br-1) ทำให้เกิดเกลือเรเดียมโบรไมด์ (RaBr2).
ไฮโดรเนียมไอออนบวก (H+1) ด้วยประจุลบออกไซด์ (O-2) ก่อตัวเป็นน้ำ (H2อ.)
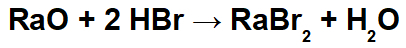
ดูด้วย:ปฏิกิริยากับดับเบิ้ลออกไซด์
ปฏิกิริยากับเบสออกไซด์และกรดออกไซด์
ในปฏิกิริยาเหล่านี้ เกลืออนินทรีย์จะเกิดขึ้นจากปฏิกิริยาระหว่างไอออนบวกออกไซด์พื้นฐาน (Y+) และประจุลบที่เป็นกรด (WONS-) ของปฏิกิริยาเคมีระหว่างกรดออกไซด์กับน้ำ
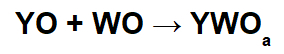
ตัวอย่าง: โซเดียมออกไซด์และซัลเฟอร์ไดออกไซด์
ในปฏิกิริยานี้ เรามีโซเดียมออกไซด์ (Na2O) และซัลเฟอร์ไดออกไซด์ (SO2). เป็นที่น่าสังเกตว่า ในตอนแรก เมื่อกรดออกไซด์ทำปฏิกิริยากับน้ำ เราจะเกิดกรดกำมะถัน (H2เท่านั้น3):

จากการก่อตัวของกรดนี้ ปฏิกิริยาระหว่างโซเดียมไอออนบวก (Na+1) ของออกไซด์พื้นฐานและประจุลบซัลไฟต์ (SO3-2) ของกรด ทำให้เกิดเกลือโซเดียมซัลไฟต์ (Na2เท่านั้น3):
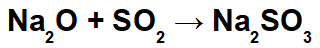
ปฏิกิริยากับออกไซด์พื้นฐานและแอมโฟเทอริกออกไซด์
แอมโฟเทอริกออกไซด์เป็นสารที่แสดงพฤติกรรมทางเคมีแบบคู่: ในที่ที่มีสารที่เป็นกรด มันจะทำตัวเหมือนออกไซด์พื้นฐาน ในที่ที่มีสารที่มีลักษณะพื้นฐาน มันจะทำตัวเหมือนกรดออกไซด์
ดังนั้นเมื่อ ออกไซด์พื้นฐานทำปฏิกิริยากับแอมโฟเทอริกออกไซด์ซึ่งจะมีพฤติกรรมเหมือนกรดออกไซด์ ก่อตัวเป็นกรดอนินทรีย์ในที่ที่มีน้ำ ปฏิกิริยาระหว่างประจุลบของกรดอนินทรีย์และไอออนบวกของออกไซด์พื้นฐานจะก่อให้เกิดผลิตภัณฑ์เกลือ
ตัวอย่าง: โพแทสเซียมออกไซด์และโครเมียม III ออกไซด์
ในปฏิกิริยานี้ เรามีโพแทสเซียมออกไซด์เป็นสารตั้งต้น (K2O) และโครเมียมออกไซด์ (Cr2อู๋3). เป็นที่น่าสังเกตว่า ในตอนแรก เมื่อแอมโฟเทอริกออกไซด์ทำปฏิกิริยากับน้ำ เรามีกรดโครโมโซมเกิดขึ้น (2HCrO)2):

จากการก่อตัวของกรดนี้ อันตรกิริยาระหว่างโพแทสเซียมไอออนเกิดขึ้น (K+1) ของออกไซด์พื้นฐานและแอนไอออนของโครไมต์ (SO3-2) ของกรดทำให้เกิดเกลือโพแทสเซียมโครไมต์ (2KCrO2):

By Me. ดิโอโก้ โลเปส ดิอาส
แหล่งที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/reacoes-com-oxidos-basicos.htm

