หน้าที่ทางเคมีคือการรวมกลุ่มของสารที่มีคุณสมบัติใกล้เคียงกัน คุณสมบัติเหล่านี้เรียกว่าการทำงาน เนื่องจากเป็นตัวกำหนดพฤติกรรมของสาร
หน้าที่หลักของสารเคมีอนินทรีย์ ได้แก่ กรด เบส เกลือ และออกไซด์
กรด
กรดเป็นสารประกอบที่เกิดจากพันธะโควาเลนต์ ซึ่งใช้อิเล็กตรอนร่วมกัน ตามคำกล่าวของนักเคมี Svante Arrhenius (1859-1927) สารประกอบเหล่านี้ปล่อย H ไอออน+ เมื่อสัมผัสกับน้ำ
จะระบุกรดได้อย่างไร?
สูตรทั่วไปของกรดคือ HxA โดยที่ A แทนประจุลบ H คือไฮโดรเจน และ x คือจำนวนอะตอมของธาตุนี้ที่มีอยู่ในโมเลกุล
วันนี้ เรารู้ว่าเมื่อสัมผัสกับน้ำ กรดจะปล่อย H เป็นไอออนบวกเพียงตัวเดียว+ และสร้างไฮโดรเนียมไอออนบนไอออไนเซชัน นอกจากนี้ เมื่อกรดถูกแตกตัวเป็นไอออนในสารละลายที่เป็นน้ำ กรดเหล่านี้สามารถนำไฟฟ้าได้
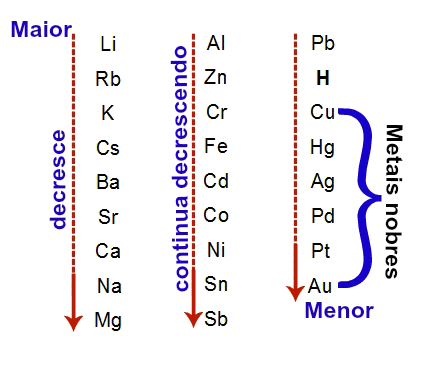
ความแรงของกรดวัดจากความสามารถในการแตกตัวเป็นไอออนเมื่อสัมผัสกับน้ำ ยิ่งโมเลกุลของกรดแตกตัวเป็นไอออนในน้ำมาก กรดก็จะยิ่งแรง
ตัวอย่าง: HCl เป็นกรดแก่ เนื่องจากมีระดับการแตกตัวเป็นไอออน 92% H2CO3 มันเป็นกรดอ่อน เนื่องจากโมเลกุลของกรดเพียง 0.18% เท่านั้นที่แตกตัวเป็นไอออนในสารละลาย
การจำแนกกรด
เราสามารถจำแนกกรดตามจำนวนไฮโดรเจนที่แตกตัวเป็นไอออนได้ใน:
- กรดโมโน: มีไฮโดรเจนที่แตกตัวเป็นไอออนได้เพียงตัวเดียว เช่น HCN;
- Diacid: มีไฮโดรเจนสองชนิดที่แตกตัวเป็นไอออนได้ เช่น H2เท่านั้น3;
- Triacid: มีไฮโดรเจนที่แตกตัวเป็นไอออนได้สามชนิด เช่น H3ฝุ่น4;
- Tetracid: มีไฮโดรเจนที่แตกตัวเป็นไอออนได้สี่ชนิด เช่น H4พี2อู๋7.
กรดยังจำแนกตามการขาดออกซิเจนใน ให้ความชุ่มชื้นเช่น HCl และ HCN และเมื่อมีธาตุออกซิเจนจะเรียกว่า ออกซีแอซิดเช่น H2เท่านั้น4 และ HNO3.
ตัวอย่างของกรด
- กรดกำมะถัน H2เท่านั้น4
- กรดไฮโดรคลอริก HCl
- กรดไฮโดรฟลูออริก HF
- กรดไนตริก HNO3
- กรดฟอสฟอริก H3ฝุ่น4
- กรดคาร์บอนิก H2CO3
ดูข้อมูลเพิ่มเติมเกี่ยวกับ กรด.
ฐาน
เบสเป็นสารประกอบที่เกิดจากพันธะไอออนิกซึ่งมีการบริจาคอิเล็กตรอน ตามคำกล่าวของนักเคมี Svante Arrhenius (1859-1927) สารประกอบเหล่านี้จะปล่อย OH ไอออน- เมื่อสัมผัสกับน้ำเนื่องจากสารประกอบจะแยกตัวออกจากกัน
จะระบุฐานได้อย่างไร?
สูตรทั่วไปของเบสคือ โดยที่ B แทนประจุบวก (อนุมูลบวก) ที่ประกอบเป็นฐาน และ y คือประจุที่กำหนดจำนวนไฮดรอกซิล (OH-).
เบสมีรสฝาด กัดกร่อนและขม เมื่อแยกตัวออกจากตัวกลางที่เป็นน้ำ เบสก็นำไฟฟ้าด้วย
เบสคือสารประกอบที่แยกตัวออกจากสารละลายในน้ำ และความแข็งแรงของเบสวัดจากระดับความแตกตัว ดังนั้น ยิ่งโครงสร้างแยกตัวในน้ำมาก ฐานก็จะยิ่งแข็งแรง
ตัวอย่าง: NaOH เป็นเบสที่แข็งแรง เนื่องจากมีระดับการแตกตัวเป็นไอออน 95% NH4OH เป็นเบสที่อ่อนแอเนื่องจากสารประกอบเพียง 1.5% เท่านั้นที่ผ่านการแยกตัวของไอออนิก
การจำแนกฐาน
เบสสามารถจำแนกได้ตามจำนวนของไฮดรอกซิลที่ปล่อยออกมาในสารละลายใน:
- Monobase: มีไฮดรอกซิลเพียงตัวเดียว เช่น NaOH;
- Dibase: มีไฮดรอกซิลสองตัวเช่น Ca (OH)2;
- Tribase: มีไฮดรอกซิลสามชนิดเช่น Al (OH)3;
- Tetrabase: มีไฮดรอกซิลสี่ชนิด เช่น Pb (OH)4.
ฐานโลหะอัลคาไลและโลหะอัลคาไลน์เอิร์ ธ ยกเว้นเบริลเลียมและแมกนีเซียมถือเป็นเบสที่แข็งแรงเนื่องจากมีความแตกแยกในระดับสูง ในทางกลับกันฐานที่อ่อนแอมีระดับการแยกตัวน้อยกว่า 5% เช่น NH4OH และ Zn(OH)2.
ตัวอย่างของฐาน
- โซเดียมไฮดรอกไซด์ NaOH
- แอมโมเนียมไฮดรอกไซด์ NH4โอ้
- โพแทสเซียมไฮดรอกไซด์ KOH
- แมกนีเซียมไฮดรอกไซด์ Mg(OH)2
- เหล็กไฮดรอกไซด์ Fe(OH)3
- แคลเซียมไฮดรอกไซด์ Ca(OH)2
ดูข้อมูลเพิ่มเติมเกี่ยวกับ ฐาน.
เกลือ
เกลือเป็นสารประกอบที่เกิดจากปฏิกิริยาที่เกิดขึ้นระหว่างกรดกับเบส เรียกว่าปฏิกิริยาการทำให้เป็นกลาง
ดังนั้นเกลือจึงเกิดจากไอออนบวกที่มาจากเบสและแอนไอออนที่มาจากกรด
จะระบุเกลือได้อย่างไร?
เกลือเป็นสารประกอบไอออนิกที่มีโครงสร้างเป็น CxTHEy เกิดจาก C cationy+ (ไอออนบวก) นอกจาก H+และประจุลบ Ax- (ไอออนลบ) ซึ่งต่างจาก OH-.
เกลือในสภาวะแวดล้อมจะปรากฏเป็นของแข็งผลึก โดยมีจุดหลอมเหลวและจุดเดือดสูง นอกจากนี้หลายชนิดยังมีรสเค็มที่มีลักษณะเฉพาะ
แม้ว่าเกลือบางชนิดจะเป็นที่รู้จักและนำไปใช้ในอาหาร เช่น โซเดียมคลอไรด์ (เกลือแกง) แต่ก็มีเกลือที่เป็นพิษร้ายแรง
เมื่ออยู่ในสารละลายที่เป็นน้ำ เกลือสามารถนำไฟฟ้าได้ เกลือหลายชนิดสามารถดูดซับความชื้นจากสิ่งแวดล้อมได้ง่ายจึงเรียกว่าดูดความชื้น
การจำแนกประเภทของเกลือ
เกลือถูกจำแนกตามลักษณะของมันในสารละลายที่เป็นน้ำ
เกลือเป็นกลาง: เกิดจากไอออนบวกเบสแก่และไอออนที่เป็นกรดแก่หรือไอออนบวกเบสอ่อนและไอออนกรดอ่อน
ตัวอย่าง: HCl (กรดแก่) + NaOH (เบสแก่) → NaCl (เกลือเป็นกลาง) + H2โอ (น้ำ)
เกลือกรด: เกิดจากไอออนบวกเบสอ่อนและไอออนที่เป็นกรดแก่
ตัวอย่าง: HNO3 (กรดแก่) + AgOH (เบสอ่อน) → AgNO3 (เกลือกรด) + H2โอ (น้ำ)
เกลือพื้นฐาน: เกิดจากไอออนบวกเบสแก่และแอนไอออนกรดอ่อน
ตัวอย่าง: H2CO3 (กรดอ่อน) + NaOH (เบสแก่) → NaHCO3 (เกลือพื้นฐาน) + H2โอ (น้ำ)
ตัวอย่างของเกลือ
- โพแทสเซียมไนเตรต KNO3
- โซเดียมไฮโปคลอไรท์ NaClO
- โซเดียมฟลูออไรด์ NaF
- โซเดียมคาร์บอเนต Na2CO3
- แคลเซียมซัลเฟต CaSO4
- อะลูมิเนียมฟอสเฟต AlPO4
ดูข้อมูลเพิ่มเติมเกี่ยวกับ เกลือ.
ออกไซด์
ออกไซด์เป็นสารประกอบที่เกิดจากองค์ประกอบทางเคมีสองชนิด ซึ่งหนึ่งในนั้นคือออกซิเจน ซึ่งเป็นสารประกอบที่มีอิเลคโตรเนกาติตีมากที่สุด
จะระบุออกไซด์ได้อย่างไร?
สูตรทั่วไปของออกไซด์คือ โดยที่ C แทนไอออนบวก (ไอออนบวก) ที่จับกับออกซิเจน ค่า y (ประจุไอออนบวก) ระบุจำนวนอะตอมของออกซิเจนที่ต้องประกอบเป็นออกไซด์
ออกไซด์เป็นสารเลขฐานสองซึ่งออกซิเจนเชื่อมโยงกับองค์ประกอบทางเคมีที่มีอิเล็กโตรเนกาติตีน้อยกว่า ดังนั้นการจับตัวของออกซิเจนกับฟลูออรีนเช่นเดียวกับในสารประกอบ OF2 มันเป็น2F2ไม่ถือเป็นออกไซด์
การจำแนกประเภทของออกไซด์
โมเลกุลออกไซด์ (ออกซิเจน + อะเมทัล) มีลักษณะเป็นกรด เพราะเมื่ออยู่ในสารละลายในน้ำ พวกมันจะทำปฏิกิริยากับกรดที่ผลิตได้ เช่น คาร์บอนไดออกไซด์ (CO2).
ไอออนิกออกไซด์ (ออกซิเจน + โลหะ) มีลักษณะพื้นฐาน เมื่อสัมผัสกับน้ำ จะสร้างสารละลายพื้นฐาน เช่น แคลเซียมออกไซด์ (CaO)
เมื่อออกไซด์ไม่ทำปฏิกิริยากับน้ำ เช่น คาร์บอนมอนอกไซด์ (CO) จะมีลักษณะเป็นออกไซด์ที่เป็นกลาง
ตัวอย่างของออกไซด์
- ดีบุกออกไซด์ SnO2
- เหล็กออกไซด์ III, Fe2อู๋3
- โซเดียมออกไซด์ Na2อู๋
- ลิเธียมออกไซด์ Li2อู๋
- ดีบุกไดออกไซด์ SnO2
- ไนโตรเจนไดออกไซด์ NO2
ดูข้อมูลเพิ่มเติมเกี่ยวกับ ออกไซด์.
ความสนใจ!
คลาสของกรด เบส เกลือ และออกไซด์ จัดเป็นหน้าที่ทางเคมีเพื่ออำนวยความสะดวกในการศึกษาสารประกอบอนินทรีย์ เนื่องจากจำนวนของสารมีมาก
อย่างไรก็ตาม บางครั้งพวกมันสามารถผสมกันได้ เช่นเดียวกับในกรณีของเกลือและออกไซด์ ซึ่งอาจมีลักษณะเป็นกรดหรือด่าง นอกจากนี้ พฤติกรรมของสารยังได้รับอิทธิพลจากปฏิกิริยากับสารประกอบอื่นๆ
ในเคมีอินทรีย์ เป็นไปได้ที่จะเห็นภาพกลุ่มหน้าที่ต่างๆ ของสารประกอบอินทรีย์
รู้ยัง ฟังก์ชั่นอินทรีย์.
สารประกอบอนินทรีย์หลัก
ดูตัวอย่างบางส่วนของสารประกอบจาก ฟังก์ชั่นอนินทรีย์ และการใช้งานคืออะไร
กรด
กรดไฮโดรคลอริก HCl
กรดไฮโดรคลอริกเป็นกรด monoacid ที่แรง เป็นสารละลายในน้ำที่มี HCl 37%, ไฮโดรเจนคลอไรด์, ก๊าซไม่มีสี เป็นพิษมากและมีฤทธิ์กัดกร่อน
ใช้สำหรับทำความสะอาดโลหะ ในกระบวนการผลิตเครื่องหนัง และเป็นวัตถุดิบสำหรับสารประกอบทางเคมีอื่นๆ สารนี้จำหน่ายเป็นกรดมูริอาติกสำหรับทำความสะอาดพื้น กระเบื้อง และพื้นผิวโลหะ
กรดกำมะถัน H2เท่านั้น4
อู๋ กรดซัลฟูริก มันเป็นไดแอซิดที่แรง เป็นของเหลวไม่มีสีและหนืด ซึ่งถือว่ามีความเข้มข้นเนื่องจากระดับการแตกตัวเป็นไอออนมากกว่า 50% ที่อุณหภูมิ 18º C
กรดอนินทรีย์นี้ใช้ในอุตสาหกรรมเคมีขนาดใหญ่เป็นวัตถุดิบสำหรับ การผลิตวัสดุหลายชนิด ดังนั้น การบริโภคจึงสามารถบ่งบอกถึงดัชนีการพัฒนาเศรษฐกิจ ของประเทศ
ฐาน
แมกนีเซียมไฮดรอกไซด์ Mg(OH)2
แมกนีเซียมไฮดรอกไซด์เป็นไดเบสเนื่องจากมีไฮดรอกซิลสองชนิดในรัฐธรรมนูญ ภายใต้สภาวะแวดล้อม สารประกอบทางเคมีจะเป็นของแข็งสีขาว และสารแขวนลอยในน้ำมีจำหน่ายภายใต้ชื่อ Milk of Magnesia
นมแมกนีเซียใช้เป็นยาลดกรด ช่วยลดกรดในกระเพาะ และเป็นยาระบาย ช่วยปรับปรุงการทำงานของลำไส้
โซเดียมไฮดรอกไซด์ NaOH
อู๋ โซเดียมไฮดรอกไซด์เรียกอีกอย่างว่าโซดาไฟ ในสภาวะแวดล้อมอยู่ในสถานะของแข็ง มีสีขาวนวล และมีความเป็นพิษสูงและมีฤทธิ์กัดกร่อนสูง
เป็นฐานที่แข็งแกร่ง ใช้ทั้งในอุตสาหกรรม การผลิตผลิตภัณฑ์ทำความสะอาด และสำหรับใช้ในบ้าน เพื่อคลายการอุดตันของท่อ เป็นต้น
การใช้ผลิตภัณฑ์ต้องได้รับการดูแลเป็นอย่างมากเนื่องจากการสัมผัสกับผิวหนังอาจทำให้เกิดแผลไหม้อย่างรุนแรง
เกลือ
โซเดียมคลอไรด์ NaCl
เกลือแกงซึ่งมีชื่อทางเคมีว่าโซเดียมคลอไรด์ เป็นสารที่ใช้กันอย่างแพร่หลายในฐานะเครื่องปรุงและสารกันบูดอาหาร
เทคนิคหนึ่งที่ใช้ในการผลิตเกลือแกงคือการระเหยน้ำทะเลและทำให้สารประกอบทางเคมีตกผลึก ต่อจากนั้นเกลือจะผ่านกระบวนการกลั่น
อีกวิธีหนึ่งที่โซเดียมคลอไรด์มีอยู่ในชีวิตของเราคือในน้ำเกลือ ซึ่งเป็นสารละลายในน้ำที่มีเกลือ 0.9%
โซเดียมไบคาร์บอเนต NaHCO3
โซเดียม ไฮโดรเจน คาร์บอเนต หรือที่รู้จักกันแพร่หลายว่า โซเดียม ไบคาร์บอเนต เป็นเกลือที่มีผลึกขนาดเล็กมาก มีลักษณะเป็นผง ซึ่งละลายในน้ำได้ง่าย
เป็นสารที่มีการใช้งานในครัวเรือนมากมาย ไม่ว่าจะใช้ทำความสะอาด ผสมกับสารอื่นๆ หรือเพื่อสุขภาพ เนื่องจากมีอยู่ในองค์ประกอบของสารฟู่
ออกไซด์
ไฮโดรเจนเปอร์ออกไซด์ H2อู๋2
อู๋ ไฮโดรเจนเปอร์ออกไซด์ มันถูกวางตลาดเป็นสารละลายที่เรียกว่าไฮโดรเจนเปอร์ออกไซด์ซึ่งเป็นของเหลวที่ออกซิไดซ์สูง เมื่อไม่ละลายในน้ำ ไฮโดรเจนเปอร์ออกไซด์ค่อนข้างไม่เสถียรและสลายตัวอย่างรวดเร็ว
การใช้งานหลักของสารละลายไฮโดรเจนเปอร์ออกไซด์ ได้แก่ น้ำยาฆ่าเชื้อ สารฟอกสีฟัน และสารฟอกสีผม
คาร์บอนไดออกไซด์ CO2
อู๋ คาร์บอนไดออกไซด์เรียกอีกอย่างว่าคาร์บอนไดออกไซด์เป็นโมเลกุลออกไซด์ที่ไม่มีสี ไม่มีกลิ่น และหนักกว่าอากาศ
ในการสังเคราะห์ด้วยแสง CO2 บรรยากาศถูกจับจากชั้นบรรยากาศและทำปฏิกิริยากับน้ำ ทำให้เกิดกลูโคสและออกซิเจน ดังนั้นกระบวนการนี้จึงมีความสำคัญต่อการต่ออายุออกซิเจนในอากาศ
อย่างไรก็ตาม ความเข้มข้นสูงของคาร์บอนไดออกไซด์ในชั้นบรรยากาศเป็นสาเหตุหนึ่งที่ทำให้ปรากฏการณ์เรือนกระจกรุนแรงขึ้น โดยยังคงรักษาระดับความร้อนในชั้นบรรยากาศไว้ได้มากขึ้น