ปฏิกิริยารีดอกซ์เกี่ยวข้องกับการถ่ายโอนอิเล็กตรอนระหว่างอะตอม ไอออน หรือโมเลกุล
ในปฏิกิริยาออกซิเดชัน-รีดิวซ์ การเปลี่ยนแปลงของเลขออกซิเดชัน (nox) จะเกิดขึ้น การลดออกซิเจนประกอบด้วยกระบวนการออกซิเดชันและรีดักชัน:
- ออกซิเดชัน: ผลลัพธ์ใน การสูญเสียอิเล็กตรอน และน็อกซ์ที่เพิ่มขึ้น
- ลดกระหน่ำ: ผลลัพธ์ใน การรับอิเล็กตรอน และ nox ที่ลดลง
เมื่อธาตุหนึ่งละอิเลคตรอน อีกธาตุหนึ่งก็จะได้รับอิเล็กตรอน ดังนั้นจำนวนอิเล็กตรอนทั้งหมดที่ได้รับจึงเท่ากับจำนวนอิเล็กตรอนที่สูญเสียไปทั้งหมด
ตัวอย่างปฏิกิริยารีดอกซ์ต่อการเผาไหม้ การกัดกร่อน และการสังเคราะห์ด้วยแสง
ตัวอย่าง
ขึ้นอยู่กับองค์ประกอบที่รับหรือบริจาคอิเล็กตรอน เรามีชื่อดังต่อไปนี้:
- ตัวแทนลด: สารที่ผ่านออกซิเดชันทำให้เกิดการลดลงและเพิ่มจำนวน nox ของมัน เป็นสิ่งที่สูญเสียอิเล็กตรอน
- ออกซิไดซ์: สารที่ผ่านการรีดักชันทำให้เกิดปฏิกิริยาออกซิเดชันและลดจำนวนน็อกซ์ลง เป็นสิ่งที่ได้รับอิเล็กตรอน
อู๋ เลขออกซิเดชัน แสดงถึงประจุไฟฟ้าของธาตุ ณ เวลาที่มันเข้าร่วมในa พันธะเคมี.
เงื่อนไขนี้เกี่ยวข้องกับ อิเล็กโตรเนกาติวีตี้ซึ่งเป็นแนวโน้มที่ธาตุบางชนิดจะได้รับอิเล็กตรอน
1. สังเกตตัวอย่างแรก สังเกตว่าในปฏิกิริยาระหว่างเหล็กกับคลอรีนจะมีการเปลี่ยนแปลงในเลขออกซิเดชัน อู๋
คลอรีน โดยเป็นอิเลคโตรเนกาติตีมากขึ้น จะได้รับอิเล็กตรอน: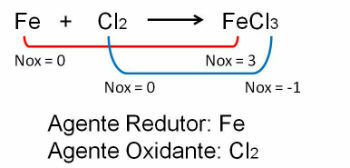
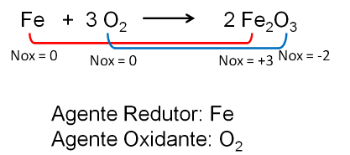
2. ปฏิกิริยาระหว่างเหล็กกับออกซิเจน ออกซิเจนมีอิเลคโตรเนกาติตีมากกว่าและจบลงด้วยการรับอิเล็กตรอนและลดจำนวนออกซิเดชันของพวกมัน
เรียนรู้เพิ่มเติมอ่านยัง:
- ออกซิเดชัน
- การเผาไหม้
- ปฏิกริยาเคมี
- อิเล็กตรอน
แก้ไขการออกกำลังกาย
1. (PUC-RS) สัมพันธ์กับสมการออกซิเดชัน - การรีดิวซ์แบบไม่สมดุล Fe0 + CuSO4 → เฟ2(เท่านั้น4)3 + Cu0, อาจกล่าวได้ว่า:
ก) จำนวนออกซิเดชันของทองแดงในคิวปริกซัลเฟตคือ +1
b) อะตอมของเหล็กสูญเสียอิเล็กตรอน 2 ตัว
c) ทองแดงผ่านการเกิดออกซิเดชัน
ง) เหล็กเป็นตัวออกซิไดซ์
จ) เหล็กผ่านการเกิดออกซิเดชัน
ความละเอียด:
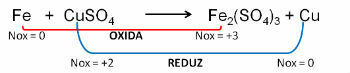
ตอบ:
จ) เหล็กผ่านการเกิดออกซิเดชัน
การออกกำลังกาย
1. (UFAC-AC) ในสมการเคมีต่อไปนี้: Zn + 2 HCℓ → ZnCℓ2 + โฮ2
ก) ธาตุ Zn ออกซิไดซ์และทำปฏิกิริยาเป็นตัวออกซิไดซ์
b) ธาตุ Zn ออกซิไดซ์และทำปฏิกิริยาเป็นตัวรีดิวซ์
c) องค์ประกอบ Zn ลดลงและทำปฏิกิริยาเป็นตัวรีดิวซ์
d) HCℓ เป็นตัวรีดิวซ์
จ) สมการถูกจัดประเภทย้อนกลับได้
b) ธาตุ Zn ออกซิไดซ์และทำปฏิกิริยาเป็นตัวรีดิวซ์
2. (ITA-SP) ในปฏิกิริยาไอออนิก Ni(s) + Cu2+(aq) → นิ2+(aq) + ลูกบาศ์ก (s)
ก) นิกเกิลเป็นตัวออกซิไดซ์เพราะถูกออกซิไดซ์
b) นิกเกิลเป็นตัวลดเพราะมันถูกออกซิไดซ์
c) คิวปริกไอออนเป็นตัวออกซิไดซ์เพราะถูกออกซิไดซ์
d) คิวปริกไอออนเป็นตัวลดเพราะมันลดลง
จ) ไม่ใช่ปฏิกิริยารีดอกซ์ ดังนั้นจึงไม่มีสารออกซิไดซ์หรือรีดิวเซอร์
b) นิกเกิลเป็นตัวลดเพราะมันถูกออกซิไดซ์
3. (UFRGS) สารออกฤทธิ์ในสารฟอกขาวในครัวเรือนคือไฮโปคลอไรท์ไอออน ClO- ในกระบวนการฟอกขาว ไอออนนี้จะลดลง ซึ่งหมายความว่า:
ก) สารที่ผ่านการกระทำของไฮโปคลอไรท์จะได้รับอิเล็กตรอน
b) จำนวนอิเล็กตรอนในโครงสร้างลดลง
c) ClO- เป็นตัวรีดิวซ์
d) ClO- ถูกแปลงเป็นธาตุคลอรีนหรือคลอไรด์ไอออน
จ) ไม่มีการถ่ายโอนอิเล็กตรอนเกิดขึ้น
d) ClO- ถูกแปลงเป็นธาตุคลอรีนหรือคลอไรด์ไอออน