THE การกลั่น เป็นกระบวนการหนึ่งของการแยกของผสมที่เป็นเนื้อเดียวกันซึ่งเกิดขึ้นผ่านการต้ม โดยที่ของเหลวจะระเหยกลายเป็นไอและควบแน่น ดังนั้นของผสมที่จะแยกออกมาจึงมีจุดเดือดต่างกัน
กล่าวอีกนัยหนึ่ง การกลั่นเป็นกระบวนการทางเคมีกายภาพของการแยกสารผสมที่เกิดขึ้นจากการให้ความร้อนและความเย็นของสารผสม เมื่อส่วนผสมถูกทำให้ร้อน สารที่มีจุดเดือดต่ำที่สุดคือระเหยง่ายที่สุดก่อนจะระเหย
การกลั่นดำเนินการในห้องปฏิบัติการเคมีและอุตสาหกรรมโดยใช้อุปกรณ์เฉพาะ (คอนเดนเซอร์ เทอร์โมมิเตอร์ การกลั่น หัวเป่า บีกเกอร์ เสื้อคลุมให้ความร้อน คอลัมน์การแยกส่วน) ตัวอย่างเช่น เมื่อแยกน้ำออกจากแอลกอฮอล์หรือน้ำออกจากเครื่อง เกลือ.
ตัวอย่างที่เป็นธรรมชาติของกระบวนการกลั่นเกิดขึ้นเมื่อหยดน้ำกลั่นตัวในวันที่อากาศเย็นกว่า นอกจากนี้เครื่องดื่มกลั่นที่เรียกว่า (cachaça, วอดก้า, บรั่นดี, เตกีลา, รัม, วิสกี้) ถูกผลิตขึ้นโดยกระบวนการกลั่นแบบเศษส่วนซึ่งใช้มาตั้งแต่สมัยโบราณ
ประเภทของการกลั่น
การกลั่นสามารถทำได้สองวิธีขึ้นอยู่กับลักษณะของสารผสมที่แยกจากกัน:
การกลั่นอย่างง่าย
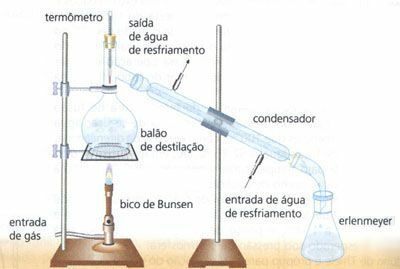 การกลั่นอย่างง่าย
การกลั่นอย่างง่าย
การแยกของผสมที่เป็นเนื้อเดียวกันของของแข็งและของเหลว เช่น น้ำ (H
2O) ของเกลือ (NaCl) ด้วยวิธีนี้ น้ำจะระเหยผ่านความร้อน ซึ่งไหลผ่านคอนเดนเซอร์ในรูปของ ของเหลว (หยดน้ำ) โดยที่เกลือจะถูกกักและแยกไว้ในภาชนะที่เรียกว่า a การกลั่นการกลั่นแบบเศษส่วน
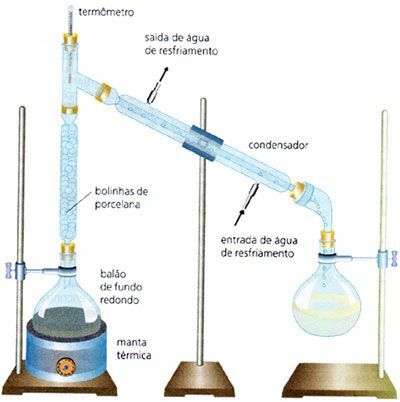 การกลั่นแบบเศษส่วน
การกลั่นแบบเศษส่วน
ใช้กันอย่างแพร่หลายในอุตสาหกรรมคือการแยกส่วนผสมที่เป็นเนื้อเดียวกันของของเหลวและของเหลวโดย ตัวอย่าง น้ำและแอลกอฮอล์ (จุดเดือดของน้ำคือ 100°C และจุดเดือดของเอทิลแอลกอฮอล์ คือ 78°C) จะดำเนินการผ่านสารผสมที่มีจุดเดือดใกล้มาก ในกรณีนี้มีคอลัมน์การแยกส่วนต่างจากกระบวนการกลั่นอย่างง่าย
การกลั่นน้ำมัน
เพื่อให้ได้ผลิตภัณฑ์ปิโตรเลียม (น้ำมันเบนซิน น้ำมันก๊าด น้ำมันเชื้อเพลิง พาราฟิน ยางมะตอย) กระบวนการกลั่น การแยกส่วนใช้เมื่อของเหลวที่มีจุดเดือดต่ำสุดถูกแยกออกก่อนจนกว่าจะถึงของเหลวที่มีจุดเดือดสูงสุด เดือด
จำไว้ว่า ปิโตรเลียม เป็นสารธรรมชาติที่ประกอบด้วยส่วนประกอบอินทรีย์หลายชนิด โดยเฉพาะไฮโดรคาร์บอน (โมเลกุลของคาร์บอนและไฮโดรเจน)
การกลั่นแบบอะซีโอทรอปิก
การกลั่นอะซีโอโทรปิกเกิดขึ้นเมื่อการแยกสารผสมก่อให้เกิดอะซีโอโทรป กล่าวคือ มีความผันผวนและจุดต่ำ จุดเดือดคงที่ซึ่งไม่สามารถแยกออกได้โดยวิธีการกลั่นอย่างง่าย เช่น กรดไฮโดรคลอริก (HCL) และน้ำ (H2อ.)
เรื่องน่ารู้: รู้ยัง?
น้ำกลั่น (น้ำปราศจากแร่ธาตุ) เป็นสารบริสุทธิ์ที่ได้จากการกลั่นและมักใช้ในห้องปฏิบัติการ โปรดทราบว่าน้ำที่เราดื่มนั้นไม่บริสุทธิ์ กล่าวคือ มีเกลือแร่รวมอยู่ด้วย อย่างไรก็ตาม น้ำกลั่นสามารถนำมาใช้เพื่อการบริโภคของมนุษย์ได้เช่นเดียวกับการรักษาโรคบางชนิด เช่น นิ่วในไต
เสริมงานวิจัยของคุณโดยการอ่านบทความ:
- จุดหลอมเหลวและจุดเดือด
- การทำให้เป็นของเหลวหรือการควบแน่น
- การทำให้กลายเป็นไอ
- การแยกสารผสม
ตรวจสอบคำถามสอบเข้าพร้อมคำติชมแสดงความคิดเห็นบน: แบบฝึกหัดการแยกผสม.