องค์ประกอบที่ตั้งชื่อตาม โลหะอัลคาไลน์เอิร์ ธ เป็นของตระกูล 2 หรือ IIA ของตารางธาตุ กลุ่มดังกล่าวประกอบด้วยองค์ประกอบทางเคมีดังต่อไปนี้: Be (เบริลเลียม), Mg (แมกนีเซียม), Ca (แคลเซียม), Sr (สตรอนเทียม), Ba (แบเรียม) และเรเดียม (Ra)

พวกมันมีอิเล็กตรอนสองตัวในเปลือกเวเลนซ์ และการกระจายทั่วไปของพวกมันจะถูกแทนด้วย ns2 โดยที่ ไม่ หมายถึงจำนวนของระดับสุดท้าย เนื่องจากลักษณะเฉพาะนี้ พวกมันมักจะสูญเสียอิเล็กตรอนสองตัวนี้ ทำให้เกิดประจุบวก 2+
คำว่า "โลก" หมายถึง "มีอยู่บนโลก" เนื่องจากเป็นตำแหน่งที่พบธาตุเหล่านี้ ส่วนใหญ่อยู่ในแร่ธาตุ เช่น แคลเซียมในรูปของสารประกอบแคลเซียมฟอสเฟต (Ca3(ฝุ่น4)2) พบในเปลือกโลกและทำหน้าที่เป็นวัตถุดิบในการผลิตฟอสฟอรัส นอกจากนี้ยังมีอยู่ในกระดูกของสัตว์มากจนเมื่อเผาสิ่งเหล่านี้จะได้รับ "กระดูกป่น" ซึ่งประกอบด้วยแคลเซียมฟอสเฟต
ในบรรดาโลหะอัลคาไลน์เอิร์ ธ สิ่งที่โดดเด่นที่สุดคือ แคลเซียม มันเป็น แมกนีเซียม.
- แคลเซียม
แคลเซียมไอออน (Ca2+) มีอยู่ในประมาณ 90% ของกระดูกและฟันของเรา และในสัตว์ก็มีอยู่ในเปลือกหอยด้วย หน้าที่ของมันคือเสริมสร้างโครงสร้างกระดูกและทำหน้าที่เป็นตัวคลายกล้ามเนื้อ การขาดแคลเซียมในร่างกายอาจทำให้กล้ามเนื้อเป็นตะคริว บาดทะยัก และโรคกระดูกพรุนได้ ด้วยเหตุนี้จึงเป็นสิ่งสำคัญที่จะกินมันผ่านอาหารที่อุดมด้วยแคลเซียม เช่น นมและอนุพันธ์ (เนย ชีส ฯลฯ) เนื้อสัตว์และผัก
ในทางกลับกัน แคลเซียมที่มากเกินไปอาจทำให้กล้ามเนื้อผ่อนคลาย นิ่วในไต และปวดกระดูกได้
นอกจากอาหารดังกล่าวแล้ว แคลเซียมยังมีอยู่ในธรรมชาติหลายๆ ส่วน โดยเฉพาะในแร่ธาตุ เช่น แคลไซต์ (CaCO)3) หรือแคลเซียมคาร์บอเนตซึ่งเป็นส่วนประกอบของหินปูนและหินอ่อน และใช้หินอ่อนในการผลิตอ่างล้างมือ รูปปั้น พื้นและบันได แคลเซียมคาร์บอเนตยังเป็นตัวสร้างหินงอกหินย้อยในถ้ำอีกด้วย แคลเซียมยังมีอยู่ในยิปซั่มธรรมชาติ (CaSO4. 2 ชั่วโมง2O) เรียกว่า ยิปซั่ม เกลือนี้สามารถถูกคายน้ำได้ ทำให้เกิดCaSO4 ปราศจากน้ำซึ่งเป็นชอล์กโรงเรียน
ในอุตสาหกรรม ปูนขาว (CaO) ถูกผลิตขึ้น ปูนขาว เรียกอีกอย่างว่าปูนขาวหรือปูนขาว ซึ่งจริงๆ แล้วเป็นแคลเซียมไฮดรอกไซด์ (Ca (OH)2) ใช้ในน้ำยาล้างจานและในการเตรียมปูน การให้ความร้อนเล็กน้อยของยิปซั่มทำให้ได้แคลเซียมซัลเฟตซึ่งก็คือยิปซั่มที่ใช้ในการก่อสร้าง ในการผลิตแม่พิมพ์ทางทันตกรรมและการแพทย์เพื่อป้องกันกระดูกหัก เช่น แขนข้างหนึ่งที่แสดงด้านล่าง
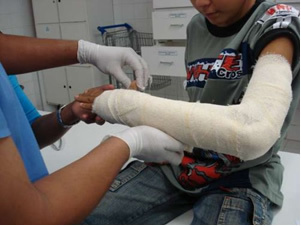
- แมกนีเซียม
ไอออนของ แมกนีเซียม นอกจากนี้ยังมีความสำคัญทางชีวภาพอย่างมาก เนื่องจากกระดูกของเรามีอยู่ใน 70% ซึ่งสนับสนุนการทำงานของเอนไซม์ กล้ามเนื้อ และการประสานงานของมอเตอร์ การขาดสารอาหารในร่างกายอาจทำให้เกิดอาการเวียนศีรษะ ความดันโลหิตสูง อาการสั่น และชีพจรที่อ่อนแอ ดังนั้นเราควรรับประทานอาหารที่มีธาตุนี้ ได้แก่ ถั่ว ธัญพืช และผักใบเขียว นอกจากนี้ แมกนีเซียมส่วนเกินในร่างกายอาจทำให้เกิดอาการง่วงนอนได้
แมกนีเซียมยังมีอยู่ในน้ำทะเลและแร่ธาตุ ใช้ในโลหะผสม เช่น โลหะบูชายัญ (ซึ่งออกซิไดซ์แทนเหล็ก ป้องกันการกัดกร่อน) ในล้อ "แมกนีเซียม" และในดอกไม้ไฟ (ให้สีเงินและสีขาว) สารประกอบที่สำคัญมากของแมกนีเซียมคือแมกนีเซียมไฮดรอกไซด์ (Mg(OH)2) ซึ่งเมื่อกระจายตัวในน้ำที่ความเข้มข้นประมาณ 7% จะทำให้เกิดสารแขวนลอยที่ทราบ นิยมเป็นน้ำนมจากแมกนีเซีย ซึ่งทำหน้าที่เป็นยาลดกรด ต่อสู้กับกรดในกระเพาะ (อิจฉาริษยา) และ as ยาระบาย

โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/quimica/metais-alcalinoterrosos.htm
