พลังงานความร้อน เป็นคำกว้างๆ ที่ใช้เพื่อแสดงปริมาณทางอุณหพลศาสตร์ที่แตกต่างกัน เช่น กำลังภายใน หรือจำนวน ความร้อน แลกเปลี่ยนระหว่างระบบของ หลากหลายความแตกต่างอุณหภูมิ ในบทความนี้ เราจะพิจารณาพลังงานความร้อนเป็นคำพ้องสำหรับ พลังงานภายในซึ่งสามารถเข้าใจได้ว่าเป็นผลรวมของ พลังงานจลนศาสตร์ และ ศักยภาพ จาก อะตอม และโมเลกุลที่ประกอบขึ้นเป็นระบบเทอร์โมไดนามิกส์
ดูยัง:ก่อนดำเนินการต่อ โปรดดูบทสรุปที่น่าทึ่งเกี่ยวกับความร้อน
พลังงานความร้อน
พลังงานความร้อน เป็นผลจาก ผลรวม ให้ พลังงานจลนศาสตร์ และ ศักยภาพ ของอนุภาคที่เป็นส่วนประกอบทั้งหมดของร่างกาย พลังงานความร้อน มันขึ้นอยู่กับโดยตรง ให้ อุณหภูมิแน่นอน ของร่างกายวัดเป็นเคลวิน (K) และยังขึ้นอยู่กับปริมาณของ องศาในเสรีภาพ ของระบบ กล่าวคือ จำนวนทิศทางที่โมเลกุลสามารถเคลื่อนที่ สั่น สั่น หรือแม้แต่หมุนได้

โอ ทฤษฎีบทให้อุปกรณ์ ของพลังงานระบุว่า: ในแต่ละระดับความเป็นอิสระของระบบ พลังงานภายในสามารถคำนวณได้จากผลคูณของจำนวนเต็มของนิพจน์ ½ kบีT โดยที่ Kb คือ ค่าคงที่ในBoltzmann และ T คือ อุณหภูมิ วัดเป็นเคลวิน สูตรที่ใช้ในการคำนวณพลังงานความร้อนของก๊าซโมโนอะตอมในอุดมคติแสดงไว้ด้านล่าง โปรดตรวจสอบ:
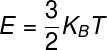
Kบี – ค่าคงที่ Boltzmann (Kบี = 1,38.10-23 ตรม.กก./วินาที² เค)
เนื่องจากพลังงานความร้อนของก๊าซในอุดมคติแสดงโดยสูตรข้างต้นและแสดงถึง พลังงานจลนศาสตร์เฉลี่ย ของระบบเราสามารถเขียนความเท่าเทียมกันต่อไปนี้:
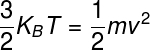
ดูยัง:สรุปแล้วน้ำเป็นสีอะไรครับ?
โดยใช้สูตรข้างต้นก็เป็นไปได้ ประมาณการความเร็วในการแปลเฉลี่ย ของอะตอมที่มีอยู่ใน ก๊าซในบรรยากาศ. โดยคำนึงถึงอุณหภูมิ 25 °C และอะตอมของ ออกซิเจน (M = 16 g/mol) เราพบความเร็วเฉลี่ย 680 m/s หรือ 1525 km/h ซึ่งเป็นความเร็วที่อนุภาคก๊าซในบรรยากาศกระทบเราตลอดเวลา
ในกรณีของก๊าซไดอะตอมมิก แฟกเตอร์ ½k จะถูกเติมลงในนิพจน์ที่ใช้สำหรับแก๊สอะตอมเดี่ยวบีT เนื่องจากการเพิ่มขึ้นของระดับความเป็นอิสระหนึ่งระดับทำให้เกิดนิพจน์ต่อไปนี้:

ให้เป็นไปตาม กฎข้อที่หนึ่งของ อุณหพลศาสตร์, แ พลังงานความร้อน ของระบบสามารถแปลงเป็นพลังงานรูปแบบอื่นได้ เช่น ความร้อน และ งาน. ความร้อน เช่น หมายถึง โอนในพลังงานความร้อน,เฉพาะเนื่องจากความแตกต่างของอุณหภูมิ ระหว่างระบบกับสภาพแวดล้อม ในทางกลับกัน การทำงานเกี่ยวข้องกับการใช้กำลังกับระบบหรือโดยระบบ
ในแง่นี้ งานนี้สามารถใช้ในการเคลื่อนย้ายลูกสูบ เช่นเดียวกับในตู้รถไฟที่ขับเคลื่อนด้วยไอน้ำและใน เครื่องยนต์สันดาปภายในซึ่งให้กำลังแก่ยานยนต์ในปัจจุบันแทบทั้งหมด ด้านล่างนี้ เรานำกฎข้อที่หนึ่งของเทอร์โมไดนามิกส์มาพิจารณา:
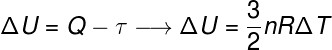
ตามกฎข้อที่ 1 ของอุณหพลศาสตร์ การแปรผันของพลังงานภายในคือความแตกต่างระหว่างงานและความร้อน
มีวิธีอื่นในการคำนวณโมดูลัสพลังงานความร้อนของร่างกายในกรณีของ ก๊าซอุดมคติซึ่งพลังงานศักย์ระหว่างอนุภาคถือเป็นโมฆะ ด้วยเหตุนี้เราจึงแสดงพลังงานภายในเป็นจำนวน ไฝ (n) และจาก ค่าคงที่สากลของก๊าซสมบูรณ์ (R) ตรวจสอบ:
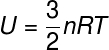
n - จำนวนโมล (โมล)
R – ค่าคงที่สากลของก๊าซสมบูรณ์ (R = 0.082 atm. ลิตร/โมล K หรือ 8.31 จูล/โมล เค)
ยังอยู่ในขอบเขตของก๊าซสมบูรณ์ ซึ่งรวมเอา สมการ clapeyron (PV = nRT) โดยเปิดเผยคำจำกัดความของพลังงาน เป็นไปได้ที่จะได้รับนิพจน์ใหม่ หมายเหตุ:

พี – แรงดัน (Pa)
วี – ปริมาณ (m³)
ดูด้วย:อากาศร้อนขึ้นอากาศเย็นลง แต่ทำไม?
ข้อดีและข้อเสียของพลังงานความร้อน
ทุกวันเราใช้ .จำนวนมาก แหล่งที่มาในพลังงานความร้อน เพื่อผลิตพลังงาน โอ ร่างกายมนุษย์เช่น กินมาก สารอาหาร เพื่อสร้างพลังงานความร้อนที่จำเป็นสำหรับการทำงานของกระบวนการที่สำคัญของเรา ส่วนมากของ ไฟฟ้า ผลิตในโลก ขึ้นอยู่กับความสามารถของเราในการเปลี่ยนพลังงานความร้อนให้เป็นไฟฟ้า
ตรวจสอบวิธีการใช้พลังงานความร้อนเพื่อผลิตไฟฟ้าและข้อดีและข้อเสียหลัก:
ชนิดพืช |
ประโยชน์ |
ข้อเสีย |
โรงงานเทอร์โมนิวเคลียร์ |
ปล่อยก๊าซมลพิษต่ำและมีประสิทธิภาพสูง |
การผลิตกากกัมมันตภาพรังสีและการได้รับรังสี |
โรงไฟฟ้าพลังความร้อนจากถ่านหิน |
การผลิตพลังงานขนาดใหญ่และต้นทุนต่ำ |
การปล่อยมลพิษและก๊าซเรือนกระจก |
โรงไฟฟ้าเทอร์โมอิเล็กทริกที่ใช้ก๊าซธรรมชาติ |
มลพิษน้อยกว่าการเผาไหม้ถ่านหิน |
ค่าใช้จ่ายแตกต่างกันมาก เนื่องจากก๊าซธรรมชาติเป็นอนุพันธ์ของปิโตรเลียม |
โรงไฟฟ้าพลังความร้อนจากชีวมวล |
ต้นทุนการติดตั้งต่ำและการปล่อยก๊าซเรือนกระจกต่ำ |
การตัดไม้ทำลายป่าและการปลูกพืชเชิงเดี่ยวขนาดใหญ่ |
พืชความร้อนใต้พิภพ |
ไม่ก่อให้เกิดมลพิษ |
ค่าติดตั้งและบำรุงรักษาสูง |
ดูด้วย: เรียนรู้ไฮโดรสแตติกทันทีและสำหรับทั้งหมด!
แบบฝึกหัดเกี่ยวกับพลังงานความร้อน
คำถามที่ 1) ก๊าซไดอะตอมมิกในอุดมคติสองโมลมาบรรจบกันที่อุณหภูมิ 127 °C พลังงานความร้อนของก๊าซนี้มีค่าประมาณ:
ข้อมูล: R = 8.31 J/โมล K
ก) 1.5.106 เจ
ข) 1.7.104 เจ
ค) 8.5.103 เจ
ง) 5.3.104 เจ
จ) 8.5.104 เจ
คำติชม: ตัวอักษร B
ความละเอียด:
ลองคำนวณพลังงานของก๊าซโดยใช้นิพจน์ต่อไปนี้ เนื่องจากก๊าซเป็นไดอะตอมมิก ก่อนดำเนินการดังกล่าว จำเป็นต้องแปลงอุณหภูมิจากองศาเซลเซียสเป็นเคลวิน โปรดทราบว่า note การคำนวณ:
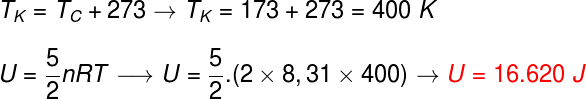
จากการคำนวณ ก๊าซไดอะตอมมิกนี้มีพลังงาน 16,620 J นั่นคือประมาณ 1,7.104 เจหากแสดงเป็นสัญกรณ์วิทยาศาสตร์และใช้กฎการปัดเศษ
คำถามที่ 2) ก๊าซโมโนอะตอมในอุดมคติสามโมลได้รับความร้อนเท่ากับ 5.102 cal และทำงาน 2.102 มะนาวในระหว่างกระบวนการ กำหนดความแปรผันของอุณหภูมิที่ก๊าซนี้ประสบในหน่วยองศาเซลเซียส
ข้อมูล: R = 0.082 atm. ลิตร/โมล K
ก) 214°C
ข) 813°C
ค) 1620 °C
ง) 740 องศาเซลเซียส
จ) 370°C
คำติชม: ตัวอักษร B
ความละเอียด:
ในการแก้แบบฝึกหัดนี้ จำเป็นต้องรวมสูตรที่แตกต่างกันสองสูตรเข้าด้วยกัน คือ กฎข้อที่หนึ่งของ อุณหพลศาสตร์ซึ่งกำหนดรูปแบบพลังงานและสูตรของพลังงานความร้อนของก๊าซโมโนอะตอมในอุดมคติ ดู:
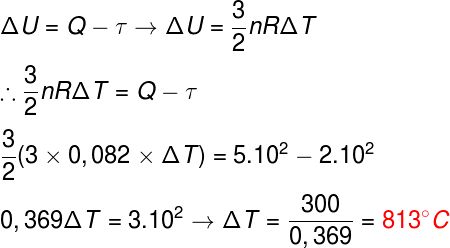
หลังจากที่เราแทนที่ข้อมูลในสูตรแล้ว เราจะพบการเปลี่ยนแปลง 813 °C ดังนั้นทางเลือกที่ถูกต้องคือตัวอักษร B
By Me. ราฟาเอล เฮเลอร์บร็อก
ที่มา: โรงเรียนบราซิล - https://brasilescola.uol.com.br/fisica/energia-termica.htm

