ที่ สูตรเคมี เป็นตัวแทนที่ใช้ในการระบุว่าองค์ประกอบทางเคมีใดเป็นส่วนหนึ่งขององค์ประกอบของสารและยังเป็นตัวแทนของประเภทของปฏิสัมพันธ์ระหว่างอะตอมที่มีส่วนร่วม
ผ่านการวิเคราะห์ของ สูตรของสารเคมี เราสามารถกำหนดลักษณะของพันธะเคมี (ไอออนิก, โควาเลนต์ หรือโลหะ) ที่ก่อตัวขึ้น ตลอดจนพฤติกรรมทางเคมีกายภาพของมัน คุณสมบัติบางอย่างที่เกี่ยวข้องกับพฤติกรรมทางเคมีกายภาพของสารคือ:
ความสามารถในการละลาย
จุดหลอมเหลว
จุดเดือด
ปฏิกิริยา
ตอนนี้รู้ประเภทของสารประกอบที่ประกอบเป็นสารเคมีและสูตรที่เป็นตัวแทนของพวกมัน
ประเภทของสารประกอบ
ก) สารประกอบไอออนิก
สารประกอบไอออนิกเป็นสารเคมีทั้งหมดที่เกิดขึ้นจากพันธะไอออนิกระหว่างอะตอม กล่าวคือ ในสารประกอบเหล่านี้ มีอะตอมที่สูญเสียและอะตอมที่ได้รับอิเล็กตรอน การรวมกันขององค์ประกอบทางเคมีที่สร้างสารประกอบประเภทนี้สามารถ:
โลหะ ด้วยอะเมทัล
โลหะที่มีไฮโดรเจน
b) สารประกอบโควาเลนต์
สารประกอบโควาเลนต์เป็นสารเคมีทั้งหมดที่เกิดขึ้นจากพันธะโควาเลนต์ระหว่างอะตอม กล่าวคือ ในสารประกอบเหล่านี้ มีอะตอมที่ใช้อิเล็กตรอนร่วมกัน การรวมกันขององค์ประกอบทางเคมีที่สร้างสารประกอบประเภทนี้สามารถ:
อะเมทัลกับอเมทัล
อเมทัลกับไฮโดรเจน
ไฮโดรเจนกับไฮโดรเจน
ค) สารประกอบโลหะ
สารประกอบโลหะเป็นสารเคมีทั้งหมดที่เกิดขึ้นจากอะตอมของธาตุโลหะเดี่ยว ในสารประกอบเหล่านี้ อะตอมใช้อิเล็กตรอนร่วมกันเท่านั้น
สูตรสำหรับสารประกอบไอออนิก
ก) สูตรไอออน
สูตรไอออนระบุจำนวนอะตอมที่ก่อรูปหน่วยไอออนิกของสารประกอบ เช่นในกรณีของคลอไรด์ ของโซเดียมซึ่งมีสูตรไอออนคือ NaCl ในสูตร เราระบุการมีอยู่ของโซเดียมอะตอมและอะตอมของ คลอรีน.
ในการสร้างสูตรไอออน เพียงแค่ตัดประจุของไอออนแต่ละตัวที่ประกอบเป็นสารประกอบไอออนิก สำหรับอัล cation+3 และประจุลบ O-2ตัวอย่างเช่น เมื่อเราตัดประจุและไม่สนใจสัญญาณ เรามีสูตรไอออนต่อไปนี้:
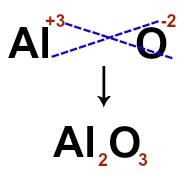
ข) สูตรอิเล็กทรอนิกส์
สูตรอิเล็กทรอนิกส์ใช้เพื่อแสดงถึงการสูญเสียและการเพิ่มของอิเล็กตรอนของอะตอมที่เกี่ยวข้องกับการก่อตัวของสารประกอบ รอบๆ ตัวย่อของแต่ละธาตุ เรามีอิเลคตรอนแต่ละตัวของ ชั้นวาเลนซ์.
ในกรณีของโซเดียมคลอไรด์ (NaCl) เรามีวาเลนซ์อิเล็กตรอนเพียงตัวเดียวใน Na (เพราะมาจากตระกูล IA) และใน Cl เรามีวาเลนซ์อิเล็กตรอนเจ็ดตัว (เนื่องจากมาจากตระกูล VIIA)
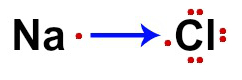
สูตรอิเล็กทรอนิกส์ NaCl
การเพิ่มของอิเล็กตรอนโดย Cl (อโลหะ) และการสูญเสียอิเล็กตรอนโดย Na (อโลหะ) จะแสดงด้วยลูกศร ให้เป็นไปตาม ทฤษฎีออคเต็ต, Na เสียอิเล็กตรอนไปหนึ่งตัวเพราะมีเพียงตัวเดียว และ Cl ได้ 1 ตัวเพื่อให้ครบแปดวาเลนซ์อิเล็กตรอน
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
สำหรับสารประกอบโควาเลนต์
ก) สูตรโมเลกุล
สูตรโมเลกุลใช้เพื่อแสดงสารโควาเลนต์ในรูปแบบย่อ สูตรโมเลกุลของน้ำ คือ H2ตัวอย่างเช่น O มีไฮโดรเจนสองอะตอมและออกซิเจนหนึ่งอะตอม
สูตรโมเลกุลของสารประกอบโควาเลนต์ไม่เหมือนกับสูตรไอออนของสารประกอบไอออนิก ความเรียบง่าย เนื่องจากปริมาณอะตอมของธาตุเดียวกันจำนวนต่างกันจะเกิดสารที่ต่างกัน เช่น น้ำ (ฮ2O) และไฮโดรเจนเปอร์ออกไซด์ (H2โอ2).
เป็นเรื่องธรรมดามากในการออกกำลังกาย สูตรโมเลกุล:
ให้โดยการออกกำลังกายเอง;
ถูกกำหนดโดยการคำนวณ
ถูกกำหนดโดยการนับแต่ละองค์ประกอบจากสูตรโครงสร้าง
กำหนดจากชื่อสาร
ข) สูตรโครงสร้าง
สูตรโครงสร้างของสารโควาเลนต์ใช้แทนจำนวนพันธะที่อะตอมแต่ละอะตอมสร้างขึ้นในโมเลกุล ลิงค์ที่ใช้ในสูตรโครงสร้างคือ:
ลิงก์เดี่ยว: แสดงด้วยขีดกลาง (─) ระบุลิงก์เดียว
พันธะคู่: แทนด้วยขีดกลางสองอัน (=) หมายถึงพันธะสองอัน;
พันธะสาม: แสดงด้วยขีดกลางสามขีด (≡) ระบุสามพันธะ;
ลิงค์ข้อมูล: แสดงด้วยลูกศร (→) หมายถึงการเชื่อมต่อเดียว
ควรแสดงสูตรโครงสร้างของสารประกอบโควาเลนต์เมื่อใดก็ตามที่เป็นไปได้ ตามเรขาคณิตของโมเลกุลที่เป็นปัญหา ดูการแสดงสูตรโครงสร้างของแอมโมเนียซึ่งมีรูปเรขาคณิตเสี้ยม:
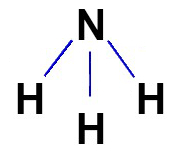
ค) สูตรอิเล็กทรอนิกส์
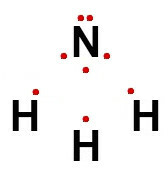
สูตรอิเล็กทรอนิกส์สำหรับสารประกอบโควาเลนต์แสดงให้เห็นถึงการแบ่งปันอิเล็กตรอนระหว่างอะตอมที่ประกอบเป็นโมเลกุล แทนที่จะใช้ขีดกลางในสูตรโครงสร้าง เรามีการใช้ทรงกลมเพื่อเป็นตัวแทนของอิเล็กตรอนที่ใช้ร่วมกันระหว่างอะตอม ดู:
พันธะเดี่ยว: แบ่งอิเล็กตรอนสองตัว (หนึ่งตัวจากแต่ละอะตอมที่เกี่ยวข้อง);
พันธะคู่: แบ่งอิเล็กตรอนสี่ตัว (สองอะตอมจากแต่ละอะตอมที่เกี่ยวข้อง);
พันธะสาม: ใช้อิเล็กตรอนร่วมกัน 6 ตัว (สามจากแต่ละอะตอมที่เกี่ยวข้อง);
Dative bond: การแบ่งปันอิเล็กตรอนสองตัว (ทั้งคู่มาจากอะตอมเดียวระหว่างผู้ที่เกี่ยวข้อง)
ดังนั้น สำหรับแอมโมเนียซึ่งมีสูตรโครงสร้างแสดงไว้ข้างต้น สูตรอิเล็กทรอนิกส์ของแอมโมเนียคือ:
สำหรับสารประกอบโลหะ
สารประกอบโลหะเนื่องจากเกิดขึ้นจากอะตอมของโลหะชนิดเดียวมีสูตรทางเคมีเป็นตัวย่อขององค์ประกอบทางเคมี:
สารทองแดง: Cu
สารทองคำ: Au
ธาตุเหล็ก: Fe
By Me. Diogo Lopes Dias
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "สูตรสารเคมี"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/formulas-substancias-quimicas.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.