THE พลังงานผูกพัน มีส่วนร่วม ในช่วงพักหรือในการฝึก พันธะระหว่างอะตอมของโมเลกุลตั้งแต่หนึ่งอะตอมขึ้นไป ตัวอย่างเช่น โมเลกุลของก๊าซไฮโดรเจนมีพันธะเดี่ยว (ซิกมา) ระหว่างอะตอมที่เกี่ยวข้อง:

สูตรโครงสร้างก๊าซไฮโดรเจน
เพื่อให้โมเลกุลนี้กำเนิดขึ้น พันธะเดี่ยวระหว่างอะตอมของมันจึงถูกสร้างขึ้น เมื่อโมเลกุลนี้มีส่วนร่วมในปฏิกิริยาเคมีกับก๊าซคลอรีน (Cl2) ตัวอย่างเช่น สำหรับการก่อตัวของกรดไฮโดรคลอริก (HCl) พันธะเดี่ยวมีอยู่ใน H2 และใน Cl2 จะต้องถูกทำลายด้วยการเกิดพันธะเดี่ยวใน HCl
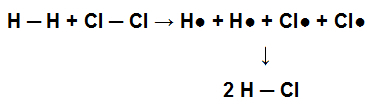
การแสดงการแตกของพันธะเดี่ยวในรีเอเจนต์และการเกิดพันธะเดี่ยวในผลิตภัณฑ์
อะตอมประสานกันเพื่อบรรลุ เสถียรภาพทางอิเล็กทรอนิกส์นั่นคือพวกเขาย้ายจากสถานการณ์พลังงานที่สูงขึ้นไปเป็นสถานการณ์พลังงานที่ต่ำกว่า ดังนั้น เราสามารถพูดได้ว่าเมื่อพันธะระหว่างอะตอมเกิดขึ้น พลังงานจะถูกปล่อยออกมา ดังนั้นการสลายจึงขึ้นอยู่กับการดูดกลืนพลังงาน
ถ้าเราเข้าใจว่า understand เลิก (การแตก) ของพันธะเคมีเกิดขึ้นเมื่อมันถูกจ่ายให้ ปริมาณพลังงาน (xKcal)เราสรุปได้ว่านี่คือกระบวนการ ดูดความร้อน. ในทางตรงกันข้าม การสร้างความผูกพันจะเกี่ยวข้องกับ ปล่อย ให้ ปริมาณพลังงานเท่ากัน (-xkcal)จึงเป็นกระบวนการ คายความร้อน.
ชอบ ปฏิกิริยาเคมีแบ่งออกเป็น ดูดความร้อนหรือคายความร้อนเราสามารถใช้ความรู้เกี่ยวกับพลังงานยึดเหนี่ยวของโมเลกุลของสารตั้งต้นและผลิตภัณฑ์เพื่อกำหนดการเปลี่ยนแปลงของพลังงาน (ΔH) ของกระบวนการทางเคมีแล้วจัดประเภทได้
ตัวอย่างเช่น ดูสมการด้านล่าง:
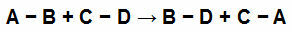
พันธะเคมีในผู้เข้าร่วมในสมการเคมี
เรามีลิงค์ง่ายๆ ในผู้เข้าร่วมปฏิกิริยาแต่ละคน มีค่าดังต่อไปนี้:
[A-B] = 50 กิโลแคลอรี
[ซีดี] = 100 กิโลแคลอรี
[บี-ดี] = 80 กิโลแคลอรี
[บี.ซี.] = 230 กิโลแคลอรี
ด้วยค่าข้างต้น เราสามารถคำนวณพลังงานที่เกี่ยวข้องกับการสลายพันธะของสารตั้งต้นและสร้างพันธะของผลิตภัณฑ์ได้ดังนี้
ในรีเอเจนต์
50 Kcal เพื่อทำลายพันธะ AB และ 100 Kcal เพื่อทำลายพันธะซีดีนั่นคือในรีเอเจนต์ 150 Kcal จะใช้ในการทำลายพันธะ
ในผลิตภัณฑ์
80 Kcal เพื่อสร้างพันธะ BD และ 230 Kcal เพื่อสร้างพันธะ ACนั่นคือ 310 Kcal จะถูกปล่อยออกมาในผลิตภัณฑ์ในรูปแบบของพันธะ
ด้วยค่าพลังงานที่เกี่ยวข้องกับสารตั้งต้นและผลิตภัณฑ์ จึงสามารถทราบได้ว่าปฏิกิริยาดูดกลืนหรือ ปล่อยพลังงานมากขึ้นเพียงแค่ลบพลังงานที่ใช้ในการหยุดชะงักออกจากพลังงานที่ปล่อยออกมาใน รูปแบบ:
ΔH = พลังงานของรีเอเจนต์ - พลังงานของผลิตภัณฑ์
ΔH = 230 - 310
ΔH = -80 กิโลแคลอรี
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
เนื่องจากปฏิกิริยามีการปลดปล่อยพลังงานมากกว่าการดูดกลืน ลบ ΔH จึงเป็นแบบคายความร้อน
บันทึก: หากค่าสัมประสิทธิ์ปริมาณสัมพันธ์ของผู้เข้าร่วมแตกต่างจาก 1 เราต้องคูณค่าพลังงานของการเชื่อมต่อด้วยสัมประสิทธิ์ ตัวอย่างเช่น
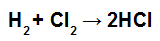
สมการการก่อตัวของ HCl
เนื่องจากสัมประสิทธิ์ของ HCl เป็น 2 เราจึงต้องคูณค่าของการรวมของ HCl ด้วย 2
ตอนนี้ให้ทำตามมติของการออกกำลังกายเกี่ยวกับพลังงานผูกมัดในปฏิกิริยาเคมี:
ตัวอย่าง: รับพลังงานยึดเหนี่ยวต่อไปนี้ในหน่วยกิโลจูลต่อโมลของพันธะ (ค่าสัมบูรณ์):
H − H = 436
ยังไม่มีข้อความ ≡ ยังไม่มีข้อความ = 945.6
ยังไม่มีข้อความ - H = 391
คำนวณความร้อน (เป็นกิโลจูลต่อโมลของ NH3(ก.)) เกี่ยวข้องกับปฏิกิริยาที่แสดงโดย:
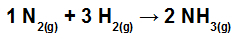
พันธะเคมีในปฏิกิริยาการเกิด NH3
ความละเอียด:
ขั้นตอนแรกในการแก้แบบฝึกหัดนี้คือการเขียนสมการใหม่ที่แสดงพันธะเคมีที่มีอยู่ในแต่ละโมเลกุล:
ไม่มีน2: เรามีพันธะสามตัว (เพราะว่า N ตระกูลไนโตรเจน ต้องสร้างพันธะสามอันเพราะมีอิเล็กตรอนห้าตัวในเปลือกเวเลนซ์)
ที่ H2: เรามีพันธะเดี่ยว (เพราะ H ต้องสร้างพันธะเดียวเพราะมีอิเล็กตรอนเพียงตัวเดียวในเปลือกเวเลนซ์)
ใน NH3: เรามีพันธะธรรมดาสามพันธะ (เพราะ H แต่ละตัวต้องการพันธะ และ N คือพันธะสามตัว)
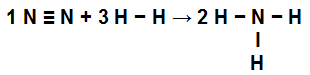
สมการแสดงการเชื่อมโยงในรูปแบบ NH3
เนื่องจากแบบฝึกหัดได้ระบุค่าสำหรับการผูกมัดแต่ละครั้ง ขั้นตอนแรกคือการกำหนดพลังงานการผูกมัดที่เกี่ยวข้องกับผู้เข้าร่วมแต่ละคน:
- ถึง N2
เรามี 1 โมล ใน นู๋2ในสมการ และเพื่อตัดการเชื่อมต่อของคุณ เราต้องการ 945.4 KJ ดังนั้น:
1.945,4 = 945.4 KJ
- สู่ H2
เรามี 3 โมล ใน โฮ2ในสมการ และเพื่อตัดการเชื่อมต่อของคุณ เราต้องการ 436 KJ ดังนั้น:
3.346 = 1038 KJ K
- ถึง NH3
เรามี 2 โมลของ NH3ในสมการแต่มีพันธะ N-H สามเท่า ดังนั้นลองคูณปริมาณพลังงานที่เกี่ยวข้องเพื่อสร้างพันธะนั้นด้วย 2 และ 3:
2.3.391 = 2346 KJ
สุดท้าย เราสามารถระบุความร้อนที่เกี่ยวข้องกับปฏิกิริยาได้โดยการลบพลังงานที่ใช้ในการแยกสารตั้งต้นออกจากพลังงานที่ปล่อยออกมาในการก่อตัวของผลิตภัณฑ์:
ΔH = พลังงานในสารตั้งต้น - พลังงานในผลิตภัณฑ์
ΔH = (945.4 + 1038) - 2346
ΔH = 1983.4 - 2346
ΔH = - 362.6 KJ ต่อโมลของ NH3(ก.)
เนื่องจากความแปรผันเป็นลบ หมายความว่าพลังงานที่ปล่อยออกมาในการก่อตัวของพันธะในผลิตภัณฑ์นั้นมากกว่าพลังงานที่ดูดซับในการทำลายพันธะของสารตั้งต้น ดังนั้น ปฏิกิริยาคายความร้อน.
By Me. Diogo Lopes Dias