เลขอะตอมซึ่งแสดงโดยตัวอักษร Z สอดคล้องกับปริมาณโปรตอนที่มีอยู่ในนิวเคลียสของอะตอมขององค์ประกอบทางเคมีที่กำหนด ตัวอย่างเช่น เลขอะตอมของไฮโดรเจนคือ 1 ซึ่งหมายความว่ามีโปรตอนเพียง 1 ตัวในนิวเคลียสของอะตอม
เลขอะตอมมักจะปรากฏถัดจากสัญลักษณ์ตัวห้อยขององค์ประกอบทางเคมี (ที่มุมล่าง) ทางด้านซ้าย ตัวอย่าง: 1เอช
ในสถานะพื้นดิน เลขอะตอมจะเท่ากับจำนวนอิเล็กตรอน เนื่องจากในสถานะนี้ธาตุคือ เป็นกลาง ดังนั้น ปริมาณประจุบวก (โปรตอน) ต้องเท่ากับปริมาณประจุลบ (อิเล็กตรอน) ของ อะตอม.
เลขอะตอมมีความสำคัญเพราะ เป็นผู้กำหนดลักษณะและคุณสมบัติหลักขององค์ประกอบตลอดจนพฤติกรรมและตำแหน่งของธาตุในตารางธาตุ ธาตุต่างๆ ถูกระบุไว้ในตารางธาตุโดยเรียงจากน้อยไปมากของเลขอะตอม ซึ่งมักจะปรากฏเหนือธาตุดังที่แสดงด้านล่าง โปรดทราบว่าองค์ประกอบแรกคือไฮโดรเจน H (Z = 1) ตามด้วยฮีเลียม He (Z = 2) จากนั้นลิเธียม Li (Z = 3) เป็นต้น
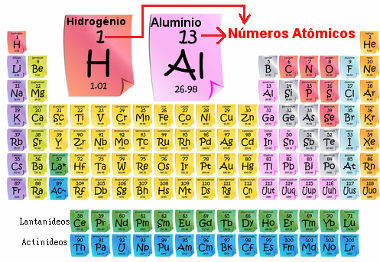
เลขอะตอมของธาตุในตารางธาตุ
เรายังสร้างแนวคิดเกี่ยวกับองค์ประกอบทางเคมีว่ากำลังเป็นอยู่ได้ “ชุดของอะตอมที่มีเลขอะตอมเท่ากัน” ตัวอย่างเช่น เมื่อเราพูดถึงองค์ประกอบทางเคมี ออกซิเจน เรากำลังพูดถึงอะตอมที่มีเลขอะตอม 8 ด้านล่างมีอะตอมขององค์ประกอบทางเคมีจากช่วงที่ 1 และ 2 ของตารางธาตุโดยเรียงจากน้อยไปมากของเลขอะตอม:

องค์ประกอบทางเคมีจากช่วงที่ 1 และ 2 ของตารางธาตุโดยเรียงจากน้อยไปมากของเลขอะตอม
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
เลขอะตอมถูกกำหนดโดยนักฟิสิกส์ชาวอังกฤษ Henry Gwyn Jeffreys Moseley (1887-1915) และเมื่อทำการทดลองเกี่ยวกับการทิ้งระเบิดขององค์ประกอบต่างๆ นักเคมีที่ใช้รังสีเอกซ์ เขาสังเกตว่ารากที่สองของความถี่ของรังสีเอกซ์ที่เกิดจากการปล่อยนิวเคลียสของอะตอมเป็นสัดส่วนโดยตรงกับเลขอะตอมของธาตุในตาราง เป็นระยะ ด้วยเหตุนี้ เขาจึงสรุปว่าเลขอะตอมสัมพันธ์กับคุณสมบัติของอะตอม เพราะมันแทนจำนวนประจุบวกในนิวเคลียสของแต่ละอะตอม
พันธะเคมีไม่ส่งผลต่อเลขอะตอมของอะตอม เนื่องจากเกี่ยวข้องกับอิเล็กตรอนที่อยู่ในอิเล็กโตรสเฟียร์เท่านั้น อย่างไรก็ตาม ปฏิกิริยานิวเคลียร์เกี่ยวข้องกับนิวเคลียสของอะตอมและด้วยเหตุนี้จึงรวมเลขอะตอมไว้ด้วย
ตัวอย่างเช่น เมื่ออนุภาค (ส่วนใหญ่เป็นนิวตรอนปานกลาง) ถูกทิ้งระเบิดลงบนนิวเคลียสอะตอมที่หนักและไม่เสถียร นิวเคลียสนั้นจะเป็น แตกและทำให้เกิดนิวเคลียสของอะตอมที่เล็กกว่าสองตัว นั่นคือ ด้วยจำนวนโปรตอนและนิวตรอนที่น้อยกว่า ปล่อยจำนวนมหาศาลของ พลังงาน.
ในทางกลับกัน ปฏิกิริยานิวเคลียร์ฟิวชันเป็นกระบวนการที่ตรงกันข้าม เมื่อนิวเคลียสขนาดเล็กและเบาสองนิวเคลียสมารวมกัน ทำให้เกิดนิวเคลียสที่ใหญ่กว่าและเสถียรกว่า ปล่อยพลังงานออกมาในปริมาณที่มากขึ้น
ดังนั้น เมื่อใดก็ตามที่เกิดปฏิกิริยานิวเคลียร์เหล่านี้ องค์ประกอบทางเคมีใหม่จะเกิดขึ้น เนื่องจากเลขอะตอมของธาตุตั้งต้นจะแตกต่างจากเลขอะตอมของธาตุสุดท้าย ตัวอย่างเช่น ดูด้านล่างที่ฟิชชันของยูเรเนียม-235 ที่มีเลขอะตอม 92 ทำให้เกิดแบเรียม (Z = 56), คริปทอน (Z = 36) และนิวตรอนสามตัว:

ปฏิกิริยานิวเคลียร์ฟิชชันของยูเรเนียม-235
โดย เจนนิเฟอร์ โฟกาซา
จบเคมี
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
โฟกาซ่า, เจนนิเฟอร์ โรชา วาร์กัส "เลขอะตอมคืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-atomico.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.