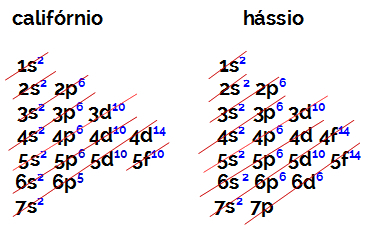
ความแตกแยกของ ฐาน มันคือ กระบวนการทางกายภาพ ที่เกิดขึ้นกับสารอนินทรีย์กลุ่มสำคัญนี้เมื่อละลายในน้ำหรือ เมื่อผ่านกระบวนการหลอมรวม (ผ่านจากสถานะของแข็งไปยังสถานะของเหลวผ่าน ความร้อน)
โดยทั่วไปปรากฏการณ์ของ ความแตกแยกของฐาน มันคือการปล่อยของไพเพอร์และแอนไอออนที่สร้าง สารประกอบไอออนิกซึ่งในกรณีนี้คือฐาน ดังนั้น ในช่วง during ความแตกแยกของฐาน, การเปิดตัวของ ไอออน ที่มีอยู่แล้วในสารประกอบ กล่าวคือ ไม่มีไอออนใหม่เกิดขึ้น
ฐานประกอบด้วยโลหะใด ๆ (X) ซึ่งเป็นไอออนบวกของสารประกอบหรือโดยไอออนบวกของแอมโมเนียม (กลุ่ม NH4+) ถูกผูกมัดกับไฮดรอกไซด์แอนไอออน (แสดงโดยหมู่ OH) ดังที่แสดงด้านล่าง:
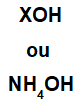
การแสดงทั่วไปของสูตรฐาน
รูปแบบของ เป็นตัวแทนของ ความแตกแยกของฐาน มันทำผ่านสมการซึ่งในสารตั้งต้น เรามีฐาน และในผลิตภัณฑ์ เรามีไอออน (ไพเพอร์และแอนไอออน) สิ่งที่ทำให้แตกต่างคือความแตกแยกเกิดขึ้นได้อย่างไร:
การละลายของเบสในน้ำ:
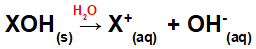
สมการแทนการแตกตัวของเบสในตัวกลางที่เป็นน้ำ
การแยกตัวจากการควบรวมฐาน:
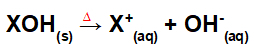
สมการที่แสดงถึงความแตกแยกของฐานโดยกระบวนการหลอมรวม
จากการวิเคราะห์สมการทั่วไปข้างต้น เรายืนยันว่าในสมการทั้งหมดนั้น เราจะมีเบส ไอออนบวก (ซึ่งเป็นโลหะหรือกลุ่ม NH เสมอ)
4+) และประจุลบ (OH-). แต่พวกเขาทั้งหมดเป็นเช่นนั้นหรือไม่? ไม่มีความแตกต่างระหว่างพวกเขา? สำหรับคำถามแรกคำตอบคือไม่ และสำหรับคำถามที่สองคำตอบคือใช่อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
เมื่อเราดำเนินการ การแยกตัวออกจากฐานการวิเคราะห์สูตรพื้นฐานก่อนเป็นพื้นฐานเพราะจากนั้นเราสามารถกำหนดภาระของ ไอออนบวกและปริมาณโมลของไฮดรอกไซด์แอนไอออน เนื่องจากปริมาณโมลของไอออนบวกเป็นค่ามาตรฐาน (เสมอ 1 โมล)
เป็นที่น่าจดจำว่าปริมาณของกลุ่ม OH ที่มีอยู่ในสูตรฐานจะเป็นตัวกำหนดประจุของไอออนบวกและปริมาณในโมลของไฮดรอกไซด์แอนไอออนในการแยกตัวของเบส
มาดูตัวอย่างอะลูมิเนียมไฮดรอกไซด์ [Al(OH)3] และทองคำไฮดรอกไซด์ (AuOH) ในสูตรฐานอะลูมิเนียม มีหมู่ OH สามกลุ่ม และในสูตรฐานทอง มีกลุ่ม OH เพียงกลุ่มเดียว ดังนั้น ในการแยกตัวของฐานเหล่านี้ เรามี:
การแยกตัวของอัล (OH)3:
เนื่องจากฐานนี้มีหมู่ OH สามกลุ่มในสูตร ประจุบนไอออนบวกจะเป็น +3 และปริมาณในโมลของแอนไอออนจะเท่ากับ 3 โมล ดังที่เราเห็นในสมการต่อไปนี้:
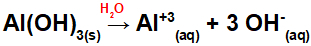
สมการการแตกตัวของฐานอะลูมิเนียมในตัวกลางที่เป็นน้ำ
การแยกตัวออกจาก AuOH:
เนื่องจากฐานนี้มีหมู่ OH ในสูตร ประจุบนไอออนบวกจะเป็น +1 และปริมาณในโมลของแอนไอออนจะเท่ากับ 1 โมล ดังที่เราเห็นในสมการต่อไปนี้:
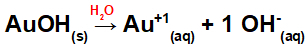
สมการการแยกฐานด้วยทองคำในตัวกลางที่เป็นน้ำ
By Me. Diogo Lopes Dias
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "ความแตกแยกฐานคืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.
เคมี

การแยกตัวและการแตกตัวเป็นไอออน, Volta นักวิทยาศาสตร์ชาวอิตาลี, กระแสไฟฟ้า, นักเคมีกายภาพชาวสวีเดน Svant August Arrhenius, ทฤษฎีของ อาร์เรเนียส, ไอออนบวก, ไพเพอร์, ไอออนลบ, แอนไอออน, โซดาไฟ, เกลือแกง, โมเลกุลมีขั้ว, การแยกตัวออกจากกัน อิออน,