พันธะโควาเลนต์สามารถเกิดขึ้นได้ในรูปแบบโมเลกุลหรือเดทีฟและโคออร์ดิเนต
พันธะโควาเลนต์โมเลกุล
ในพันธะนี้ อะตอมจะเชื่อมต่อกันเนื่องจากการแบ่งปันอิเล็กตรอน จากนั้นคู่อิเล็กทรอนิกส์ที่ระบุโดยวงกลมจะปรากฏขึ้น:
พันธะโควาเลนต์ระดับโมเลกุลของคลอรีน (Cl) สองอะตอม
คู่อิเล็กทรอนิกส์แต่ละคู่ที่เกิดขึ้นพร้อมกันนั้นเป็นของสองอะตอม โมเลกุลเป็นโครงสร้างที่เป็นกลางทางไฟฟ้าเพราะไม่มีการได้รับหรือสูญเสียอิเล็กตรอน มีเพียงการแบ่งปันเท่านั้น
น้ำเป็นสารประกอบโมเลกุลที่ประกอบด้วยไฮโดรเจนสองอะตอม (H2) และออกซิเจนหนึ่งตัว (O)
พันธะโควาเลนต์และประสาน
พันธะนี้เป็นไปตามทฤษฎีออคเต็ต: อะตอมรวมตัวกันพยายามรับอิเล็กตรอนแปดตัวในเปลือกเวเลนซ์ นั่นคือการกำหนดค่าทางอิเล็กทรอนิกส์ของก๊าซมีตระกูล
ดังนั้นอะตอมที่มีความเสถียรทางอิเล็กทรอนิกส์แล้วจึงรวมตัวกับอีกอะตอมที่ต้องการอิเล็กตรอนเพื่อทำให้เปลือกเวเลนซ์สมบูรณ์ ตัวอย่างของพันธะนี้คือเมื่ออะตอมของกำมะถันจับกับออกซิเจนสองอะตอมเพื่อสร้างซัลเฟอร์ไดออกไซด์ (SO2).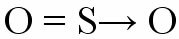
อะตอมของกำมะถัน (S) ได้รับออกเตตด้วยการก่อตัวของพันธะคู่กับออกซิเจนที่อยู่ทางด้านซ้าย (พันธะประสาน) แต่ในขณะเดียวกัน ออกซิเจนที่อยู่ทางด้านขวาก็ต้องการอิเล็กตรอนเพื่อทำให้สมบูรณ์ ออกเตต จากนั้นพันธะโควาเลนต์ dative จะแสดงด้วยเวกเตอร์ขนาดเล็ก (ลูกศร) ลูกศรแสดงว่า that
มาดูการแบ่งปันอิเล็กตรอนในการก่อตัวของสารประกอบซัลเฟอร์ไตรออกไซด์ (SO)3).
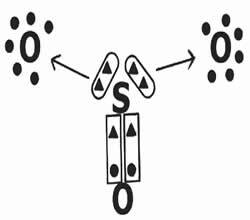
สังเกตว่าธาตุกลาง (กำมะถัน) สร้างพันธะคู่ (ประสานกัน) กับออกซิเจนตัวใดตัวหนึ่ง ทำให้เกิดความเสถียรทางอิเล็กทรอนิกส์ (อิเล็กตรอนแปดตัวในเปลือกเวเลนซ์) ในทางกลับกัน มันบริจาคอิเล็กตรอนสองคู่ให้กับอ็อกซิเจน (พันธะเดิมที่ระบุโดยลูกศร →) เพื่อพยายามทำให้ออคเต็ตสมบูรณ์
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
โดย Liria Alves
จบเคมี
ดูเพิ่มเติม!
การเชื่อมต่อโลหะ
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
ซูซ่า, ลิเรีย อัลเวส เดอ "พันธะโควาเลนต์"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/quimica/ligacao-covalente.htm. เข้าถึงเมื่อ 27 มิถุนายน 2021.