เกลือคู่ เป็นชื่อที่กำหนดให้หนึ่งในประเภทที่ เกลืออนินทรีย์ สามารถรับได้ การจำแนกประเภทอื่นๆ ได้แก่ แบบง่าย, สารส้ม, ไฮดรอกซิเลต, เติมไฮโดรเจน และชุ่มชื้น เพื่อให้มีลักษณะเป็นเกลือสองเท่า เกลืออนินทรีย์ต้องมีหนึ่งในชุดค่าผสมที่อธิบายไว้ด้านล่าง:
ไอออนบวก (Y) และแอนไอออนสองตัว (X และ W) และแสดงโดยสูตรต่อไปนี้:
YXW
แอนไอออน (X) และสองไอออนบวกใดๆ (Y และ Z) และแสดงโดยสูตรต่อไปนี้:
YZX
บันทึก: เกลือเหล่านี้เกิดขึ้นเมื่อ a ปฏิกิริยาการวางตัวเป็นกลาง จะดำเนินการระหว่างสอง ฐาน แตกต่างและเป็นหนึ่ง กรดหรือระหว่างกรดที่ต่างกันสองชนิดกับเบส
กฎการตั้งชื่อเกลือสองเท่า
ในการตั้งชื่อ a เกลือคู่จำเป็นต้องรู้รัฐธรรมนูญก่อนเพราะสำหรับเกลือคู่แต่ละประเภทมีกฎการตั้งชื่อเฉพาะดังที่แสดงด้านล่าง:
ก) กฎการตั้งชื่อสำหรับเกลือสองเท่าที่มีสองไพเพอร์
เมื่อหนึ่ง เกลือคู่ มีสองไพเพอร์ เราต้องใช้กฎต่อไปนี้:

กฎการตั้งชื่อที่ใช้สำหรับเกลือสองเท่าที่มีสองไพเพอร์
ต่อไปนี้คือตัวอย่างการใช้กฎการตั้งชื่อนี้สองตัวอย่าง:
ตัวอย่างที่ 1: ไลน์4ส
เกลือนี้ประกอบด้วย:
ประจุลบ: ซัลไฟด์ (S-2);
ไอออนบวกด้วยไฟฟ้าเพิ่มเติม: ลิเธียม (Li+1);
ประจุบวกด้วยไฟฟ้าน้อย: แอมโมเนียม (NH4+1).
ดังนั้นชื่อของมันก็คือลิเธียม (สองเท่า) แอมโมเนียมซัลไฟด์
ตัวอย่างที่ 2: RbCaBO3
เกลือนี้ประกอบด้วย:
ประจุลบ: borate (BO3-3);
ไอออนบวกด้วยไฟฟ้าเพิ่มเติม: รูบิเดียม (Rb+1);
ประจุบวกด้วยไฟฟ้าน้อย: แคลเซียม (Ca+2).
ดังนั้น ชื่อของมันคือบอเรต (สองเท่า) ของรูบิเดียมและแคลเซียม
b) กฎการตั้งชื่อสำหรับเกลือสองเท่าที่มีประจุลบสองตัว two
เมื่อหนึ่ง เกลือคู่ มีสองแอนไอออน เราต้องใช้กฎต่อไปนี้:
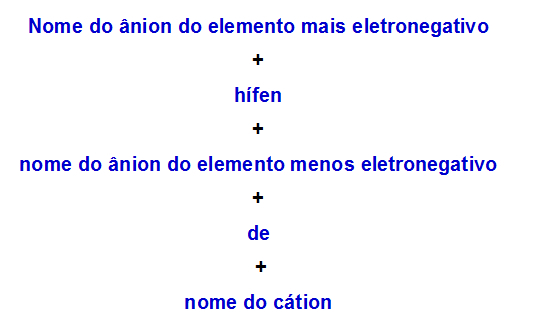
กฎการตั้งชื่อที่ใช้สำหรับเกลือสองเท่าที่มีประจุลบสองตัว
อย่าเพิ่งหยุด... มีมากขึ้นหลังจากโฆษณา ;)
ต่อไปนี้คือตัวอย่างสองตัวอย่างในการใช้กฎนี้:
ตัวอย่างที่ 1: MgFI
เกลือนี้ประกอบด้วย:
ไอออนบวก: แมกนีเซียม (Mg+2);
แอนไอออนที่มีไฟฟ้ามากที่สุด: ฟลูออไรด์ (F-1);
ประจุลบที่มีประจุไฟฟ้าน้อย: ไอโอไดด์ (I-1).
ดังนั้นชื่อของมันก็คือแมกนีเซียมฟลูออไรด์-ไอโอไดด์
ตัวอย่างที่ 2: ZnNO2br
เกลือนี้ประกอบด้วย:
ไอออนบวก: สังกะสี (Zn+2);
ไอออนประจุลบเพิ่มเติม: ไนไตรท์ (NO2-1);
ประจุลบที่มีประจุไฟฟ้าน้อย: โบรไมด์ (Br-1).
ดังนั้นชื่อของมันก็คือซิงค์ไนไตรท์โบรไมด์
การประกอบสูตรของเกลือคู่จากการตั้งชื่อของมัน
ก) สำหรับเกลือสองเท่าที่มีสองไพเพอร์
การสร้างสูตรของ เกลือคู่ ขึ้นอยู่กับการรู้ชื่อของมัน ซึ่งเป็นมาตรฐานเช่นเดียวกับเกลือทั้งหมด นั่นคือ ประจุบวกก่อนแล้วจึงตามด้วยประจุลบ เนื่องจากเกลือคู่สามารถมีได้สองไพเพอร์ ลำดับและการจัดวางในสูตรจึงเป็นไปตามชื่อที่กำหนด
ตัวอย่างที่ 1: แบเรียม นิกเกิล ไพโรฟอสเฟต II
เกลือนี้มีฟอสเฟต (P2อู๋7), แบเรียม (Ba+2) และนิกเกิล II (Ni+2) ไพเพอร์ที่เขียนในลำดับนั้น ดังนั้นสูตรของมันคือ BaNiP2อู๋7.
ตัวอย่างที่ 2: ทองแดง II ฟอสเฟตและทองคำ I
เกลือนี้มีฟอสเฟต (PO4-3), ทองแดง II (Cu+2) และ ทอง ฉัน (Au+1) ไพเพอร์ที่เขียนในลำดับนั้น ดังนั้นสูตรของมันคือ CuAuPO4.
b) สำหรับเกลือสองเท่าที่มีประจุลบสองตัว
ในกรณีที่ เกลือคู่ ด้วยแอนไอออนสองตัว เรายังทำตาม เมื่อวางแอนไอออนในสูตร ลำดับตามที่ปรากฏในชื่อที่กำหนด
ตัวอย่างที่ 1: นิกเกิลซัลเฟต-ไอโอไดด์ III
เกลือนี้มีแอนไอออนซัลเฟต (SO4-2) และไอโอไดด์ (I-1) เขียนในลำดับนี้และไอออนบวกของนิกเกิล III (Ni+3). ดังนั้นสูตรของมันคือ NiSO4ผม.
ตัวอย่างที่ 2: ตะกั่วไซยาไนด์ฟอสเฟต IV
เกลือนี้มีแอนไอออนฟอสเฟต (PO4-3) และไซยาไนด์ (CN-1) เขียนในลำดับนี้และไอออนบวก IV (Pb+4). ดังนั้นสูตรของมันคือ PbPO4ซีเอ็น.
By Me. ดิโอโก้ โลเปส ดิอาส
คุณต้องการอ้างอิงข้อความนี้ในโรงเรียนหรืองานวิชาการหรือไม่ ดู:
DAYS ดิโอโก้ โลเปส "เกลือสองเท่าคืออะไร"; โรงเรียนบราซิล. มีจำหน่ายใน: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm. เข้าถึงเมื่อ 28 มิถุนายน 2021.
การตั้งชื่อเกลือ การจำแนกเกลือ ชื่อไอออน ชื่อไอออนบวก เหล็กซัลเฟต เฟอร์รัสซัลเฟต ไนเตรต ของเงิน โพแทสเซียมคลอไรด์ โซเดียมคลอไรด์ แคลเซียมคลอไรด์ ซิลเวอร์ไนเตรต คอปเปอร์ซัลเฟต คาร์บอเนต แคลเซียม.
เคมี

เกลือในชีวิตประจำวัน แคลเซียมคาร์บอเนต โซเดียมคลอไรด์ โซเดียมฟลูออไรด์ โพแทสเซียมไนเตรต โซเดียมไนเตรต โซเดียม, โซเดียมคาร์บอเนต, โซเดียมไบคาร์บอเนต, โซเดียมไบคาร์บอเนต, โซเดียมซัลไฟต์, ดินประสิว, โซดา.

