Ett substitutionsreaktion den är baserad på utbytet mellan komponenter i två olika reagens. Föreningar med större stabilitet (mättad, det vill säga med endast enkla bindningar mellan kol) är mer benägna att genomgå denna process. Men bensen kan också göra det.
Vi vet att i strukturen av bensen det finns tre dubbelbindningar (tre pi-bindningar), det vill säga denna förening är omättad, men dessa dubbla genomgår fenomenet resonans (alternering av positionen för de tre pi-bindningarna) hela tiden. Av denna anledning har dess struktur större stabilitet, eftersom obligationerna passerar genom alla kol.
De substitutionsreaktioner som kan förekomma i bensen är:
Halogenering;
Nitrering;
Sulfonering;
Alkylering;
Acylering.
a) Halogenering
I denna reaktion samverkar bensen med halogener (Br2Cl2 Hallå2), alltid med närvaron av en katalysator, som kan vara ett oorganiskt salt (AlCl3FeCl3 och FeBr3). Processen sker med utbyte av ett bensenväte mot en halogenatom. Resultatet är bildning av en organisk halogenid och en halogenerad hydrid. Se ett exempel:
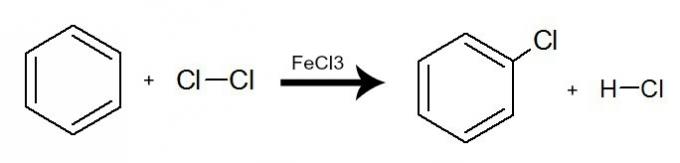
Ekvation som representerar en halogenering av bensen genom användning av molekylärt klor (Cl2)
b) Nitrering
I denna reaktion interagerar bensen med salpetersyra (HNO)3), alltid med närvaron av svavelsyrakatalysatorn (H2ENDAST4) och uppvärmning. Processen sker med utbytet av ett väte från bensen mot NO-gruppen2 av syran. Resultatet är bildande av en nitroförening och vatten.
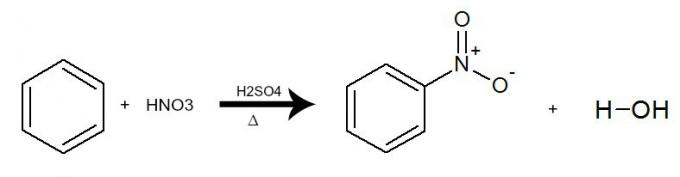
Ekvation som representerar nitreringen av bensen genom användning av salpetersyra
c) Sulfonering
I denna reaktion samverkar bensen med svavelsyra (H2ENDAST4), alltid med närvaron av svaveltrioxidkatalysatorn (SO3) och uppvärmning. Processen sker med utbytet av väte från bensen med SO-gruppen3H syra. Resultatet är formation av syra sulfonisk och vatten.
Sluta inte nu... Det finns mer efter reklam;)
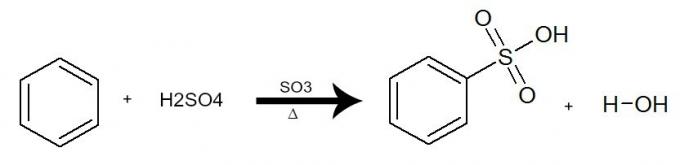
Ekvation som representerar en sulfonering av bensen genom att använda svavelsyra
d) Alkylering
I denna reaktion samverkar bensen med a organisk halogenid (R-X), alltid med närvaron av katalysator aluminiumtriklorid (AlCl3) och uppvärmning. Processen äger rum med utbytet av väte från bensen med R-gruppen (organisk substituent) från halogeniden. Resultatet är bildning av ett grenat aromatiskt kolväteoch en oorganisk syra (HX).
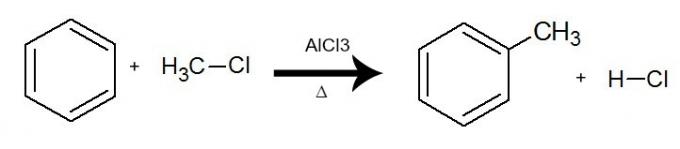
Ekvation som representerar en alkylering av bensen med användning av klormetan
e) Acylering
I denna reaktion samverkar bensen med en syrahalogenid, som kan representeras av etanolklorid:
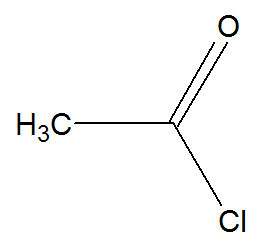
Strukturformel av etanoylklorid
Reaktionen sker med närvaron av katalysator aluminiumtriklorid (AlCl3) och det sker ett utbyte av ett väte från bensen mot hela syrahalogenidgruppen (med undantag av X-halogen). Resultatet är bildande av en keton och en oorganisk syra (HX). Se ett exempel:
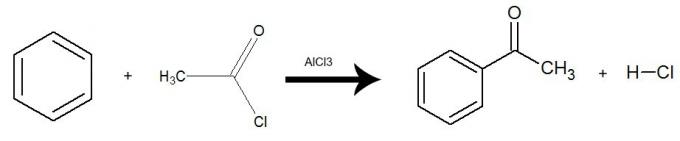
Ekvation som representerar en acylering av bensen genom användning av etanolklorid
Av mig Diogo Lopes Dias
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
DAGAR, Diogo Lopes. "Substitutionsreaktioner i bensen"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm. Åtkomst den 27 juni 2021.
Kemi

Aromatiska föreningar, aren, polaritet, olösliga, lösliga, icke-polära lösningsmedel, eter, koltetraklorid, kolväten, insekticider, färgämnen, lösningsmedel, sprängämnen, cancerframkallande ämnen, toluen, metylbensen, läkemedel, lim skomakare.
Kemi

Klicka här och lär dig mer om substitutionsreaktion, en kemisk process där de använda reagensen (organiska och oorganiska) utbyter en av dess komponenter med varandra och bildar nya ämnen. Bland de ämnen som mest används som reagens är alkaner, bensen och organiska halider.