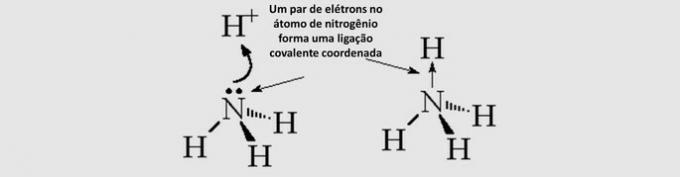
På organiska eliminationsreaktioner är de i vilka atomer eller grupper av atomer i en molekyl avlägsnas eller elimineras från den, skapa en ny organisk förening, förutom en oorganisk förening som bildas av den del som var raderade.
En typ av eliminationsreaktion är uttorkning, där molekylen som går förlorad är vatten. Dehydrering av alkoholer (föreningar som har OH-gruppen bunden till ett mättat kol i en öppen kedja) kan ske på två sätt: intramolekylär och intermolekylär.
"Intra" betyder "inuti", därför den intramolekylära uttorkningen av alkoholer inträffar när en vattenmolekyl går ut från "inuti" själva alkoholmolekylen. I detta fall kommer den organiska produkten som bildas att vara en alken.
Denna reaktion äger rum endast i närvaro av en katalysator som fungerar som ett torkmedel och för det mesta är den koncentrerad svavelsyra (H2ENDAST4) och temperaturen bör vara cirka 170 ° C.
Exempel:
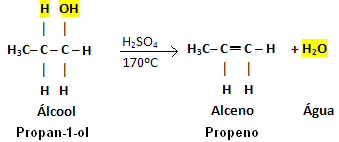
Observera att OH-gruppen lämnade och väte lämnade det angränsande kolet, vilket gav upphov till vatten. Dessutom skapades dubbelbindningen som gav upphov till alkenet.
Anläggningen att drabbas av uttorkning följer följande fallande ordning:
Tertiära alkoholer> Sekundära alkoholer> Primära alkoholer
Men hur är det när OH-gruppen kommer mitt i kolkedjan? Väteatomen från vilken angränsande kolatom frigörs och bildar vattenmolekylen?
Sluta inte nu... Det finns mer efter reklam;)
Till exempel är nästa 2-metylpentan-3-ol. Observera att en angränsande kolatom är tertiär (markerad i rött), medan den andra är sekundär (markerad i blått):
H OH H
│ │ │
H3C - Ç ─ Ç ─ Ç CH3
│ │ │
H H CH3
Vätet bundet till den tertiära kolatomen blir lättare att lämna, eftersom dess elektronegativa karaktär är lika med δ+1Ju mindre negativ karbon karaktär är, desto svagare är bindningen mellan dem och desto lättare blir det att bryta deras bindning.
I sådana fall bildas alla möjliga föreningar, men övervägande kommer att ges i ordningen: Tertiära alkoholer> Sekundära alkoholer> Primära alkoholer.
Så vi har:
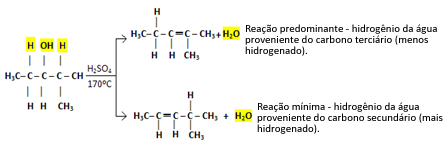
Denna typ av reaktion lyder Saytzefs regel, som säger det det kommer att finnas en större tendens för väte att lämna kol mindre hydrerat. Denna regel är precis motsatsen till Markovnikovs regel används för additionsreaktioner.
För att komplettera din kunskap om detta ämne, läs även texten "Intermolekylär uttorkning av alkoholer”.
Av Jennifer Fogaça
Examen i kemi
Vill du hänvisa till texten i en skola eller ett akademiskt arbete? Se:
FOGAÇA, Jennifer Rocha Vargas. "Intramolekylär uttorkning av alkoholer"; Brasilien skola. Tillgänglig i: https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm. Åtkomst den 28 juni 2021.