Molekyl är en uppsättning atomer, samma eller olika, förenade med kovalenta bindningar.
Dessa kemiska ämnen är elektriskt neutrala och representerar den bildande enheten för ett ämne.
Det finns enkla molekyler som syre (O2) av luften vi andas in. Det finns emellertid också komplexa föreningar, såsom buckyballs (60 kolatomer bundna i en sfärform), som är de största molekylerna som någonsin hittats i rymden.
Molekylstudie
Kovalent bindning i en molekyl motsvarar delningselektroner, vanligtvis mellan icke-metalliska element.
Se vattenmolekylen som ett exempel på en enkel förening.
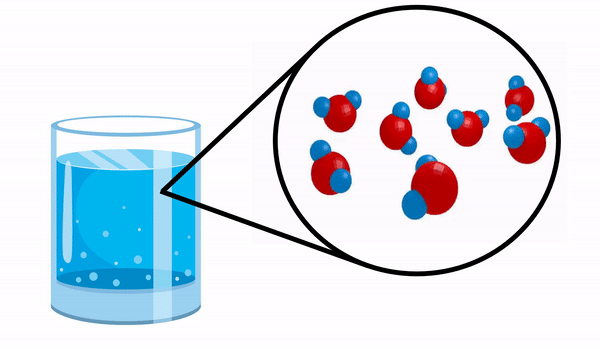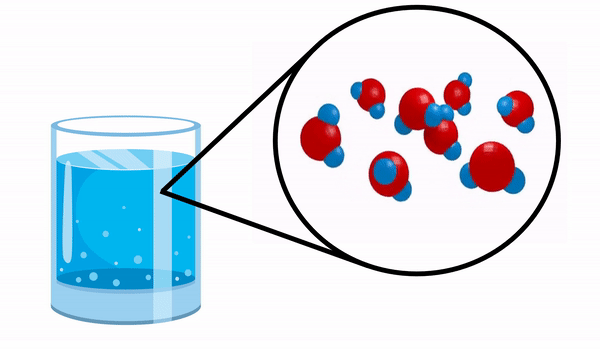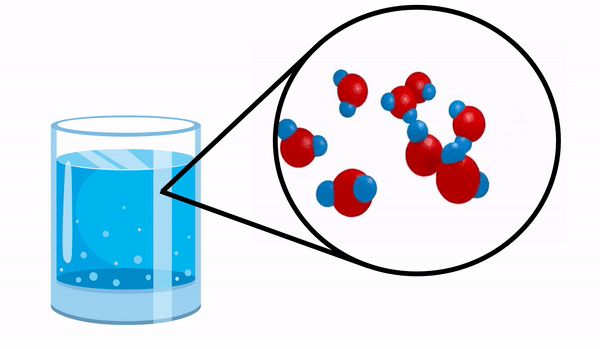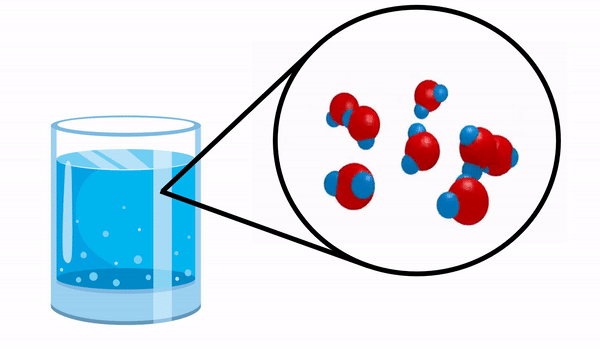
När vi observerar ett glas med Vatten vi har ingen aning om att detta ämne består av flera H-molekyler2O. Denna formel indikerar att vatten består av 3 atomer: två väte- och en syreatomer, som delar elektroner med varandra.
Socker, som vi använder för att sötna juice och göra kakor, består också av molekyler. Den bildande enheten av socker är sackaros.

Denna molekyl är mycket mer komplex, eftersom det finns 45
atomer ansluten. Den bildas av: 12 kolatomer, 22 väteatomer och 11 syreatomer.Molekyler är strukturer med känd molekylvikt, men det finns också makromolekyler, som är "jätte strukturer" bildade av så många atomer att deras sammansättning till och med är odefinierad. Ett exempel på denna typ är diamant, en makromolekyl bildad av många atomer av kol i ett kovalent nätverk.
Kovalent bindning
En kovalent kemisk bindning upprättas mellan två atomer när de delar sina elektroner mer extern (av valens). Molekyler kan ha två typer av bindningar:
Molekylär kovalent bindning: paret elektroner av de två bindningsatomerna delas.

Kovalent kovalent bindning (dativ): de delade elektronerna kommer från endast en av de inblandade atomerna.
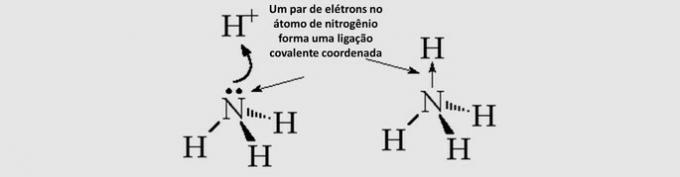
Molekylär geometri
När en molekyl bildas placeras atomerna på olika sätt så att det rumsliga arrangemanget blir mer stabilt. Därför har kompositer olika geometrier.
Här är några av de geometrier som molekyler kan ha.
| Molekylär geometri | ||
|---|---|---|
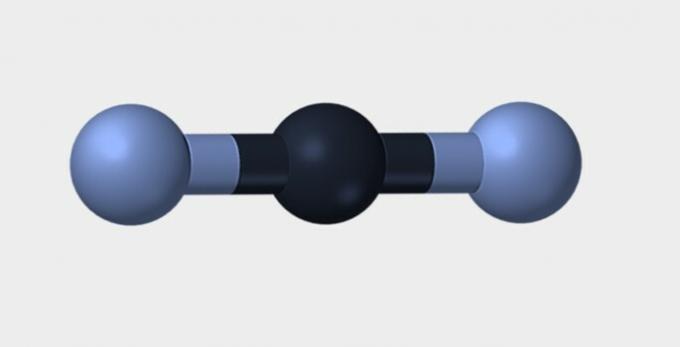
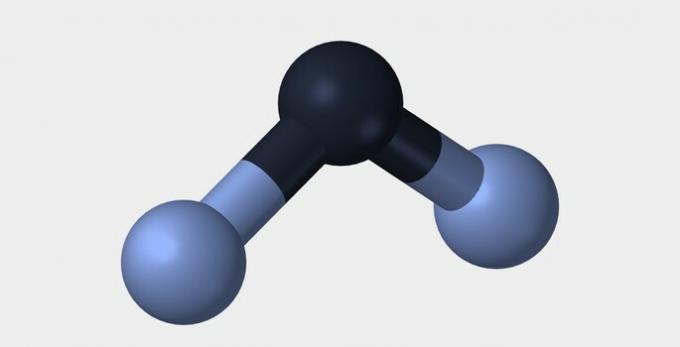
| Linjär | Vinkel | Triangulärt |
 |
 |
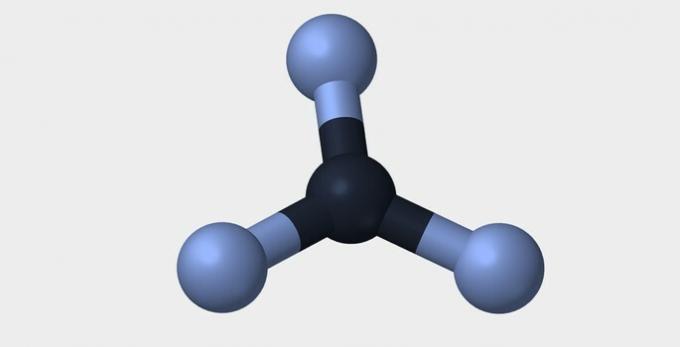 |
| Pyramidal | tetrahedral | oktaedrisk |
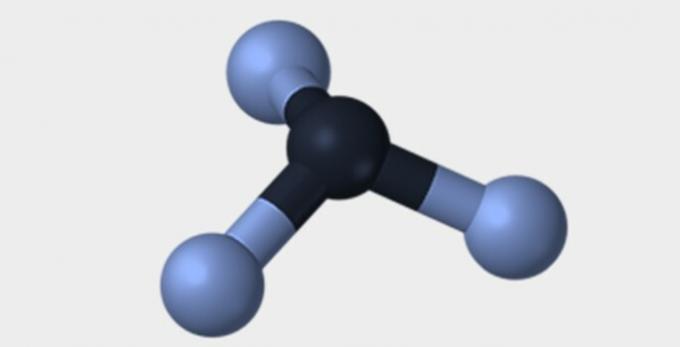 |
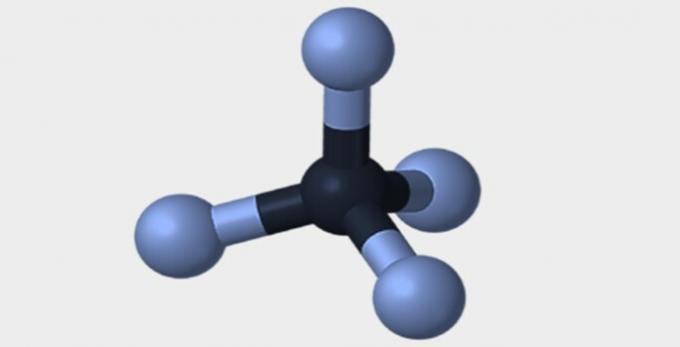 |
 |
Polära och opolära molekyler
Molekyler klassificeras enligt polaritet.
icke-polära molekyler: det finns ingen skillnad i elektronegativitet mellan atomer.
| Kväve (N2) | koldioxid (CO2) |
|---|---|
 |
 |
Kväve (N2) är en icke-polär molekyl eftersom den bildas av den. kemiskt element och därför finns det ingen skillnad i elektronegativitet. koldioxid (CO2) är opolärt på grund av dess linjära geometri, vilket stabiliserar syrgasattraktionen av elektroner.
polära molekyler: det finns en skillnad i elektronegativitet mellan atomerna, med en positiv pol och en negativ pol.
| Vatten (H2O) | Ammoniak (NH3) |
|---|---|
 |
 |
I båda exemplen ser vi att de centrala atomerna, syre och kväve, har oparade elektronpar som bildar elektronmoln. Eftersom det finns fler elektroniska moln runt de centrala atomerna än det finns etablerade kemiska bindningar, är molekylerna polära.
Exempel på molekyler
| Ämne | Funktioner | Molekyl | Formel |
|---|---|---|---|
| Väte | Bränsle och rikligt i jordskorpan. | 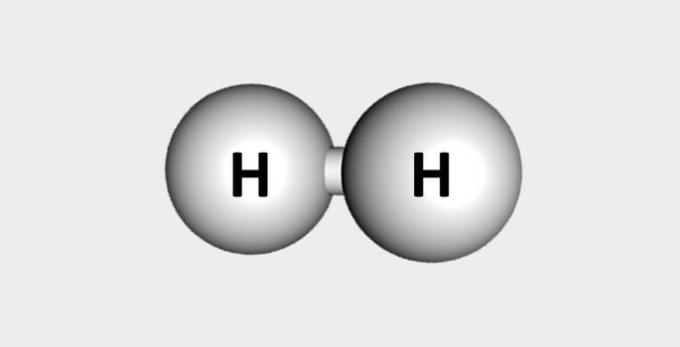 |
H2 |
| Syre | Viktigt för andning och deltar i olika kemiska reaktioner | 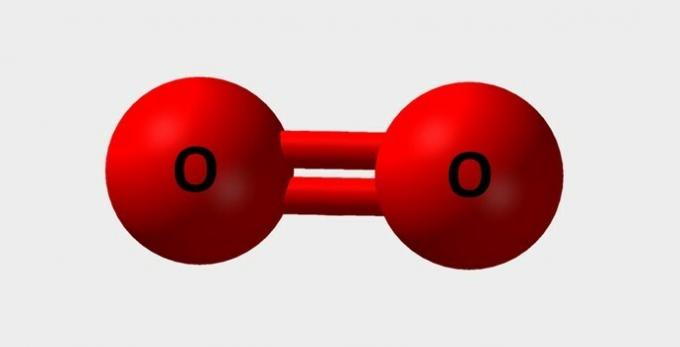 |
O2 |
| Svavel | Gult pulver som används för att göra färgämnen. | 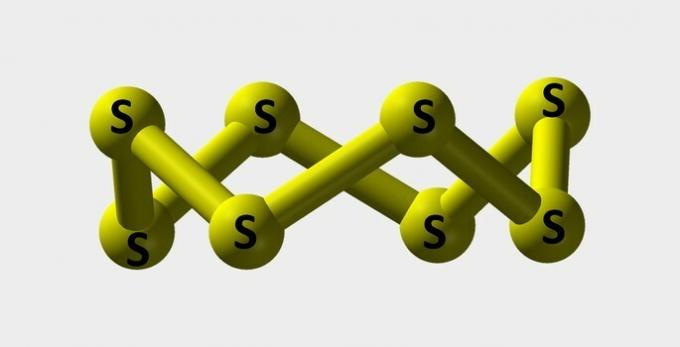 |
s8 |
| Koldioxid | Används i brandsläckare och köldmedier. | 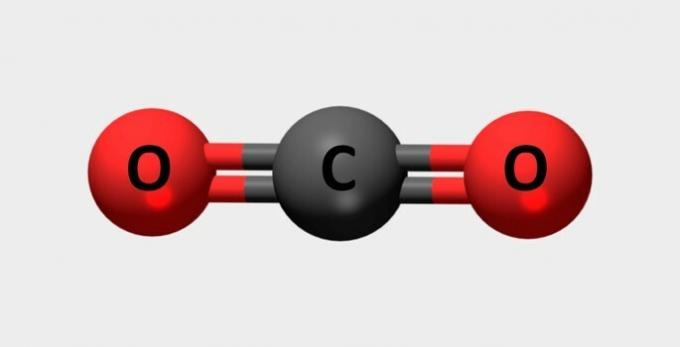 |
CO2 |
| Etanol | Vanlig alkohol som används som bränsle och i parfymer. | 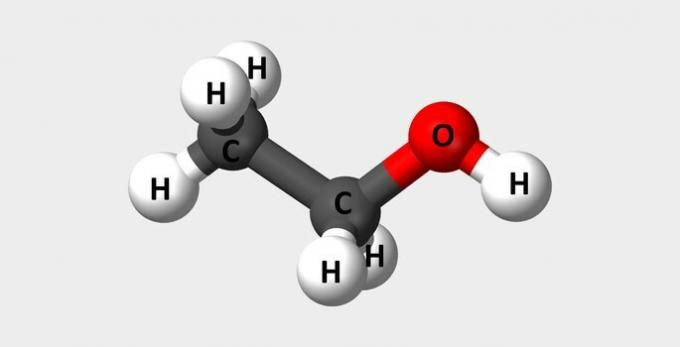 |
Ç2H6O |
Var noga med att kolla in dessa texter om ämnen relaterade till vad du just har lärt dig:
- Biomolekyler
- Organiska föreningar
- Molekylär massa
- Octet Rule
- Kemiska bindningar
- Anslutningens polaritet
- Intermolekylära krafter