се зове јонски сноп величине јона. Проучавање овог својства зависи од знања о атомском радијусу и јонима.
Атомски радијус: је мера величине неутралног атома (теоријска удаљеност од језгра до последње електросфере).
јони: атоми који губе (катиони) или добијају електроне (ањони).
Протони унутар језгра а атом врше привлачну силу на електроне (негативне честице) присутне у електросферама. Што је већи број протона, већа је ова привлачност и обрнуто. Када се број електрона у атому модификује губитком или добитком ових честица, привлачење између протона и електрона се мења на следећи начин:
У случају катиона:
Број електрона у електросферама постаје мањи од броја протона унутар језгра, што чини привлачну силу језгра већом, привлачећи електроне ближе њему. електросфере. Резултат је смањење радијуса атома. Дакле, радијус катиона увек ће бити мањи од радијуса његовог неутралног атома.
Полупречник неутралног атома> Радијус катјона
У случају аниона:
Број електрона у електросферама постаје већи од броја протона унутар језгра. У овом случају, сила привлачења коју језгро делује превазилази сила одбијања између електрона присутних у електросферама, што резултира повећањем радијуса атома. Дакле, радијус аниона ће увек бити већи од радијуса његовог неутралног атома.
Не заустављај се сада... После оглашавања има још;)
Радијус аниона> Полупречник неутралног атома
Две ситуације представљене у наставку су добар пример онога што се догађа са радијусом јона:
1. Неутрални атом натријума (11На) и натријум катион (11У+)
Док неутрални атом натријума има једанаест протона (жуте сфере) и једанаест електрона (црвене сфере), натријум катион има једанаест протона и десет електрона.

Модел неутралног атома натријума
Када неутрални атом натријума изгуби електрон, радијус се смањује.
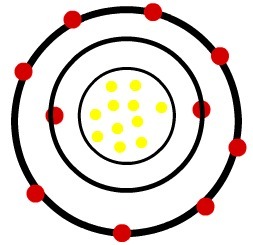
Модел натријумовог катјона
Посматрање: Трећи ниво није представљен на слици катиона, јер је, пошто је изгубио једини електрон који је имао, постао празан и, према томе, занемарен, али је присутан.
2.) Фосфорни неутрални атом (15П) и фосфорни катион (15П.-3)
Док неутрални атом фосфора има петнаест протона (жуте сфере) и петнаест електрона (црвене сфере), фосфорни анион има петнаест протона и осамнаест електрона.
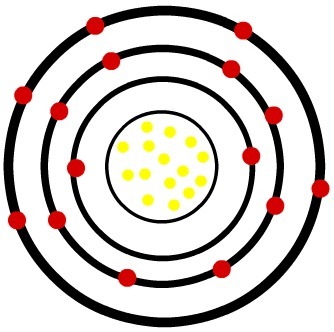
Модел неутралног атома фосфора
Када неутрални атом фосфора добије три електрона, радијус се повећава.
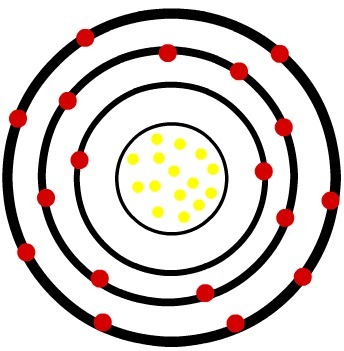
Модел ањона фосфора
Ја сам, Диого Лопес Диас
Да ли бисте желели да се на овај текст упутите у школи или у академском раду? Погледајте:
ДАНИ, Диого Лопес. „Јонски радијус“; Бразил Сцхоол. Може се наћи у: https://brasilescola.uol.com.br/quimica/raio-ionico.htm. Приступљено 28. јуна 2021.