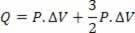карбоксилне киселине су органска једињења која имају карбоксилну функционалну групу, односно угљеник који ствара двоструку везу са кисеоником и једноструку везу са ОХ групом.
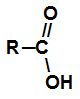
Карбоксил је функционална група сваке карбоксилне киселине
Термин карбоксилне киселине се користи за означавање кисеоничне органске функције, односно оне која у својој структури има атом кисеоника. Једињења која припадају овој групи имају корозивну способност и киселкасти укус, јер су кисела.
Карактеристике карбоксилних киселина
Уопштено говорећи, растворљиви су у органским растварачима;
Једине карбоксилне киселине растворљиве у води су оне које у својој структури имају до четири атома угљеника;
Генерално, карбоксилне киселине су гушће од воде, са изузетком киселина са једним или два атома угљеника;
Карбоксилне киселине које имају до девет угљеника су течне на собној температури;
У чврстом стању су беличасте боје и имају воштани (воштани) изглед;
У течном стању су безбојне;
Како имају карбоксил, они могу да се утврде водоничне везе;
Његова једињења су поларна;
Генерално су без мириса, са изузетком киселина са до три угљеника која имају иритантни мирис и оних са до шест угљеника који имају одвратан мирис;
владавина номенклатура за карбоксилне киселине
Да би се извршила номенклатура а карбоксилне киселине, Међународна унија чисте и примењене хемије (ИУПАЦ) утврђује следеће правило:
Киселина
+
префикс (односи се на број угљеника у ланцу)
+
инфикс (односи се на врсту веза између атома угљеника)
+
Здраво цо
Погледајте неке примере:
Карбоксилна киселина са шест атома угљеника
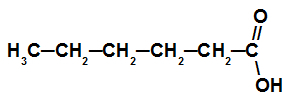
Ова киселина има ланац са шест атома угљеника (префикс хек), само једноструке везе (инфик ан) и карбоксил (оиц), па је њено име хексанска киселина.
Карбоксилна киселина са седам атома угљеника
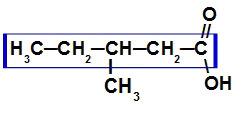
Како је ова киселина разграната, главни ланац је онај са највећим бројем угљеника и карбоксила. У овом једињењу главни ланац има пет атома угљеника (префикс пент), само једноструке везе између атома угљеника (инфик ан) и карбоксила (оиц), па је његово име киселина 3-метил-пентаноик.
БЕЛЕШКА: Нумерисање главног ланца мора увек да започиње од карбоксилног угљеника.
Карбоксилна киселина са два карбоксила
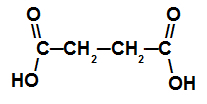
Ова киселина има ланац са четири атома угљеника (префикс али), само једноструке везе између атома угљеника (инфикс ан) и два атома карбоксила (диок), па је отуда и његово име киселина бутандиојска киселина.
БЕЛЕШКА: Између инфикса и „диоика“ додат је повезујући самогласник.
Хемијске реакције са карбоксилним киселинама
Тхе) реакција естерификације
То је хемијска реакција у којој карбоксилна киселина реагује са а алкохол и чине један естер и вода, као што је приказано у следећој једначини:

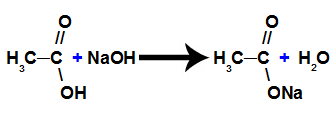
б) Реакција салификације
То је хемијска реакција у којој карбоксилна киселина реагује са неорганском базом и формира сол карбоксилне киселине и воде, као што је приказано у следећој једначини:
ц) реакција елиминације
У овој реакцији се два молекула карбоксилне киселине дехидрирају, што резултира а анхидрид и вода, као што је приказано у следећој једначини:

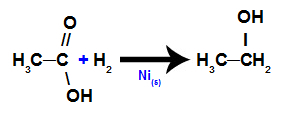
г) Смањење карбоксилних киселина
У овој реакцији, карбоксилна киселина се подвргава медијуму који садржи гас водоник (Х2) и чврсти никл, што резултира стварањем алкохола, као што је приказано у следећој једначини:
Примене карбоксилних киселина
Производња органских естара;
Производња соли карбоксилне киселине;
Припрема парфема;
Производња сирћета;
Производња вештачке свиле;
производња дезинфицијенса;
Бојење тканина.
Ја сам, Диого Лопес Диас
Извор: Бразил Сцхоол - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-acidos-carboxilicos.htm