Полимеризација је назив хемијског процеса који резултира формирањем макромолекула (великих молекула) названих полимери, кроз комбинацију мањих молекула, мономера.
реакција на полимеризација веома је уобичајен у природи, као што можемо видети у угљеним хидратима (као скроб) и протеинима (као казеин у млеку). Такође се јавља синтетички, пошто је огромна већина полимера које људска бића користе у свакодневном животу направљена вештачки.
Први полимер произведен од полимеризација синтетички је бакелит, 1909. године, од стране белгијског хемичара Леа Хендрика Бекеланда.
Генерално, да би се мономер комбиновао са другим (било да су исти или различити) у реакцији полимеризација, неопходно је постојање слободне валенције (да се изврши хемијска веза) у оба мономера.
Ове валенце настају као резултат раскидања веза, употребом катализатора (као што је никл), спољашњим условима као што су светлост и топлота, или феноменом резонанције у структури (померањем електрона).
У формирању полипропилена (ПП полимера), на пример, који се користи у кућним посуђем и играчкама,
пи линк (π) у сваком молекулу је подељен на следећи начин: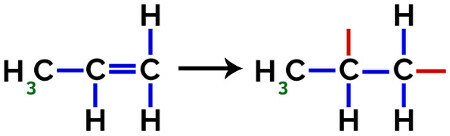
Прекид пи везе у пропилену
Дакле, сваки пропилен мономер може да се повеже са два друга пропилен мономера и формира полимер ПП или полипропилен (префикс поли означава неколико мономерних јединица). Најчешћи начин представљања полимера је мономер између заграда и, споља, слово н, које означава неколико мономера, као што видимо у случају ПП полимера:
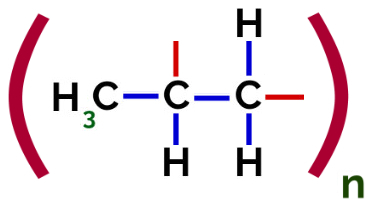
Репрезентација ПП полимера
реакција на полимеризација може се урадити на различите начине, као што ћемо видети у наставку:
а) Реакција на адициона полимеризација
У ово полимеризација, увек долази до прекида пи везе у мономеру, што доводи до појаве две слободне валенце у структури, као у формирању полиетилен, полимер који се широко користи у фармацеутској амбалажи.
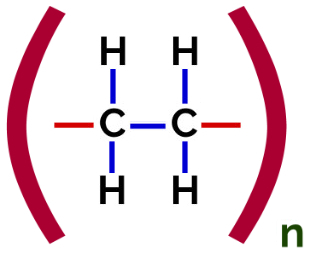
Структурна формула полиетиленског адиционог полимера
Ат полимеризација од полиетилена, молекули етилена (етена), који имају пи везу између два атома угљеника, користе се као мономер. Када је ова веза прекинута, појављују се две слободне валенце, по једна на сваком атому угљеника који је био укључен у пи везу. Мономери се уједињују тачно у свакој од ових валенција, то јест, валенца једног је повезана са валенцијом другог, и тако даље.
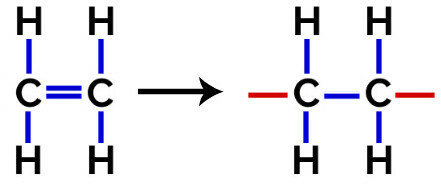
Једначина формирања полиетилена
б) Реакција адиционе полимеризације 1.4
У овој полимеризацији, мономери представљају две наизменичне двоструке везе (једна пи и једна сигма), што фаворизује феномен резонанције (наизменични положај пи електрона пи везе), као у формирању синтетичке гуме (полибутадиен)

Структурна формула полибутадиена
Мономерна јединица овог полимера је бутадиен, који има две наизменичне двоструке везе. Са резонанцом, структура има двоструку везу између угљеника 2 и 3, и две слободне валенције на угљеницима 1 и 4. Управо у овим слободним валенцијама угљеника 1 и 4 мономери се комбинују.

Бутадиенска резонанца
ц) Реакција на кондензациона полимеризација или елиминацију
То је реакција на полимеризација у којој, обавезно, два мономера (исти или различити) истовремено губе атоме или групе, што резултира две слободне валенце у свакој од њих. На овај начин увек долази до елиминације водоника из мономера, који се затим спаја са халогеном (Ф, Цл, Бр, И), ОХ, НХ2или на ЦН другог мономера.
Дакле, у полимеризација елиминацијом увек долази до стварања воде, халогенисане киселине (ХЦл, ХИ, ХФ, ХБр), амонијака (НХ3) или цијановодоничне киселине (ХЦН) поред полимера. Погледајте, на пример, приказ формирања полиестера, материјала који се користи као тканина:

Једначина формирања полиестера
Мономери који формирају полиестер су п-бензендиојева киселина и етан-1,2-диол. То можемо приметити у овоме полимеризација долази до елиминације молекула воде, пошто два мономера имају два хидроксила. У овом процесу, киселина губи два хидроксила, а дијакохол губи само водоник из својих хидроксила:

Структура полиестера
Полиестерским мономерима се придружују кисеоник у алкохолу и угљеник у карбоксилној киселини.
Од мене Диого Лопес Диас
Извор: Бразил школа - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm



