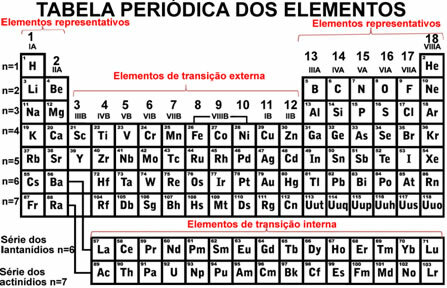
Хлор је хемијски елемент са симболом Цл, атомски број 17, атомска маса 35,5. Припада породици халогена, групи 17 или 7А, и трећем периоду периодног система.
Име му потиче од грчког кхлорос, што значи зеленкасто. То је зато што се у нормалним условима температуре и притиска хлор карактерише зеленкасто-жутим гасом са јаким мирисом.
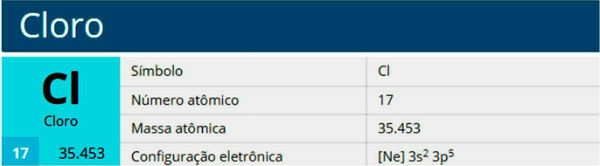
Карактеристике
Хлор је 1774. године открио шведски научник Царл Вилхелм Сцхееле (1742-1786). Међутим, тада сам веровао да је то једињење са кисеоником. 1810. године, Хумпхри Дави (1778-1829) показао је да је то нови хемијски елемент.
Како је реч о изузетно реактивном елементу, у природи се тешко може наћи у свом чистом облику, са изузетком мале количине која се емитује током ерупција вулкана у облику ХЦл.
Стога се обично налази у облику натријум хлорида (НаЦл), такође познатог као кухињска со. У минералима се јавља у облику карналита и силвита.
Такође се може добити путем електролиза НаЦл, у воденом раствору. Хлор такође производи многе соли из хлорида кроз процес оксидација.
Сазнајте више, прочитајте такође:
- Периодни систем
- Хемијски елементи
- Халогени
апликације
Гас хлора (Цл2) је токсичан и иритантан, због овог стања је коришћен као хемијско оружје током 1. светског рата. Овај гас узрокује иритацију респираторног тракта и коже, задржавање воде у плућима, сузење и када се удише у великим количинама може довести до смрти.
Неке друге употребе хлора су:
- Избељивање папира и тканина хлоровим диоксидом (ЦлО2).
- Третман воде, додавањем хлора, чини воду питком и погодном за људску употребу. Овај процес се назива хлорисање и користи се хлороводонична киселина (ХЦлО).
- Дезинфекција воде из базена и индустријског отпада, јер је хлор способан да убије микроорганизме.
- Производња пластичних једињења као што су ПВЦ (поливинил хлорид) и синтетичка гума.
- Производња неких врста органских и неорганских једињења.