Hidrogeniranje poteka z nenasičenimi acikličnimi ogljikovodiki, to je z odprtimi verigami z dvojnimi ali trojnimi vezmi, kot so alkeni, alkini in dieni. Lahko se pojavi tudi v aromatskih ogljikovodikih, saj imajo v obroču dvojne vezi, in s ciklani (cikloalkani) do pet ogljikov.
Te spojine reagirajo kot plin vodik v prisotnosti katalizatorja, kot so nikelj, platina in paladij, pri segrevanju. Tako pride do adicijske reakcije, pri kateri se pi (π) vez pretrga in tvori dve novi enojni vezi in molekul vnese vodik.
Na splošno imamo:
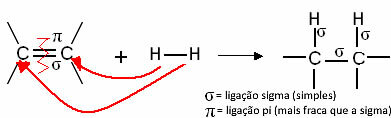
Splošna reakcija hidrogeniranja
Zdaj pa si oglejmo nekaj primerov:
- Hidrogeniranje v alkene: Dobljeni izdelek je alkan.
Spodaj imamo reakcijo hidrogeniranja etilena (ali etilena), da dobimo etan:
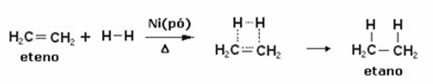
Primer reakcije hidrogeniranja etilena
To vrsto katalitskega hidrogeniranja živilska industrija uporablja za izdelavo poltrdnih maščob, kot so margarine. Rastlinska olja in maščobe se razlikujejo le po tem, da imajo olja dolge molekule z dvojnimi vezmi med ogljiki, medtem ko imajo maščobe le enojne vezi med svojimi ogljiki.
Za pretvorbo olja v maščobo je torej dovolj, da olje hidrogeniramo. Tako bodo vaše dvojne vezi pretrgane in pretvorjene v enojne. Rezultat je proizvodnja klicev hidrogenirane rastlinske maščobe.
- Hidrogeniranje alkina: Ker imajo alkini dve pi vezi, njihovo popolno hidrogeniranje poteka v dveh stopnjah, v prvi nastane alken, v drugi pa alkan.
V spodnji reakciji imamo hidrogeniranje propina s končno tvorbo propana:
1. korak: H3C C ≡ CH + H2 → H3C CH═ ÇH2
2. stopnja: H3C CH═ ÇH2 + 2 uri2 → H3C CH2─ ÇH3
Če želimo, da se ta reakcija ustavi v prvem koraku, moramo uporabiti nekaj snovi, ki prekine delovanje katalizatorja.
- Hidrogeniranje diena: Obstajajo tri vrste diena: nakopičene (dvojne obveznice so prikazane spodaj), izoliran (dvojne vezi so ločene z vsaj dvema enojnima vezema) in konjugati (dvojne vezi se pojavljajo izmenično).
Hidrogeniranje nakopičenih in izoliranih dienov poteka na enak način, kot smo ga videli pri alkenih, vendar dvojno, saj so dieni bolj nenasičeni. Oglejte si dva primera:
* Primer hidrogeniranja v nakopičenem dieni:
H H H
│ │ │
H3C CH ═ Ç ═ CH CH3 + 2 uri2 → H3C CH ─ Ç ─ CH CH3
│ │ │
H H H
* Primer hidrogeniranja v izoliranem dieni:
H H H H
│ │ │ │
H3C CH ═ CH─CH2 CH ═ CH CH3 +2 H2 → H3C CH ─ CH─CH2 CH ─ CH CH3
Po drugi strani pa lahko hidrogeniranje konjugiranih dienov poteka na dva načina: z dodatkom 1,2 in dodatkom 1,4. Najpogostejši je dodatek 1,2, pri katerem se vodiki dodajo ogljikom, ki tvorijo dvojno vez, in pri nizkih temperaturah. Dodatek 1,4 pa se pojavi pri povišanih temperaturah in je takrat, kadar v ogljikih 1 in 4 pride do resonance in pojava prostih valenc. Oglejte si primere vsakega primera:
* Primer dodajanja 1,2 v konjugiranih dienih:
H2C CH CH ═ CH2 + H2 → H2C CH ─ C ─ CH ═ CH2
│ │
H H
* Primer dodatka 1.4 v konjugiranih dienih:
H2C CH CH ═ CH2 + H2 → H2C CH ═ CH CH2
│ │
H H
- Hidrogeniranje aromatov: Pi vezi benzenskega obroča se pretrgajo in vodikovi atomi se dodajo ogljikom, ki tvorijo te vezi.
Ta vrsta celotnega hidrogeniranja je prikazana spodaj:

Reakcija skupnega hidrogeniranja benzena
- Ciklonsko hidrogeniranje: Pojavi se tvorba alkana.
Primer: Hidrogeniranje ciklopropana:
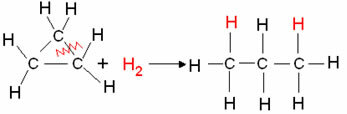
Reakcija hidrogeniranja ciklopropana
Avtorica Jennifer Fogaça
Diplomiral iz kemije
Vir: Brazilska šola - https://brasilescola.uol.com.br/quimica/reacao-organica-hidrogenacao.htm
